类器官培养 50 问-基础篇
dxy_r0meq856
Q1: 类器官培养对于起始细胞的来源有要求吗?
A1: 目前培养的类器官主要来源于上皮细胞,对于非上皮细胞来源的类器官培养方式还需要进一步研究。
Q2: 类器官按照起始细胞的类型,分为几种呢?
A2: 常见的类器官根据起始细胞的类型,可以分为两种:
(1)肿瘤组织来源的肿瘤类器官;
(2)干细胞来源的类器官,包括:多能性干细胞 (PSC) /成体干细胞 (ASC)以及诱导多能干细胞(iPSC)。
Q3: 类器官是由单一种类细胞组成的吗?
A3: 类器官并不是单一细胞组成的结构,而是由具有干细胞性质的起始细胞进行分裂和分化,并将多种类型的细胞自组装的结构,自组装后的形态和功能与体内相应器官相似。
Q4:在没有新鲜组织的情况下,可以用冻存组织提取的原代细胞进行 3D 培养吗?
A4:可以的。已有学者验证过,将人结肠癌、甲状腺癌、肺癌、肾癌和肝癌的手术组织切碎后,以梯度降温的方式进行冷冻,最终在液氮中保存 15-18 个月后进行复苏和原代细胞提取,分别对细胞进行 2D 和 3D 培养,证实了冻存对于细胞活力和生长速度均无显著影响【1】。
当然,由于组织来源不同、冻存条件不同,还需要大家根据实际情况进行验证,新鲜组织提取的细胞依然是 3D 培养的最佳选择。
Q5:类器官可以像细胞一样进行冻存和复苏吗?
A5:类器官可以冻存,通常会在传代 2-3 次之后选择冻存。为了达到最佳的效果,可以选择类器官成熟(传代 7-10 次)后再进行冻存。
Q6:类器官的尺寸需要进行控制吗?
A6:是的,主要的原因是类器官内部缺乏循环系统。
当类器官的尺寸较大时,靠近中心的细胞难以和外界进行氧气和营养成分的交换。因此这个结构尺寸越大,死亡的细胞就越多(如图 1)【2】。我们在培养的过程中,需要控制类器官的大小在 4-5mm 以内。未来的类器官技术可以与血管类器官结合在一起,建立一个功能性的封闭循环系统,用以培养出更大尺寸的类器官。
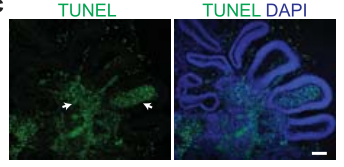
图 1. TUNEL 染色表明较大尺寸的类器官中心有大量细胞死亡(绿色),比例尺为 100μm【2】
Q7:类器官传代的标准是什么?
A7:类器官的传代通常是根据培养的时间判断。
一般在 7-14 天时进行第一次传代,后续则每 7-10 天传代一次【3】。
Q8:类器官可以进行多少次传代?
A8:大部分类器官可以在体外连续传代 10次(>6 个月),甚至有些类器官可以连续传代 20 次(>12 个月)并且维持原有的生长速度【4】。
Q9: 鉴定类器官的方法有哪些?
A9: 初步可以通过显微镜和 H&E 染色观察形态;然后可以用 Western Blot、qRT-PCR、免疫荧光、流式细胞术检测该类器官是否表达相应的 biomarker;基因测序可以鉴定所培养的类器官是否有某些特征丢失;对于部分类器官,还可以检测其是否具有功能,例如:已有研究检测出胃类器官可以分泌胃酸,心脏类器官可以自主跳动。
Q10: 类器官是如何按照我们的意愿进行定向分化的?
A10: 在进行类器官培养前,我们需要了解该器官在体内的发育过程,及早期发育相关的信号通路。
以胃类器官培养为例:胃由前后肠发育而来,早期发育需要由多种信号通路共同调控。那么在体外我们需要通过添加细胞因子的方式,指导激活/抑制相应的信号通路,来达到相同的效果,如: PSCs 在 Activin A 的作用下分化为内胚层,Wnt3a、FGF-4 和 Noggin 指导细胞向向前肠分化【5】。
参考文献
【1】He, A. et al. (2020). Cryopreservation of viable human tissues: Renewable resource for viable tissue, cell lines, and organoid development. Biopreservation and Biobanking, 18(3), 222-227.
【2】Lancaster, M. A. et al. (2013). Cerebral organoids model human brain development and microcephaly. Nature, 501(7467), 373-379.
【3】Sheridan, M. A. et al. (2020). Establishment and differentiation of long-term trophoblast organoid cultures from the human placenta. Nature Protocols, 15(10), 3441-3463.
【4】Beshiri, M. L. et al.(2018). A PDX/organoid biobank of advanced prostate cancers captures genomic and phenotypic heterogeneity for disease modeling and therapeutic screening. Clinical Cancer Research, 24(17), 4332-4345.
【5】McCracken, K. W. et al. (2014). Modelling human development and disease in pluripotent stem-cell-derived gastric organoids. Nature, 516(7531), 400-404
7 个回答
龙大人驾到
类器官培养对于起始细胞的来源通常有一定的要求。
起始细胞是指用于培养类器官的初始细胞群体,它们具有分化为特定器官类型的潜力。起始细胞可以来自不同的来源,例如胚胎组织、成体组织或干细胞。
具体要求取决于所要培养的类器官类型以及培养的目的。以下是一些常见的起始细胞来源和要求:
胚胎来源:起始细胞可以来自胚胎的早期发育阶段,例如胚胎干细胞。这些细胞具有广泛的分化潜能,可以分化为多种器官类型。然而,使用胚胎干细胞存在伦理和法律上的限制。
成体来源:起始细胞也可以来自成体组织,如器官的干细胞或多能细胞。这些细胞具有一定的分化潜能,可以分化为特定的器官类型。在这种情况下,起始细胞的获取可能需要特定的技术和方法。
诱导多能干细胞来源:另一种选择是使用诱导多能干细胞(induced pluripotent stem cells,iPSCs)。iPSCs是通过通过基因重新编程将成体细胞(如皮肤细胞)转变为类似胚胎干细胞的细胞。这些细胞可以分化为多种器官类型,并且可以从患者本身获得,具有个体化医疗的潜力。
总之,起始细胞的选择取决于所要培养的类器官类型、研究目标和可用的资源。不同的起始细胞来源具有不同的特点和优势,研究人员需要根据具体情况进行选择。
飞跃迷雾1
对于这10个问题,你给予了很好的回答,感谢分享
sswei
人工智能全都回答了,不用修改全都正确。
飞翔的小小呆6
问答很全,答案简单易懂,学习了。
feixue7758527w
写的很全面的,来学习一下,保留备存的。
高山云初
问题都是有答案的,感谢科普与分享
土井挞克树
目前最成熟的就是上皮细胞做类器官培养
相关产品推荐
相关问答