相对定量,你的内参选对了吗?
诺唯赞生物
荧光定量 PCR 的主要用途之一是相对定量,而提到相对定量,必然离不开内参,那什么是内参基因?为什么相对定量必须使用内参?如何选择正确的内参基因?今天,我们就来聊聊关于内参的那些事。
什么是内参?
内参基因,也称为管家基因,其编码蛋白是维持细胞基本生命活动所必须的蛋白质。它的表达水平不受任何内源性与外源性因素的影响。管家基因高度保守且在大多数情况下持续表达,稳定表达于不同类型的细胞和组织中。
为什么相对定量必须使用内参?
那内参基因与相对定量又有什么样的关系呢?我们通过以下实验案例一起了解一下。
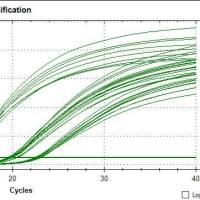
实验目的:测定肝癌细胞 X 基因相对于正常肝细胞的表达量。通过荧光定量检测可得:肝癌细胞中 X 基因的 CT= 25,正常肝细胞中 X 基因的 CT= 26,所以,利用表达量倍数计算公式 2-△CT计算,发现肝癌细胞中的 X 基因表达量是正常肝细胞表达量的 2 倍。

但是,上面这个定量结果检测有效的前提是:必须保证两盘细胞的细胞数量完全一致;RNA 提取、逆转录以及定量效率及操作必须完全一致;不存在操作误差等。这显然是无法达到的。
那如何才能使这些误差不影响 X 基因表达检测的真实性呢?
这时,为了将样本处理归一化,引入一个内参进行校正。基于前面对内参基因特点的描述,我们知道内参基因在两类细胞(正常肝细胞/肝癌细胞)中的表达量是相对一致的,所以可以对细胞上样量、细胞上样过程中存在的误差、实验过程中存在的实验误差等进行校正。再来看一下引入内参后 X 基因的表达量。
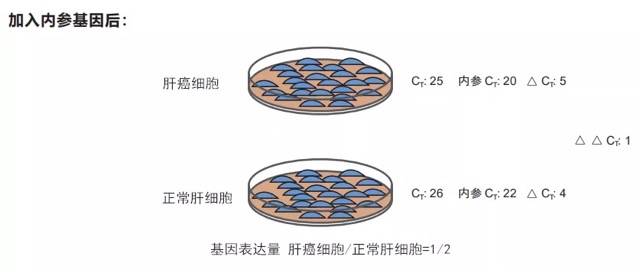
肝癌细胞 X 基因 CT= 25,内参基因 CT= 20;正常肝细胞 X 基因 CT= 26,内参基因 CT= 22。所以,内参校正后,肝癌细胞中的 X 基因表达量是正常肝细胞表达量的 1 / 2 倍(计算公式 2-△△CT)。
由此可见,若想有效检测一个特定基因的相对表达情况,选择内参进行归一化处理非常重要!
如何选择合适的内参?
理想状态下的内参应在各种实验条件下,各种类型的组织和细胞中恒定表达,且表达量稳定。那是否在实验中只要选择一个常见的内参就可以了呢?
我们来看下面这个案例:
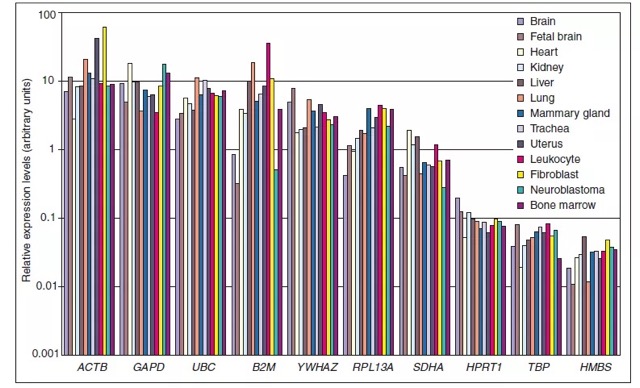
这份资料中描述了不同内参基因在不同的组织中的表达情况。以 B2M 内参基因为例,其在胎儿大脑与白细胞中的表达量相差数百倍。若使用 B2M 对胎儿大脑与白细胞中某一基因的表达量进行校准,得到结果显然是不可信的。
那如何来选择合适的内参呢?
首先,是内参的获得。常见内参获取的途径有如下三个:
途径一:通过查询相关文献,获取内参。
途径二:选择常用的多个内参进行实验验证。较常见内参基因见下图表:
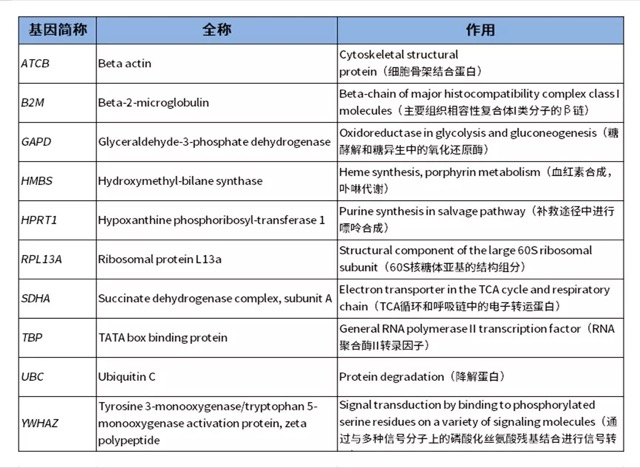
途径三:通过查询 ICG 库,获取内参
网址:http://icg.big.ac.cn/index.php/Homo_sapiens
网站中搜集了文献报道的常见细胞/组织适用的内参。
如 ICG 库中收录的肺癌常见细胞系对应的内参基因有 ACTB、PPIA、PGK1。

其次,是内参的验证。选定的内参是否满足你的实验,是否在你的不同实验组中是稳定表达的呢?
我们先一起来了解下面这个案例:
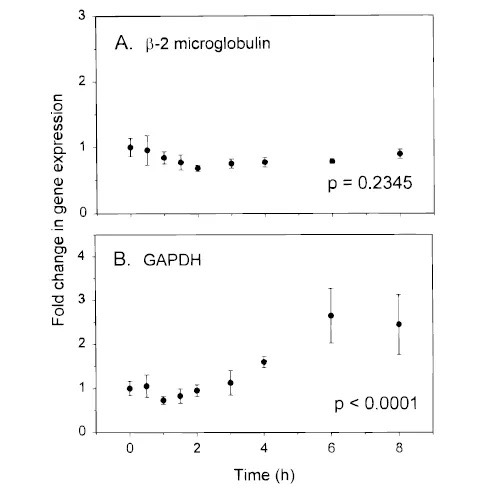
该实验主要目的: NIH3T3 细胞系在无血清培养基中培养 24 h 后,添加 15% 血清,观察 8 h 内特定基因的表达量。本实验选取了两个内参基因:GAPDH 与β-2-microglobulin进行实验验证。
在不同实验组下,通过利用 2-△CT(△CT= CT,Time x - CT,Time 0)计算得到 9 个数据,通过进行统计学分析,判定这 9 个数据差异是否显著。实验结果表明,GAPDH p<0.0001,差异极显著,β-2-microglobulin p = 0.2345,差异不显著。说明 GAPDH 在该实验模型中表达不稳定,不建议将 GAPDH 作为该实验的内参。
通过这个案例可以知道,验证内参时,其一、尽可能选用多个内参同时进行实验;其二、通过在不同样本处理上的表达差异检测情况,来选择合适的内参。
综上所述,在相对定量检测中,最重要的是选择合适的内参基因;而选择合适的内参基因中,最重要的,则是实验内参基因在不同处理间的表达稳定性。选择合适的内参,是相对定量成功的开端!