简介
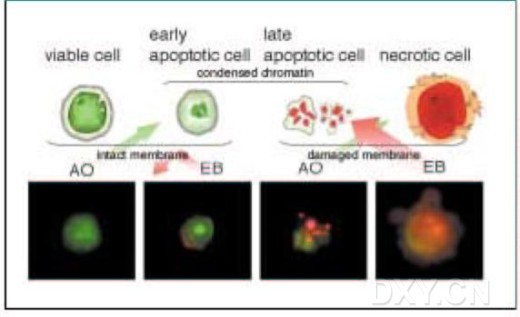
吖啶橙(acridine orange,AO)能同时与 DNA 和 RNA 结合,对活细胞和死细胞均能染色。溴化乙锭(ethidium bromise,EB)插入双链核酸,对失去膜完整性的细胞染色。
原理
吖啶橙-溴化乙锭(AO-EB)染色法检测细胞凋亡的基本原理是吖啶橙能同时与 DNA 和 RNA 结合,对活细胞和死细胞均能染色。溴化乙锭插入双链核酸,对失去膜完整性的细胞染色。
材料与仪器
步骤
吖啶橙-溴化乙锭(AO-EB)染色法检测细胞凋亡的基本过程可分为如下几步:
A 培养细胞,诱导凋亡(在超净台进行)。
B 收集细胞 先用滴管轻轻吹打,收集已脱落的细胞至离心管。加入适量的 0.02% EDTA(3~4 ml)消化未脱壁细胞并收集至上述离心管。1000 g 离心 5 min,弃上清液(悬浮细胞直接收集)。
C PBS(37 ℃)漂洗悬浮细胞。
D 固定液(4 ℃)固定 5 min,500~1000 g 离心 5 min,弃上清液。
E 蒸馏水洗,500~1000 g 离心 5 min,弃上清液。
F 调整细胞数至(0.5~2.0)x 106 个/ml。
G 取 25 μl 悬浮细胞滴于载玻片上,加入 1 μl AO-EB(1:1)染液,轻微混合。
H 直接用盖玻片封片。
I 在装有荧光滤光片的荧光显微镜下观察。
注意事项
EB 为强诱变剂,有中度毒性。提示学生操作时应戴手套。EB 污染物及废弃液应单独存放。提示学生小心甲醛。
来源:丁香实验