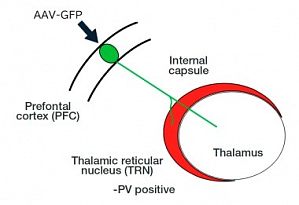
人类的前额叶皮层 (PFC) 不成比例地扩大,负责高级认知和执行机能。它的运转失灵可能导致精神疾病,如精神分裂症和阿尔茨海默病。人们对小鼠 PFC 进行了积极研究,但它缺乏与颗粒状额叶皮层相对应的区域,这表明它与灵长类动物存在巨大的结构性差异。因此,我们的研究小组正在使用狨猴这种原产于南美洲的小型猴子作为灵长动物模型。 在这项实验中,我们研究了 PFC 与丘脑网状核 (TRN) 之间的相互作用,后者是丘脑周围的一组抑制性神经元。TRN 就像一扇门,控制着从大脑皮层向丘脑的信息传输。我们研究了 TRN 中轴突纤维的详细形态,它们将信号从 PFC 传递到丘脑。 图 1. 显示神经轴突如何从前额皮质通过丘脑网状核进入丘脑的示意图。丘脑网状核起着通往丘脑大门的作用。 1.采用简单工作流程的宏观到微观成像起源于 PFC 的轴突纤维以厚束形式穿过一个叫作内囊的通道。这个轴突束穿过 TRN 的前部进入丘脑,在那里通过分裂和重新定向呈现出复杂的形态。为了准确识别 TRN,我们使用了 PV(小白蛋白)作为标记物(图 1)。 FLUOVIEW FV3000 共聚焦激光扫描显微镜的宏观到微观功能可无缝连接
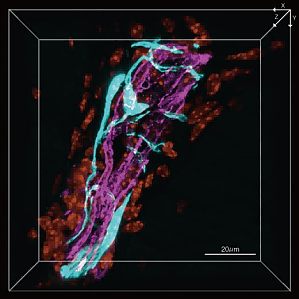
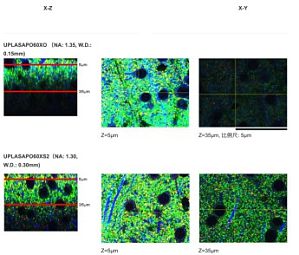
1.在降低漂白的同时对精细和复杂组织结构进行成像由于神经和血管在狭窄区域内形成了复杂结构,所以很难对膝关节骨骺中的血管和感觉神经进行成像。FLUOVIEW FV3000 共聚焦显微镜利用其高检测灵敏在低激光下对精细结构进行明亮的高分辨率成像,从而有助于降低对样品的光漂白。利用 FV3000 显微镜这一特点,我们成功对穿透胫骨骨骺椎孔的复杂 3D 结构的感觉神经及其周围血管进行成像。 图 1. 感觉神经和周围脉管系统穿透胫骨骨骺椎孔(3D 图像)。感觉神经(EYFP,青色);血管(Alexa Fluor 594,洋红色);细胞核(DAPI,橙色)。 成像设备:显微镜:FLUOVIEW FV3000 共聚焦显微镜系统(奥伟登(Evident)现已推出全新 FV4000 共聚焦显微镜)物镜:100 倍油浸物镜(UPLSAPO100XO) 2.观察胫骨骨骺的神经血管结构了解膝关节的血管和神经投射对于缓解膝关节病疼痛非常重要。然而,研究人员至今仍然无法全面观察感觉神经和血管贯穿整个膝关节的精细结构。利用 FV3000 共聚焦显微镜,我们首次清晰地观察到这些结构。我们发现,膝关节感觉神经不仅存在
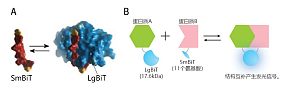
NanoBiT 是一种结构互补报告分子系统,可用于 PPI 的细胞内检测。它已成功应用于药物筛选、信号传导分析和病毒感染机制分析等一系列研究领域。该系统由一个大型 BiT(LgBiT;17.6 kDa)和一个小型 BiT(SmBiT;11 个氨基酸)亚基组成,它们将与目标蛋白质融合。这些亚基随后在细胞中表达,因此只有靶向 PPI 才能使这些亚基形成功能酶,从而产生明亮的发光信号(图 1)。 图 1. NanoBiT 蛋白质相互作用系统概览(图像 Promega 提供) 1.NanoBiT 的细胞内定位成像为进行细胞溶质和核酸表达,我们将两种载体对转染到 HeLa 细胞中。第一对为非靶向 FKBP-SmBiT 控制载体和 FRB-LgBiT 控制载体。第二对为细胞核靶向 NLS-FKBP-SmBiT 控制载体和 FRB-LgBiT 控制载体(图 2)。已知 FKBP 和 FRB 会在西罗莫司治疗下结合。 图 2. FKBP/FRB NanoBiT 和 NLS-FKBP/RRB NanoBiT 的细胞内定位 然后使用 IXplore Live for Luminescence 显微镜系统
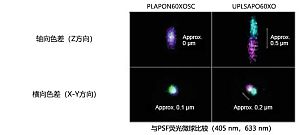
1.低色差物镜 PLAPON60XOSC 在脑组织四重免疫荧光中的应用在利用光学显微镜(如共聚焦显微镜)获取荧光图像之前使用荧光染料标记分子的方法,已成为可视化生物组织和细胞分子定位的最常用实验方法。然而,由于显微物镜的色差所致的色差导致难以使用荧光染料精准显示紫外光和近红外区域中的细胞间共定位,因此在单个标本中很难实现多个细胞间共定位的准确可视化。奥伟登(Evident)低色差物镜 PLAPON60XOSC 即使在紫外和近红外区域也能以几乎没有色差的方式准确显示荧光标记分子。下面介绍使用四种类型荧光抗体在单个标本中准确可视化荧光标记分子的共定位情况。 PLAPON60XOSC 和 UPLSAPO60XO 的性能比较 2.低色差物镜的应用-脑组织的四重免疫荧光 图 1. 脑组织的四重免疫荧光。VIAAT 染色(Alexa Fluor405,蓝色);CB1 染色(Alexa Fluor488,绿色);VGluT3 染色(Cy3,红色);DGLα染色(Alexa Fluor647,白色)。 大麻素合成酶 DGLα(白色)和大麻素受体 CB1(绿色)聚集在小鼠基底杏仁核的锥体细胞躯体(星号
1.使用让标本透明的透明化技术进行深层组织观察使用激光共聚焦显微镜对透明化标本进行深层组织观察时,物镜选择非常重要。观察这些样品时,奥伟登(Evident)硅油浸没式物镜系列具有出色的性能。以下,我们讨论了使用 FLUOVIEW 系列共聚焦激光扫描显微镜和硅油浸没物镜对透明化标本的深层组织进行高分辨率观察的两个示例。 2.使用 SCALEVIEW-A2 进行透明化小鼠大脑切片的深层组织观察SCALEVIEW-A2 是奥伟登(Evident)用于让生物标本透明的产品。可消除光散射,且不会降低福尔马林固定生物标本的光吸收或荧光。将哺乳动物的脑标本浸没在 SCALEVIEW-A2 溶液中会让其变得透明。无需脑标本切片即可观察到从表面到组织深处标记荧光蛋白的结构。 我们使用 FLUOVIEW 系列共聚焦激光扫描显微镜,对使用 SCALEVIEW-A2 渲染透明的小鼠大脑切片进行了成像。使用 60X 油浸物镜拍摄的图像与 60X 硅油浸物镜 UPLSAPO60XS2 拍摄的图像进行比较。 使用 60X 油浸物镜和 60X 硅油浸没物镜,拍摄并渲染透明的小鼠大脑的新皮层切片,进行深层组织图像比较。
1.相衬方法的变化图 1 通过相应的光学元件排列简要说明了无需染色即可观察透明物体的常见相位可视化方法。传统的相位可视化方法通过在聚光镜光瞳和物镜光瞳中分别放置特定光学元件来实现。 图 1. 各种相位可视化方法的光路布置。各种相位可视化方法的必要光学元件。a. 相衬方法;b. 微分干涉方法;c. 调制对比方法;d. 渐变对比方法。 相衬方法(图 1a)组合使用带环状孔径的专用聚光器透镜和含有相位膜环的专用物镜透镜。在通过聚光镜环状孔径的光线中,那些直接通过样品的光线会通过物镜光瞳的相位膜。另一方面,被样品偏转的光线在相位膜外通过,从而在两个分量相互干扰的点产生明暗对比。这一过程的典型特征是,在样品的折射率分布发生变化的台阶处会出现光晕现象。厚样品不适合采用这种方法,因为会出现过强的光晕。微分干涉方法(图 1b)是一种偏振剪切干涉仪,在聚光镜光瞳和物镜光瞳位置装有互补的沃拉斯顿棱镜。样品图像变为在固定方向上略微偏移的重像,并且样品的折射率梯度带有阴影,使其看起来具有三维立体感。由于采用了偏光干涉,如果有塑料皮氏培养皿或其它物体在光路中造成偏振失真,则无法进行观察。调制对比方法(图 1c
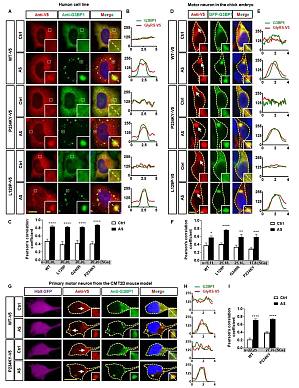
2023 年 2 月 3 日,浙江大学医学院脑科学与脑医学学院白戈课题组与合作者在 Cell 杂志 ( IF = 66.850 (2022) / JCR 分区: Q1 ) 以封面文章形式在线发表研究论文。该工作发现虽然在正常生理状态下不同 CMT 致病蛋白在细胞中的定位各异,但在应激状态下这些 CMT 致病蛋白会表现出相同的细胞定位,进入应激颗粒中并与其核心蛋白 G3BP 发生异常互作,引起应激颗粒异常,使得周围神经应对环境不良刺激的能力下降,从而导致周围神经病的发生。 该研究首先使用浙江大学医学院公用技术平台奥伟登(Evident)FV3000 激光共聚焦显微镜(奥伟登(Evident)现已推出全新 FV4000 共聚焦显微镜),在 HeLa 细胞、鸡胚运动神经元和小鼠原代培养运动神经元中确定了导致 CMT2D 亚型的 GlyRS 蛋白能够在应激状态下进入到应激颗粒中(图 1),同时利用该显微镜的时间序列和 FRAP 成像模块获得数据揭示了 GlyRS 致病蛋白对神经元生长长度的影响及 GlyRS 致病蛋白对应急颗粒动态性的影响。 图 1. GlyRS 蛋白在应激下定位到 SG
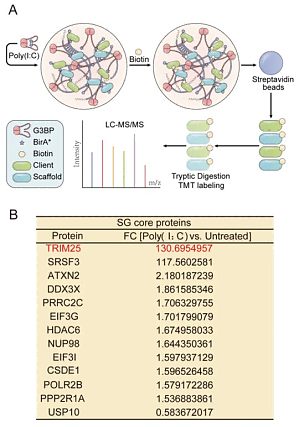
2024 年 5 月 15 日,四川大学生物治疗全国重点实验室贾大课题组与合作者在 Nature communications 杂志 ( IF = 16.6 (2023) / JCR 分区: Q1 ) 在线发表了题为「TRIM25 predominately associates with anti-viral stress granules」的研究论文。该工作利用 G3BP1 邻近蛋白生物素化标记实验发现 TRIM25 是抗病毒 SG 的有效标记物。课题组成员发现 TRIM25 会独立发生 LLPS 现象,而 dsRNA 的存在会显著增强这种反应。Poly(I:C) 处理和 RNA 病毒感染都会引发 TRIM25 和 G3BP1 的共相分离,从而显著提高 TRIM25 对底物的泛素化活性,其中许多底物都定位于 SGs 中。TRIM25 和 G3BP1 的共相分离对激活 RIG-I 信号通路和限制 RNA 病毒感染至关重要。该研究不仅为抗病毒信号通路的调控提供了新的见解,而且为研究应激特异性 SG 亚型的组成、动态和功能建立了一个研究范式。 该研究首先采用了一种邻近生物素化标记(Bio
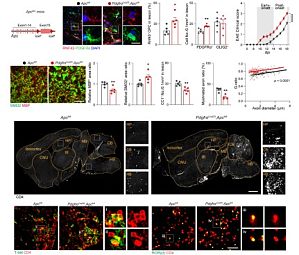
2025 年 4 月 2 日,由陆军军医大学牛建钦教授、万瑛教授与中山大学附属第七医院易陈菊研究员联合带领的研究团队在 Science translational medicine 上发表研究论文,首次揭示了少突胶质前体细胞(Oligodendrocyte precursor cell, OPC)在多发性硬化(Multiple Sclerosis, MS)早期病理过程中触发免疫反应级联激活,并导致快速脱髓鞘的新机制。 MS 是一种以中枢神经系统脱髓鞘为核心病理特征的自身免疫性疾病,全球患者超 280 万。其典型表现为免疫细胞异常浸润引发的神经髓鞘损伤、轴突退化甚至不可逆的神经功能障碍 (1)。尽管现有疗法可延缓疾病进展,但早期病理机制不明、缺乏特异性干预靶点仍是临床面临的重大挑战。陆军军医大学牛建钦教授团队前期研究发现,MS 患者脑内 OPC 存在 Wnt 信号通路异常激活现象,且其病理复杂性远超小鼠模型,但此类病理性 OPC 如何驱动疾病进展尚不清楚 (2, 3)。近日,研究团队在 Science translational medicine 发表论文揭示:MS 病理条件下,OPC
冻存和复苏
细胞治疗技术正扮演着越来越重要的角色。其中,CAR-T 细胞治疗、间充质干细胞(MSC)治疗以及 T 细胞治疗是三种备受关注的细胞治疗方法。这些治疗方法通过采集患者体内的特定细胞,经过体外激活、修饰、扩增等步骤,再将这些具有特定功能的细胞移植回患者体内,以达到治疗疾病的目的。为了更好地理解和应用这些治疗技术,下面我们将整合并详细叙述这三种细胞治疗的流程图内容,为研究人员和临床医生提供一个清晰的操作指南。CAR-T 细胞治疗流程间充质干细胞治疗流程 T 细胞治疗流程
CAR-T 细胞疗法自 2017 年首次获得 FDA 批准以来一直蓬勃发展,在血液恶性肿瘤治疗上表现优异,为 B 细胞急性淋巴细胞白血病等疾病的患者提供了完全治愈的可能性。但大部分实体瘤由于肿瘤微环境的影响,会阻碍 T 细胞浸润、活化和增殖,导致对 CAR-T 疗法反应有限。其主要的抑制机制包括 T 细胞受体信号传导的抑制以及炎性细胞因子的消耗,目前克服抑制性肿瘤微环境仍然是实体瘤免疫治疗的主要障碍。 2022 年 12 月 16 日,Science 发文表示,研究人员通过在 T 细胞上构建肿瘤特异合成性 Notch 受体(synNotch),可以在识别癌细胞后诱导产生 IL-2 促进 T 细胞活性,在胰腺肿瘤和黑色素瘤模型中可以有效增强 CAR-T 细胞或 TCR-T 细胞的肿瘤浸润,实验鼠体内的肿瘤清除能力以及其存活率均有显著提升,此类改良给 CAR / TCR-T 细胞在免疫抑制性实体瘤治疗领域带来新突破。 图:论文截图 目前 CAR-T 细胞治疗血液恶性肿瘤也仍面对四个主要挑战:肿瘤异质性以及目的抗原丢失免疫抑制性的肿瘤微环境CAR-T 细胞耗竭输注后的不良反应 面对这些挑战,
(1)促进免疫细胞的增殖和分化:生长因子能够通过调节细胞信号通路,促进免疫细胞的增殖和分化。白细胞介素-2(IL-2):IL-2 是一种重要的免疫调节因子,能够促进 T 细胞和自然杀伤细胞(NK 细胞)的增殖和活化,增强其细胞毒性。粒细胞-巨噬细胞集落刺激因子(GM-CSF):GM-CSF 能够促进骨髓中粒细胞和巨噬细胞的发育和成熟,增强其吞噬和杀伤能力。(2)调节免疫细胞的表型和功能:生长因子可以通过调节免疫细胞的表型,影响其功能和免疫反应。转化生长因子-β(TGF-β):TGF-β 是一种多功能细胞因子,能够抑制多种免疫细胞的增殖和分化,如 T 细胞、B 细胞和 NK 细胞。它在免疫抑制和免疫调节中发挥重要作用。干扰素(IFN):干扰素具有抗病毒、抗肿瘤和免疫调节功能,能够激活免疫细胞,增强其抗病原体能力。(3)改善免疫微环境:生长因子可以通过调节免疫微环境,影响免疫细胞的浸润和功能。肿瘤坏死因子-α(TNF-α):TNF-α 能够激活免疫系统,促进炎症反应,调节免疫细胞的浸润。TGF-β:在肿瘤微环境中,TGF-β 通过调节肿瘤相关巨噬细胞(TAMs)和免疫抑制细胞的浸润,影响抗
细胞治疗是细胞和基因治疗的重要组成部分,它通过使用特定类型的细胞来修复、替换或调节受损的组织和器官。在细胞治疗中,不同类型的细胞因其独特的生物学特性而被广泛应用于多种疾病的治疗。以下是一些常用的细胞类型及其在细胞治疗中的应用。 (1)免疫细胞免疫细胞是细胞治疗中最重要且研究最多的细胞类型之一,主要包括 T 细胞、自然杀伤细胞(NK 细胞)和树突状细胞(DC 细胞)。T 细胞:T 细胞是人体免疫系统的核心细胞,具有强大的抗肿瘤能力。CAR-T 细胞疗法是目前最成功的免疫细胞治疗技术之一。它通过从患者体内提取 T 细胞,利用基因工程技术在 T 细胞表面嵌入嵌合抗原受体(CAR),使其能够特异性识别并攻击癌细胞。CAR-T 细胞疗法已在急性淋巴细胞白血病(ALL)、非霍奇金淋巴瘤(NHL)等血液肿瘤中取得了显著疗效。自然杀伤细胞(NK 细胞):NK 细胞是先天免疫系统的一部分,具有天然的抗肿瘤和抗病毒感染能力。与 T 细胞不同,NK 细胞不需要预先激活即可直接识别并杀死肿瘤细胞。近年来,NK 细胞疗法在实体瘤治疗中展现出巨大潜力,尤其是在卵巢癌、乳腺癌和前列腺癌等疾病中。树突状细胞(DC 细
细胞和基因治疗(Cell and Gene Therapy,简称 CGT)是近年来生物医学领域最具革命性的前沿技术之一,它通过直接干预细胞和基因层面的病变,从源头上治疗疾病。与传统的小分子药物和大分子生物药不同,CGT 专注于遗传性或获得性疾病的根源,旨在通过修复、替换或调控异常基因或细胞,实现疾病的治疗、预防甚至治愈。 (1)定义与分类细胞和基因治疗是一种将遗传物质或细胞转移到患者体内以达到治疗效果的创新疗法。它主要分为两大类:细胞治疗和基因治疗。细胞治疗通常涉及从患者体内提取细胞,经过体外处理后再回输到患者体内,以发挥治疗作用。基因治疗则是通过基因编辑、基因添加或基因沉默等技术,直接修复或调控患者体内的异常基因。 (2)基本原理细胞和基因治疗的核心在于通过基因操作或细胞改造来纠正疾病的分子基础。例如,基因治疗可以通过以下几种方式实现:基因替代:用健康的基因替代缺陷基因,使细胞能够正常表达功能蛋白。基因修复:利用基因编辑技术(如 CRISPR-Cas9)直接修复突变基因。基因沉默:通过 RNA 干扰(RNAi)或反义寡核苷酸(ASO)技术抑制有害基因的表达。细胞治疗则主要利用免疫细胞
通过这个系列的视频,你将了解到:不同型号的层析柱的装填方法及操作要点,层析柱各部件的构造和功能等
HIS 标签蛋白纯化效果不理想,宝宝心里苦呀。今天,小编来跟大家一起找找原因。纯化所得组分中没有收集到重组的 HIS 标签蛋白。该问题主要可以分为以下两个方面:1、HIS 标签蛋白没有结合到填料上就流穿了原因一超声的功率不对。超声功率过高,容易导致蛋白炭化;功率过低,蛋白释放不出来。建议改变超声功率,同时可以在超声前加入溶菌酶。原因二结合缓冲液条件不合适。建议检查结合缓冲液中是否有影响结合的因素,如:金属离子螫合剂、强还原剂、过高的咪唑浓度。同时,优化缓冲液的 pH、盐离子浓度、添加剂(如 5% 甘油、1mM DTT) 等。原因三HIS 标签没有表达或丢失或暴露不充分。建议 1用 anti-HIS 的抗体进行 WB,检测 HIS 标签是否存在。建议 2将蛋白用 4-6M 盐酸胍或 4-8M 尿素变性后,让 HIS 标签充分暴露出来,看是否能与填料结合。建议 3改变 HIS 标签的位置或者增加其数目(常用 6-12 个 HIS),增加暴露和结合机会。建议 4改变金属结合离子,除了 Ni2+,Cu2+、Zn2+、Co2+ 也可以用来进行 HIS 标签的捕获。2、HIS标签蛋白结合了,但是洗
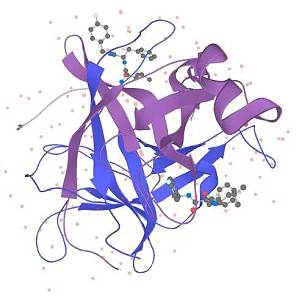
天然蛋白的特性可以说是迥然有异,每种蛋白都是不一样的烟火,共同特点就是丰度很低,自带丰富的背景杂质,并且没有特异性的纯化方法可循。然万物皆有共性,我们只需找到他们的共同点就可以求同存异,一切难题也就可以迎刃而解。凡是蛋白质都是氨基酸组成的,氨基酸既是两性电离物质又有多种多样的R 取代基,那么丰富的氨基酸组成就让不同蛋白质或多或少拥有带电性与疏水性。图1. 蛋白质结构示意图以上给我们的纯化提供了基础方案:以离子交换层析和疏水层析为核心步骤来开展。由于天然蛋白的复杂性,通常一步简单纯化很难达到我们的需求。事业已经成功了一半,另一半主要考验策略。成功有效纯化蛋白质的关键除了选择适宜的纯化技术,还要通过优化实验参数来达到要求的纯度,并且将各个纯化步骤以最合理的方式衔接起来,使用最少的纯化步骤,最少的劳动力,最经济的方案,达到蛋白质产量的最大化。图2. 蛋白质纯化技术流程图晋级之门已经开启,你的老板对你提出了三次公演的挑战!本攻略来教你如何乘风破浪。1、根据样品的初始条件选择离子交换或者疏水层析。如果样品初始处于低盐的缓冲液(中脱盐或缓冲液置换),就可以预判纯化使用的 pH 值,并选择离子交换层
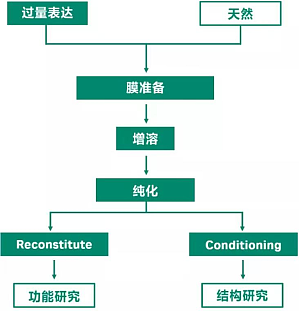
采用亲和加分子筛两种层析方法就能得到大量高纯度的蛋白样品往往是别人家的实验。到自己手上总会有各种惊喜…今天的主角更加过分,在真正纯化之前就需要我们施展十八般武艺把它从细胞上「拽」下来。没错,它就是膜蛋白…人类基因组中,有大约 30% 的基因编码膜蛋白。当今已批准上市的药物中,有超过 50% 以膜蛋白为靶点,然而目前蛋白质结构数据库 (Protein Data Bank, PDB) 中膜蛋白比例不足 1%。欲了解其功能,必解析其结构。是很多结构生物学家心头的念念不忘,随着冷冻电镜技术的发展,会有更多的膜蛋白结构得到解析,助力后续的功能研究和药物发现。有了冷冻电镜这把利器之后,真正制约膜蛋白研究的其实是样品的制备。常规的膜蛋白制备流程如下:图 1.常规的膜蛋白制备流程图特点是:蛋白含量低收率低活性易降低纯化过程需要优化去垢剂天然表达的膜蛋白含量极低,很难纯化。就算是重组表达体系,生产出的膜蛋白通常具有细胞毒性,因此表达量也远低于常规重组蛋白。在整个纯化过程中都需要选择合适的去垢剂才能使膜蛋白本身保持空间构象和活性。去垢剂可分为三种:表 1.去垢剂类型和特点表常用的去垢剂大概有十几种,根据膜
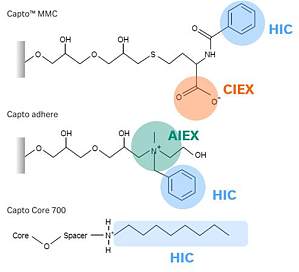
复合模式层析原理复合模式层析是一种集合多种类型的相互作用(如离子交换、疏水、氢键、嗜硫亲和等)于一种层析介质从而同时具备高选择性和高分辨率的层析技术。图15 复合模式层析配基类型特点相较于传统层析模式具备更快的传质速率和更高的分辨率。在高回收率条件下实现有效分离。能够同时去除多种杂质,如多聚体、宿主蛋白、病毒、电荷异构体等。适用于难以同时去除多种痕量杂质的层析需求。层析介质目前Cytiva共有四款复合模式层析介质:Capto™ Adhere系列可有效应用于两步法抗体纯化的精纯步骤。Capto™ MMC系列可直接用于发酵液的高盐上样,有效简化步骤,降低成本。Capto™ Core系列广泛应用于病毒、病毒样颗粒、病毒载体、外泌体等大粒径蛋白分离中。不同层析介质之间的比较1. Capto™ Core400 & Capto™ Core700Capto™ Core是一种具有独特双层结构的多模式填料。其外层是5µm的钝化层,屏蔽了所有的结合位点并精准控制孔径。分子量大于700kDa或400kDa的生物大分子不能进入填料内部。其内层是多模式配基辛胺基,可吸附进入内部的蛋白质、核酸等物质。图1