简介
为了保证长期使用医用材料的患者,以及长期接触这些材料的生产者的安全性,对材料进行全身毒性试验的研究是非常必要的。虽然材料对人的作用不完全能在动物身上表现出来,但动物试验数据对一个新材料来说仍是一个很有用的参考数据。因此,为保证患者的安全,新材料在临床应用前一定要进行毒性试验。
毒性试验的类型,可根据材料的性质及使用途径、方法和时间等加以选择。如有的材料接触后则很快产生中毒症状,有的材料需长期接触才能产生毒性症状。因此,材料的毒性试验,应由该材料的特点来决定。根据材料与人体的接触情况,可将材料与人体接触的重复接触全身毒性试验分为亚急性、亚慢性和慢性全身毒性试验。亚急性全身毒性(subacute systemic toxicity)是指在 24 小时~28 天内多次或持续接触试验样品后发生的不良作用。
由于该术语在语义上不确切,在该限定时间周期内发生的不良作用也可称为短期重复性接触全身毒性研究。国际规范性导则大多选择 14~28 天的周期,并考虑合理的方法。亚急性静脉研究一般规定接触时间大于 24 小时,但小于 14 天。亚慢性全身毒性(subchronic systemic toxicity)是指反复或持续接触试验样品后在动物寿命期的某一阶段发生的不良作用。
啮齿动物亚慢性毒性研究一般为 90 天,其他种属动物在不超过其寿命期的 10% 的阶段内。亚慢性静脉研究一般规定接触时间为 14~28 天。慢性全身毒性(chronic systemic toxicity)是指观察动物反复给予受试材料或材料浸提液后,对机体产生的毒性反应及其严重程度,主要的毒性靶器官及其损害的可逆性,为材料毒性安全性判断提供参考。对于啮齿类动物的慢性毒性研究试验周期一般为 6~12 个月。
材料与仪器
步骤
重复接触全身毒性试验的基本过程可分为如下几步:
A 体重称量,试验接触前以及试验终结时宜即刻测量体重,第一次接触后根据试验周期长短,在需要时每周测量一次。短期重复剂量全身毒性试验的临床观察阶段应与试验周期相适应,每天应至少一次采用实验室通用临床反应术语记录观察到的动物存活情况和明显的临床反应(表 10-5-14)。长期重复接触试验每天应至少两次观察记录动物的发病率和死亡率,可考虑至少每周一次观察记录更大范围内的临床不良反应。无论何种情况,观察次数和采取的适宜方式应能最大限度降低实验动物的损耗,如对死亡动物进行尸检或冷藏,隔离或处死病弱或垂死动物。

B 临床病理学检查包括血液学指标、生化指标、组织病理学检查等,必要时考虑尿液检测指标。在试验开始前、试验中期及试验终结时测定血液学指标,如凝血(PT、APTT),红细胞容积,血小板计数,红细胞计数,血红蛋白浓度,白细胞计数,白细胞分类等血液学检查项目。
C 在试验终结时测定临床化学指标,如白蛋白,ALP,ALT,AST,钙,氯化物,胆固醇,肌氨酸酐,GGT,葡萄糖,无机磷,钾,钠,总胆红素,总蛋白,甘油三酸酯、尿氮等临床生化、血液方面的项目。根据试验周期考虑增加检验次数。适合所有重复接触试验的测定项目包括电解质平衡、碳水化合物代谢,以及肝和肾功能。具体检验项目的选择还要根据样品材料作用模式方面的观察。
D 尿液检验不作为常规检验项目,仅在预期或观察到这方面的毒性反应的情况下才考虑进行。一般情况下仅考虑血液学和临床化学指标检测。
正常值的历史数据有利于建立基线水平,并可用于与当前试验对照进行比较。如历史基线数据不充分时,可考虑从同一年龄、性别、品系和来源的动物中采集该类信息,最好在同一实验室内进行。下面列出常用的实验动物大、小鼠、实验兔和试验犬的正常生理生化值(表 10-5-15 至表 10-5-18),以供试验时参考。

E 组织病理学检查包括:
① 对对照组和高剂量组动物的器官和组织进行完整的组织病理学检查。
②检查所有大体损害。
③如设有低、中剂量组,宜对动物肺脏进行组织病理学检查是否有感染迹象,因为这种检查便于判定动物的健康状态。还宜考虑对低、中剂量组进行肝和肾的组织病理学检查,其他组织病理学检查可不必常规进行,但高剂量组如显示损害迹象则必须进行器官的组织病理学检查。
④如设有附加组,可根据剂量组动物出现的反应来确定需进行的组织和器官病理学检查。
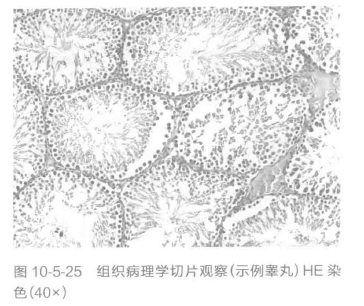
⑤慢性试验一般设有预警动物来监控感染性因子的产生,必要时可对预警动物进行血清学和组织学检查。如怀疑试验样品导致特异性器官毒性时,进行其他科学适宜性的试验(通常要求冷冻样品采集。进行组织病理学评价的器官包括肾上腺*、全部大体损害(包括试验位置)、附睾*、食管、心脏*、小肠、肾*、肝*、肺、淋巴结(接触局部位置和远端全身作用的淋巴结)、肌肉(骨骼)、鼻甲骨(用于吸入试验)、神经(坐骨神经或胫骨神经,最好贴近肌肉)、卵巢*、胰腺、甲状旁腺、精囊、脾*、胃、胸腺*、子宫*(包括子宫颈和输卵管)、阴道、睾丸*等。参见示例图 10-5-24,图 10-5-25。标*号的器官、组织在进行组织病理学评价时宜称重。临床和其他发现可显示检查其他组织的必要性,应根据已知的试验物质特性保存可能的靶器官。
对照组和最高剂量组全部动物的保存器官和组织宜进行完整的组织病理学检查。如最高剂量组观察到相关接触改变,此类检查和必要的靶器官/组织、特异性器官/组织检查须扩展至其他全部剂量组。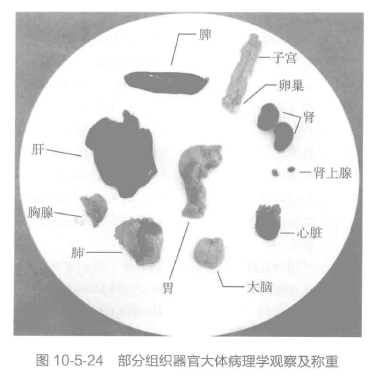


F 全部动物宜进行完整的大体尸检,包括检查体表、体表孔口、头部、胸(腹)腔及内脏等。肾上腺、附睾、心脏、肾、肝、卵巢、脾、睾丸、胸腺和子宫在取出后宜尽快称量其湿重,以防止干燥以及由此造成的重量减轻。将上述已列出的组织病理学应检查器官和组织置于适宜的固定液中保存,以进行下一步组织病理学检查。
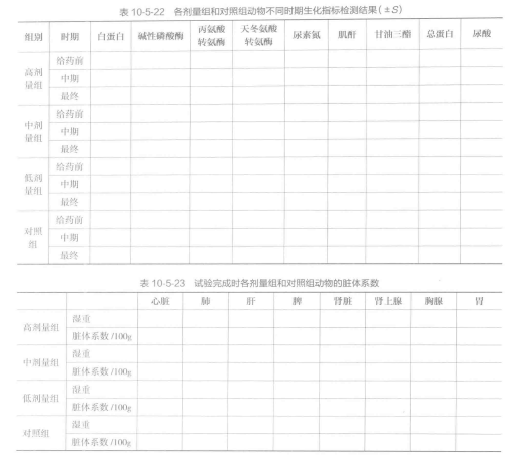
G 以表格形式摘要给出数据,包括试验开始时每一试验组动物数量、出现损害迹象的动物数量、损害的类型以及出现每种损害类型动物的百分率(表 10-5-19 至表 10-5-23)。应进行统计学评价,但首先要考虑生物学相关性。可采用任何可接受的常用统计学方法,在设计试验时选择统计学方法。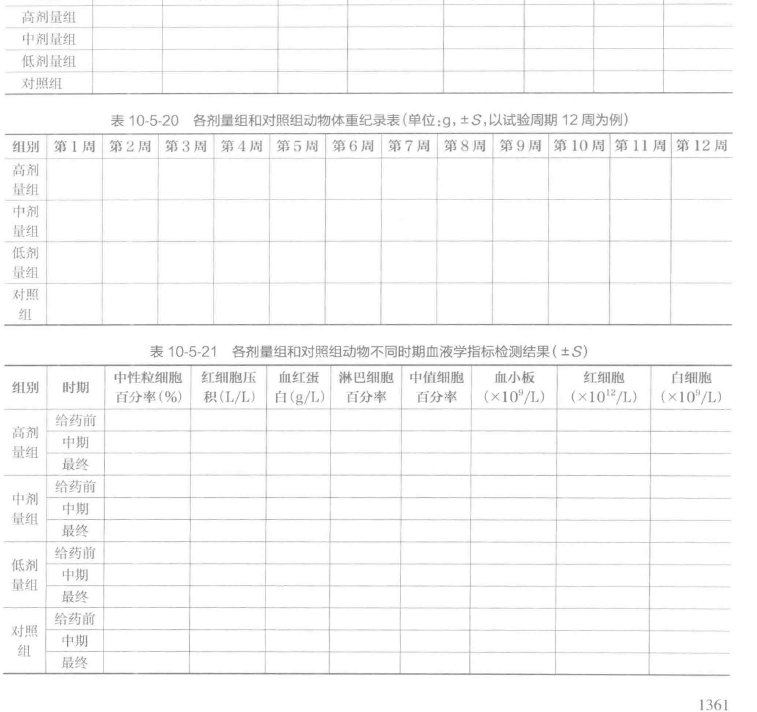


来源:丁香实验