施一公团队 2023 首秀!发现 APOE4 受体,揭示阿尔兹海默症潜在致病因子
丁香学术
导读
APOE 的基因产物 APOE 在脂质代谢、免疫调节和神经学中起着关键作用。最常见的三种 APOE 等位基因对应于三种蛋白质异构体,分别是 APOE2、APOE3 和 APOE4,它们仅在 112 和 158 两个氨基酸位置上存在差异。尽管只存在微小差别,但前期的研究数据表明,这些 APOE 亚型在生理和病理学层面却表现出不同的作用。
其中,APOE 的免疫调节作用最初是作为血浆脂蛋白对 T 细胞增殖抑制作用的一部分被发现的。研究表明,APOE 能够抑制 T 细胞增殖和中性粒细胞激活,并且可以调节巨噬细胞功能、促进脂质抗原呈递和调节炎症和氧化。
此外,APOE 亚型在神经学和神经退行性疾病如阿尔茨海默病(AD)中也有明显的作用。例如,与最常见的 APOE3 亚型相比,APOE4 亚型发病年龄相对较早,显著增加 AD 风险。相比之下,APOE2 则具有保护作用。目前,越来越多的证据表明,免疫系统功能障碍在 AD 病理中起着关键作用,特别是小胶质细胞的异常激活,而 APOE4 的过表达同样可以激活小胶质细胞。但是,APOE4 发挥作用的潜在机制却仍不明确。
2023 年 1 月 2 日,西湖大学施一公团队在 Cell Research 在线发表题为 LilrB3 is a putative cell surface receptor of APOE4 的文章,该研究发现,白细胞免疫球蛋白样受体 B3(LilrB3)是 APOE4 的潜在细胞表面受体,两者可特异性结合,并阐明了这种特异性配体-受体识别的结构基础。同时,他们的研究发现,LilrB3 与 APOE4 结合还会触发小胶质细胞的激活。这些实验结果为 APOE 亚型依赖的功能和疾病研究提供了线索。
图片来源:Cell Research
主要研究内容
APOE4 与 LilrB3 特异性相互作用
首先,研究人员通过一系列实验证实 APOE4 可与 LilrB3-胞外结构域(ECD)表现出强烈的相互作用,但与任何同家族内其他 LilrB-ECD 则没有相互作用。虽然 APOE3 也与 LilrB3-ECD 相互作用,但结合较弱。
为了进一步描述这种相互作用,他们将不断增加的 LilrB3-ECD 浓度滴定到固定量的 APOE2/3/4 中。与 APOE3 相比,LilrB3-ECD 与 APOE4 的结合更紧密,与 APOE2 的结合则检测不到。此外,他们还量化了 APOE2/3/4 与 LilrB3-ECD 之间的相互作用。与上述结果一致,APOE4 与 APOE3 相比,与 LilrB3-ECD 结合更紧密;而 APOE2 则无法与 LilrB3-ECD 结合。
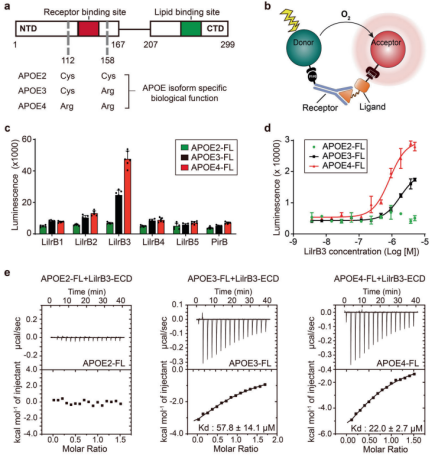
图片来源:Cell Research
APOE4 在细胞表面被 LilrB3 特异性识别
接下来,他们研究了 APOE4 是否能在细胞表面被 LilrB3 特异性识别。研究人员在 HEK293F 细胞中表达 RFP 标记的 APOE4 后,收集含有 APOE 的上清液,分别与 6 种不同的 HEK293F 培养物孵育,每种培养物都表达特定的 GFP 标记的 LilrB 受体。实验结果表明 APOE4 与细胞表面的 LilrB3 之间存在浓度依赖的相互作用,并且 APOE4 特异性地与细胞表面的 LilrB3 结合,而不与任何其他 LilrB 受体结合。
为了确认上述结果,他们还使用共聚焦显微镜进行了观察。正如预期的那样,APOE4 仅在表达 LilrB3 的细胞表面大量存在,并且 APOE4 的细胞表面定位与 LilrB3 的定位一致。
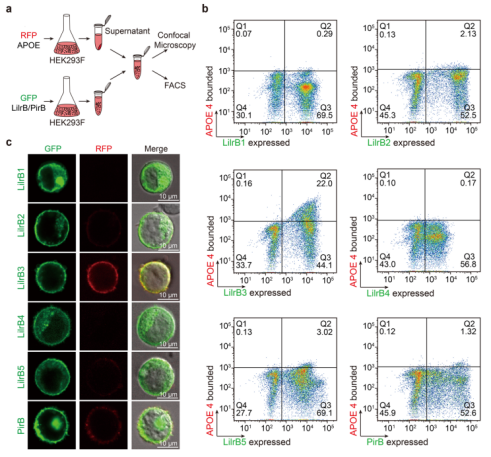
图片来源:Cell Research
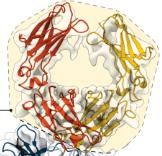
LilrB3 识别 APOE4 的结构基础
为了了解 LilrB3 识别 APOE4 的结构基础,研究人员纯化了 APOE4-N 端结构域 (NTD) 和 LilrB3-ECD 之间的二元复合物,并对样品进行冷冻电镜 (cryo-EM) 分析。在结构分析中发现,两个 APOE4-NTD 分子与两个 LilrB3-ECD 分子结合。每个 APOE4-NTD 与 LilrB3-ECD 的两个副本结合,与一个 LilrB3 分子的 D2 和另一个分子的 D4 结合。值得注意的是,两个 APOE4-NTD 分子之间没有直接接触。他们推测,这种结合模式可能有利于细胞内信号传递。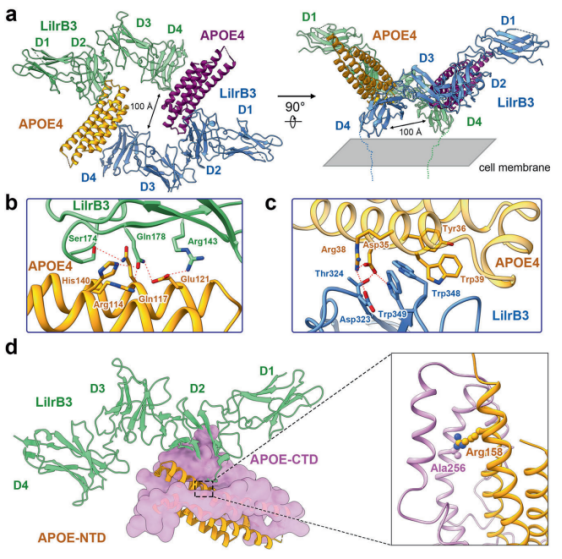
图片来源:Cell Research
APOE4 以 LilrB3 依赖的方式激活小胶质细胞
在上述体外结合实验中,LilrB3-ECD 特异性识别 APOE4,但不识别 APOE2,并且 APOE4 优先与细胞表面的 LilrB3 受体结合,而不是其他 LilrB 受体。为了检测这种相互作用的潜在后果,研究人员在人类小胶质细胞 3 (HMC3) 细胞系中敲除了 LilrB3 基因并评估了 APOE 亚型处理对 WT 和 LilrB3-null HMC3 细胞的影响。
随后,他们从这些细胞中提取总 RNA 并进行转录组测序分析。经过生物信息学分析,他们在 APOE4 处理的 WT HMC3 细胞中鉴定出 167 个差异表达基因,其中 95 个基因上调,72 个基因下调;相比之下,对于 APOE3 和 APOE2 处理组,上调和下调的基因数量分别为 76/9 和 34/1。这些数字表明,与 APOE3 或 APOE2 相比,APOE4 诱导的变化更为明显。后续的主成分分析也显示 HMC3 细胞对三种 APOE 亚型的处理存在不同的反应。
进一步的分析发现,大部分 APOE4 刺激的基因参与了促炎反应,包括干扰素、细胞因子和抗病毒信号通路。特别是 30 个 I 型干扰素刺激基因 (ISGs),其中包括抑制病毒进入的 IFITM3。这些具有代表性的 APOE4 响应基因也通过实时定量 PCR 得到了验证。
最后,他们还评估了 APOE 亚型对 LilrB3 缺失 HMC3 细胞的影响。结果发现,与 WT HMC3 细胞相反,在 LilrB3- null 细胞中,响应 APOE4 处理的上调和下调基因的数量分别急剧减少到 18 个和 1 个。综上所述,这些实验数据表明,在没有 LilrB3 表达的情况下,APOE4 激活 HMC3 细胞的能力被严重破坏。
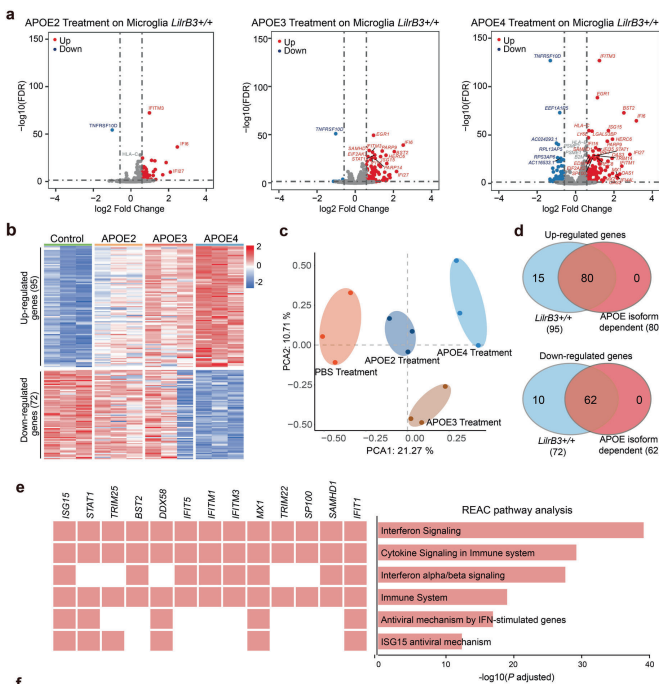
图片来源:Cell Research
结语
综上所述,在本研究中,他们鉴定出 LilrB3 可作为 APOE4 的特异性细胞表面受体,并详细解析了这种特异性配体-受体识别的结构基础。同时,他们的初步实验证据还表明,LilrB3 与 APOE4 结合可触发小胶质细胞的激活。因此,这些实验结果为将来进行更加深入的关于 APOE 亚型依赖的功能和疾病研究提供了基础,比如其在阿尔兹海默症中的作用以及发挥作用的分子机制。