【思路解读】Cell | 顶刊文章思路解读,你也可以喜提一篇…
科研论文时间
非编码 RNA 是研究的大热,常常见诸于 CNS 报端。
一直以来,非编码 RNA 被认为是转录基因组上的「暗物质」。然而,随着测序技术的提升,研究人员发现人类基因组中 97% 的基因并不编码蛋白质。
这些 DNA 不编码蛋白,却又会转录出大量的非编码 RNA,显然这不是上帝造人打盹时的「美丽错误」,非编码 RNA 应该有相应的作用,只是暂时未被发现而已。
今天,笔者分享一篇顶刊《Cell》上 lncRNA 相关的文章,题目为《Self-Recognition of an Inducible Host lncRNA by RIG-I Feedback Restricts Innate Immune Response》。
研究者发现一种全新非编码 RNA,该分子能够调控免疫系统的「进」与「退」, 拥有识别自我和非我的能力,这是此前学术界从未认识和证明的。

图片来源:Cell 期刊官网
研究人员首先锁定一个已知的模式识别受体蛋白——RIG-I(RIG-I 能够识别外源性 RNA),用来求证这个能与病毒 RNA 结合的蛋白,会不会和体内自身的 RNA 分子结合。
于是,研究人员将 RIG-I 蛋白做测序,得到了 lncRNAs 的测序图谱。
挑取前 30 个 lncRNAs 进行敲除后,测定结果发现,某条 lncRNA 含有 Lsm3 内含子和外显子的部分序列,而在 Lsm3 基因形成的 lncRNA 有两种形式,一个是 lnc-Lsm3a,一个是 lnc-Lsm3b。
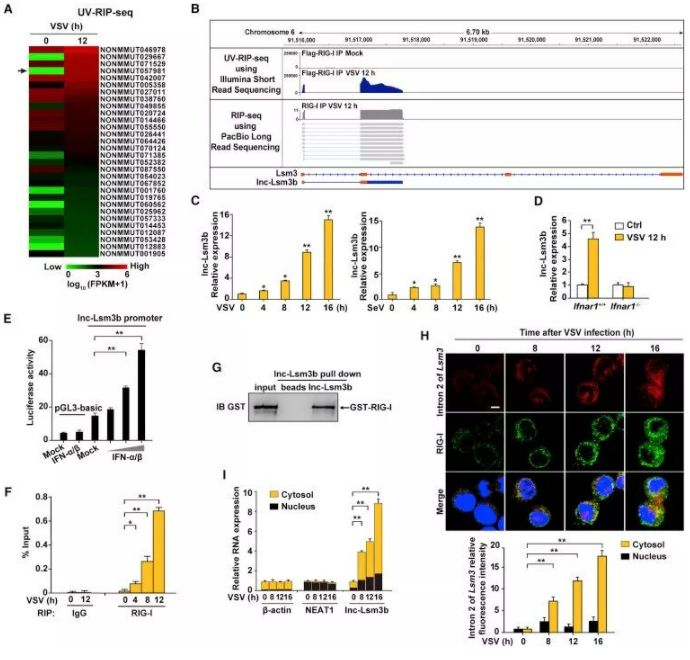
图片来源:文献截图
紧接着,对这两条 lncRNAs 进行具体验证,哪一条起关键作用。
实验发现,只在 293T 细胞中导入 lnc-Lsm3a 载体,发现 lnc-Lsm3b 比 lnc-Lsm3a 要高很多,而只导入 lnc-Lsm3a 的突变体,检测发现细胞中只有 lnc-Lsm3a。
这些实验表明 lnc-Lsm3a 是 lnc-Lsm3b 的前体物质,lnc-Lsm3b 是 Lsm3 基因座上唯一成熟的 lncRNA。
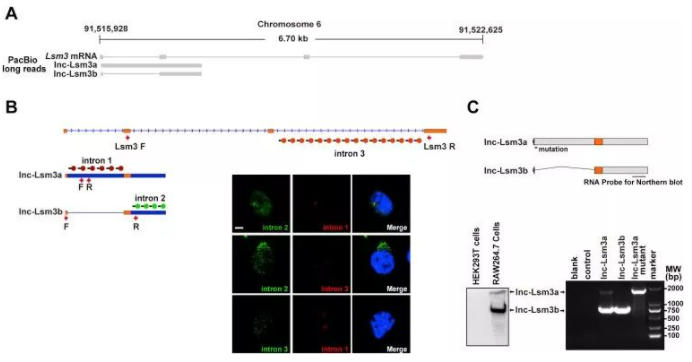
图片来源:文献截图
接着分析,lnc-Lsm3b 在病毒感染后是否会上调。
结果发现同时在细胞水平和动物水平上,外源病毒感染 lnc-Lsm3b 都会发生上调。进一步发现,是 IFN 作为启动子促进 lnc-Lsm3b 表达。
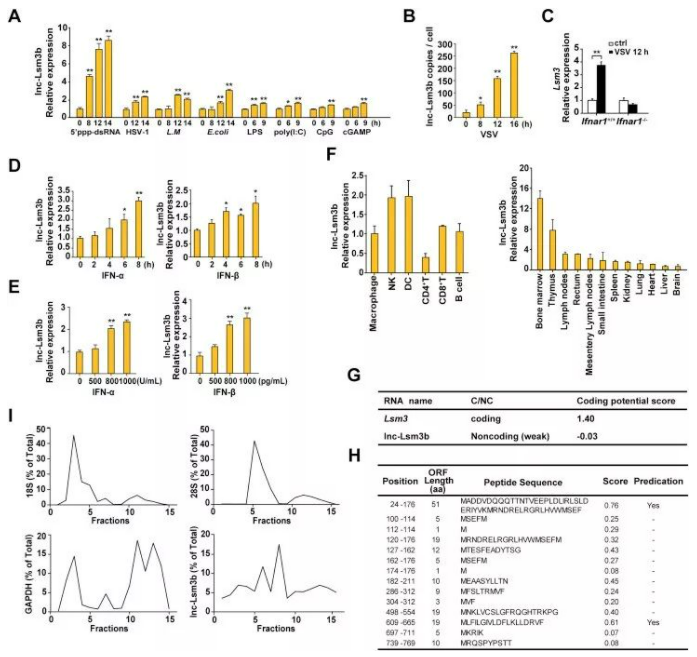
图片来源:文献截图
那 lnc-Lsm3b 是否会与 RIG-I 结合呢?
文章通过一系列实验证明:lnc-Lsm3b 的确是与 RIG-I 结合的。
团队开展了多角度的证明工作,通过干扰、敲除、过表达等技术,反复证明 lnc-Lsm3b 能够在病毒感染的细胞中,通过「分子诱饵」的方式锁定 RIG-I,使其不与病毒 RNA 结合。
图片来源:文献截图
那结合的机制,是怎么回事呢?
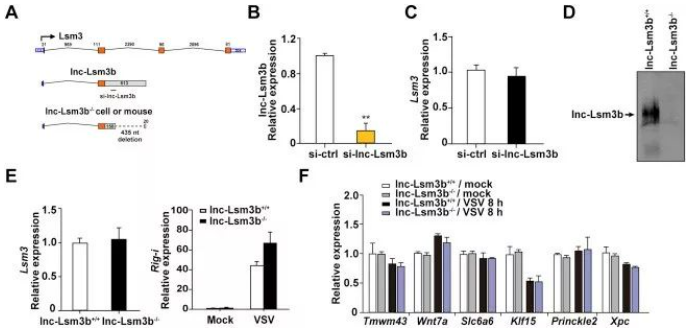
接着文章进行了机制的探究,作者试图证明 lnc-Lsm3b 是否会抑制 RIG-I 介导的信号通路,通过敲除、rescue 等大量实验验证这个思路,结果显示 lnc-Lsm3b 在敲除的细胞中显著增强。
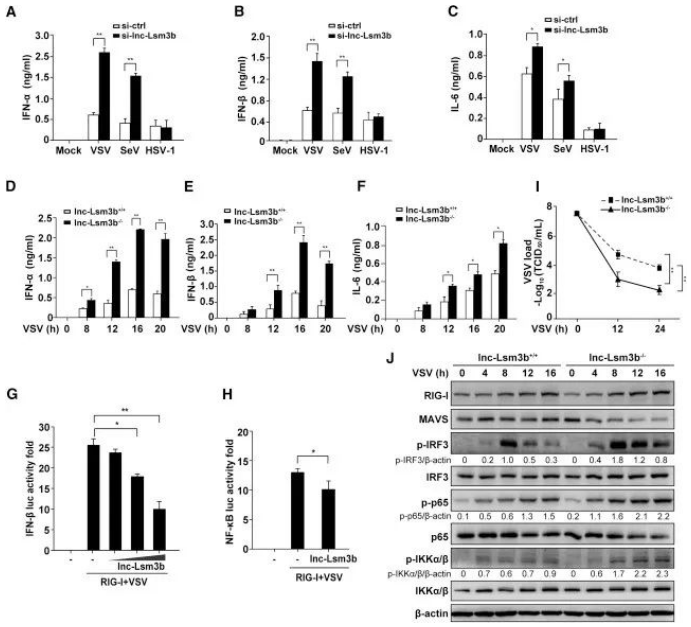
图片来源:文献截图
同时,在动物水平也证明 lnc-Lsm3b 缺陷的小鼠 IFN-I 的产生显著升高。
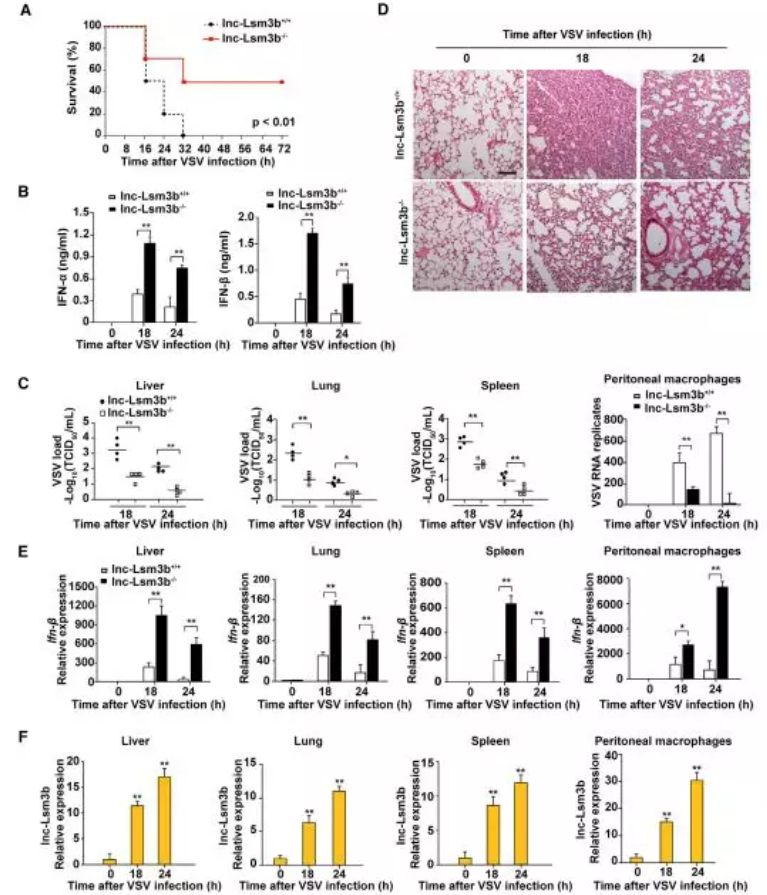
图片来源:文献截图
从整体来看,外源性 RNA 病毒入侵后会产生大量的 IFN-I ,同时能够诱导机体产生 lnc-Lsm3b,而 lnc-Lsm3b 可以与外源性 RNA 病毒竞争性结合 RIG-I 并且使其构象发生改变,最终使 IFN-I 产生减少来维持免疫稳态。
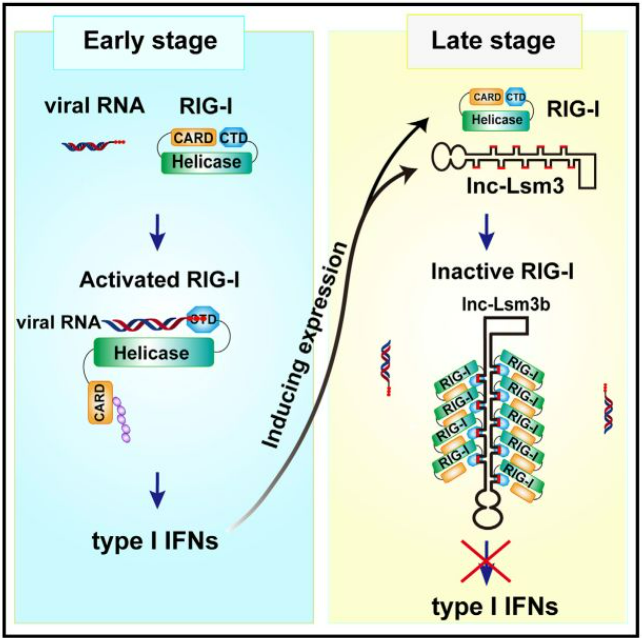
图片来源:文献截图
当然,能发在《Cell》期刊上,除去课题创新、思路严谨、工作量大外,还有更多其他亮点:
如何证明一条 lncRNA 是 lncRNA;全面严谨的发现,并且鉴定了一种全新 lncRNA 的功能;用世界领先的 CLIP(交叉互连免疫沉淀) 技术,明确 RNA 的哪一个点和蛋白质相互作用……
总之,文章巧妙地将 lncRNA 研究方法应用在 RIG-I 免疫模型中,为自身免疫病提供了一种潜在的治疗策略。
是不是有点打通任督二脉的感觉?
恭喜你,你也可以喜提一篇 Cell(手动偷笑)。