阻碍人类繁衍生息的居然是这种基因……
生物学霸
2335
2016 年 1 月 21 日,复旦大学生物医学研究院王磊教授及其团队在国际顶级医学杂志《新英格兰医学杂志》上阐述了导致人类卵母细胞成熟障碍的遗传机制(本工作中的外显子测序工作由晶能生物技术(上海)有限公司完成,本文翻译是由晶能生物完成)。
王磊教授一直致力于利用分子遗传学手段寻找人类生殖疾病相关致病基因,并利用细胞、动物模型对相关基因功能展开深入的研究,在本次研究中,他利用遗传及功能基因组学手段揭开了人类卵子成熟障碍之谜。
文章摘要
人类生殖繁衍主要依赖于成熟卵细胞和精子融合形成的受精卵,但是阻滞人卵细胞成熟的遗传机制至今未知。
研究人员利用外显子组测序技术对不孕症患者四代家系中的五名成员进行研究,其中三名患者因卵母细胞第一次减数分裂受到抑制而导致不孕。接着对这五名患者及家系中的其他成员,加上另外 23 个患病家系的 DNA 样本,利用 sanger 测序检测候选基因 TUBB8 的突变情况。然后利用 RT-PCR 技术检测卵母细胞、早期胚胎、精子细胞和部分组织中的 TUBB8 和其他 β-微管蛋白亚型的表达。
α-微管蛋白多肽和 β-微管蛋白多肽组装形成异二聚体,研究人员利用实验评估 TUBB8 突变是否影响体外异二聚体组装、HeLa 细胞系中的微管结构、酵母细胞中的微管动力学以及小鼠和人类卵母细胞的纺锤体组装。
结果研究者在灵长类动物特有基因 TUBB8 中鉴定出七个突变。24 个家系中,其中七个家系的卵母细胞第一次减数分裂阻滞是由该基因突变引起。TUBB8 在卵母细胞和早期胚胎中特异表达,该基因编码几乎所有表达的微管蛋白。
TUBB8 发生突变影响依赖伴侣蛋白的折叠以及 α/β-微管蛋白异二聚体组装过程,破坏了体外培养细胞的微管表达方式,改变了体内微管动力学,导致纺锤体组装过程出现严重缺陷,进而造成小鼠和人类卵母细胞的发育停滞。
最后研究者得出结论,TUBB8 突变具有显性负效应,可破坏微管功能并影响卵母细胞减数分裂纺锤体组装过程及卵细胞的形成,从而导致女性不孕。
研究背景
处于减数第二次分裂中期的卵母细胞与精子发生融合形成受精卵,人类的生殖繁衍真正开始。人卵母细胞进行减数分裂,在新生的卵巢中卵母细胞周期停滞于减数第一次分裂前期,直至青春期在促黄体激素的刺激下重新开始并进行排卵。
卵母细胞停滞在减数第一次分裂前期含有完整的细胞核,被称为胚泡,在重新获得减数分裂的能力时胚泡破裂。胚泡破裂后,第一次减数分裂中期通过不对称分裂产生一个极体和一个卵细胞进入第二次减数分裂。成熟的卵母细胞停滞在第二次减数分裂的中期。对绝大多数的哺乳动物而言,这一阶段是能否成功受孕的关键。
体外受精(IVF)产生的婴儿占全世界新生儿的 1~3%。在卵巢及人体绒毛膜促性腺激素的作用下,部分卵母细胞仍未发育成熟的临床病例普遍存在,但是卵母细胞全部不能发育为成熟卵细胞被报道的仅有很少几例,并且造成这种临床表型的遗传机制完全未知。
实验方法
研究对象:24 个具有卵子成熟障碍的家系
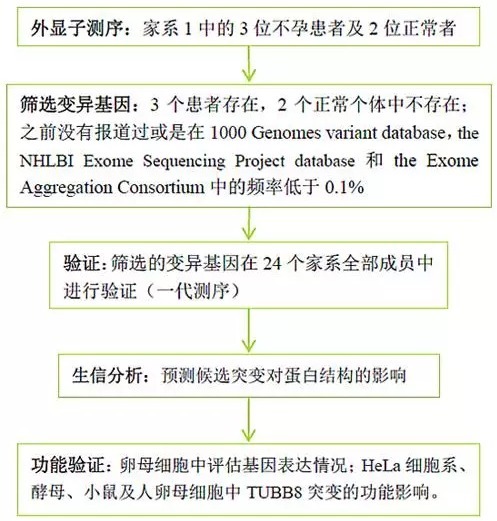
研究思路:


实验结果展示
研究人员对一个具有常染色体显性遗传模式的四代家系(家系 1)进行研究(图 1)。女性患者的配偶为正常健康男性。

患者 III-5 试图进行体外受精,结果卵母细胞处于减数第一次分裂中期(表 1),即使在体外培养也不能发育为成熟的卵细胞。
表 1:七个家系不孕患者中含有 TUBB8 突变卵母细胞的特征及临床特征


对不孕患者 III-4 的三个处于减数第一次分裂中期和一个表型不正常的卵细胞注射精子,在显微镜下观察发现,没有一个卵细胞可形成纺锤体(图 2A 和 2B)。全外显子测序分析家系 1 中的五位成员(三个患者和二个正常),结果鉴定出一个突变位点:TUBB8 基因编码区杂合性错义突变 c.T686C(p.V229A)。
TUBB8 基因编码灵长类动物特有的 β-微管蛋白亚型。这一突变在家系 1 中的不孕女性中共分离并且表现为父系遗传模式(图 1)。
除此之外,研究人员还在七个临床表型相似的不孕患者中鉴定出 TUBB8 另外六个突变位点,具体信息如下:
家系 2 中两位患者(c.G1249A,p.D417N);家系 5 中的一位患者(c.T1088C,p.M363T);家系 6 中的一位患者(c.G5A,p.R2K)以及家系 7 中一位患者(c.G900A,p.M300I),再加上家系 3 和 4 中的 denovo 突变(c.C527T,p.S176L 和 c.G785A,p.R262Q)(图 1)。
分别对家系 1、2、3、4 和 6 中不孕患者的处于减数第一次分裂中期的卵母细胞进行免疫染色,结果显示卵母细胞中的纺锤体要么为非正常状态,要么检测不到纺锤体存在(图 2C)。
因此,所有的不孕患者均不能生成成熟的处于减数第二次分裂中的卵母细胞。针对不同发育阶段的卵母细胞利用特异抗体进行免疫染色,结果证实 TUBB8 定位于纺锤体中。


图 2 卵细胞成熟受抑制的表型
A 正常卵母细胞显微拍摄图 黑色箭头标示第一极体,白色箭头标示纺锤体
B 家系 1 中不孕患者 III-4 的卵母细胞显微拍摄图 观测不到正常纺锤体及第一极体
C 正常卵母细胞及不孕患者的卵母细胞免疫染色图 蓝色标示纺锤体,绿色标示 DNA
为了检测体内 TUBB8 突变对微管产生的影响,研究人员将 FLAG 标记的重组质粒转染 HeLa 细胞系。转染野生型 TUBB8 的细胞系中,可观察到组装正常的微管网络(图 3A),而转染突变型 TUBB8,不论是正常还是高水平表达,组装出的微管均呈现出不正常表型,并且会导致微管网络的整体缺失。
这种缺失表型与预测的可能干扰异二聚体稳定性,β-微管蛋白折叠,或者聚合作用的突变(V229A、S176L、M363T、R2K 和 M300I)显着相关。微管组织结构变异表型则由干扰驱动蛋白结合相关的突变(R26Q2 和 D417N)引起(图 3B)。



图 3 HeLa 细胞系中 TUBB8 突变对微管组织产生影响
细胞系中转染野生型及突变型 TUBB8,然后进行免疫荧光染色 A 绿色为转染基因表达情况红色为内源性微管网络 B 对图 A 中的结果进行定量分析。
为了确立 TUBB8 突变和不孕表型之间的必然联系,研究人员将野生型和突变型的 TUBB8 RNA 显微注射小鼠卵母细胞。注射野生型 TUBB8 RNA 的卵母细胞,在胚泡破裂大约 12 h 后形成正常的成熟卵母细胞,而注射任何一种突变的 TUBB8 RNAs 导致卵母细胞成熟受到抑制,并且形成畸形的纺锤体。
同时,第一极体排除率显著降低(6-33% vs 61±2.2%)(图 4A)。研究人员将显微注射的 RNA 浓度提高(1000 ng/uL),结果显示,高浓度的突变型 TUBB8 RNA(S176L 和 D417N)最终导致纺锤体严重甚至彻底受损(图 4B),出现卵母细胞成熟障碍表型。
为了进一步验证 TUBB8 这一突变效应,研究人员将 TUBB8 S176L 和 D417N 突变型 RNAs 显微注射入人类胚泡期的卵母细胞,结果显示纺锤体的组装严重或者彻底受损(图 4C)。与小鼠卵母细胞用相同方式处理,结果一致。

小鼠及人卵母细胞中表达突变型 TUBB8
A 小鼠卵母细胞中注射 TUBB8 突变型 RNA 及野生型 RNA 后极体排除率比较
B 小鼠卵母细胞中注射突变及野生型 TUBB8 胚泡破裂 12 h 后免疫染色图
C 人卵母细胞中注射突变及野生型 TUBB8 胚泡破裂 16 h 后免疫染色图,蓝色为染色体绿色为纺锤体红色为 TUBB8
文章来源:晶能生物
图片来源:Mutations in TUBB8 and Human Oocyte Meiotic Arrest