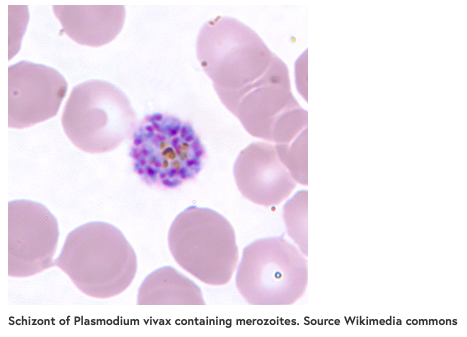
间日疟原虫疟疾:红细胞入侵的另一个关键
已知引起间日疟原虫的寄生虫通过附着在细胞表面的达菲抗原优先入侵未成熟的红细胞。一个额外的,必要的受体/配体相互作用现已被确定。
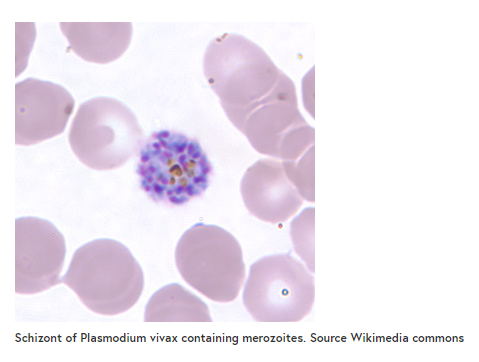
与疟疾最常见的特征之一是在感染后数月或数年内疾病的反复发作,但并不是所有感染人类的疟原虫都会导致这些复发。大多数复发的疟疾病例是由间日疟原虫引起的。这是间日疟与由更致命的物种——恶性疟原虫——引起的疾病的几个不同之处之一。
间日疟原虫疟疾
这种症状的复发是因为一些寄生虫可以在肝细胞内长期休眠;这种策略可以延长寄生虫的生命周期,前提是周围没有蚊子将其传播给另一个人。这一点,加上它在温度低于恶性疟原虫的情况下在蚊子中繁殖的能力,使它的分布能够延伸到温带气候。间日疟占亚洲和南美洲疟疾病例的65%,但在非洲大陆的大部分地区却没有。
红细胞入侵
间日疟原虫和恶性疟原虫的另一个主要区别是疟原虫入侵的红细胞类型。经历这种入侵的寄生虫的阶段是分生子。
入侵是一个多阶段的过程,由识别和附着,红细胞膜。这之后是定位和形成一个紧密的连接之间的寄生虫和宿主膜入侵前。
间日疟原虫的分生子并不利用成熟的红细胞,而是优先侵入未成熟的红细胞,即网织红细胞。与网状细胞表面的连接是通过其表面的一种被称为达菲抗原(DARC)的蛋白质实现的,DARC是几种趋化因子的受体。大多数非洲土著人口携带该基因的沉默等位基因,不表达DARC,从而保护他们的网状细胞不受间日疟原虫的入侵,并解释了该大陆没有间日疟原虫疟疾的原因。
分生子产生一种与DARC结合的分子,称为达菲结合蛋白。它位于被称为微粒体的细胞器中分生子的顶端,在分生子与网状细胞表面结合之前被释放。达菲蛋白被认为是一种可能的疫苗靶点,因为针对它的抗体可以阻止网状细胞的入侵。
两个观测表明,DARC /达菲结合蛋白相互作用不是唯一参与绑定裂殖子的网织红细胞DARC-negative一些人感染间日疟原虫和DARC表面也存在成熟的红细胞,然而这些都不是由间日疟原虫入侵。额外的受体/配体相互作用被认为是参与。
正如它们的名字所暗示的,一种被称为间日疟原虫网状细胞结合蛋白家族(PvRBP)的蛋白质也被证明参与了分生子与网状细胞的结合,但直到最近才发现它们结合的受体。
额外受体/配体系统的识别
转铁蛋白受体1 (Transferrin receptor 1, TfR1)是一种表面蛋白,作为铁负荷转铁蛋白的受体,参与铁在红细胞中的摄取。它存在于网状细胞表面,但在成熟时消失。间日疟原虫优先侵入表达高水平这种受体的网状细胞。网织红细胞结合蛋白家族PvRBP2b已被证明优先与表达TfR1的网织红细胞结合。
一组多国研究人员证实了TfR1/PvRBP2b受体/配体在网状细胞入侵中的性质和重要性,他们的发现最近发表在《科学》杂志上。
调查
最初,他们发现,如果使用酶将TfR1受体从网状细胞表面去除,或者使用抗TfR1单克隆抗体阻断受体位点,重组PvRBP2b与网状细胞的结合就会消失。免疫沉淀实验表明,PvRBP2b与TfR1的结合具有直接特异性;间日疟原虫网状结合蛋白家族的其他成员没有与之形成复合体。
TfR1受体
通过竞争性结合实验,研究人员证实TfR1的顶端区域是PvRBP2b的结合位点。此外,利用末端区域外侧表面缺乏单一甘氨酸的重组TfR1,该氨基酸对结合位点的重要性被证明,因为PvRBP2b与该重组蛋白结合的能力被完全消除。
结合蛋白
利用该分子的重组片段确定了PfRBP2b的n端结构域与受体TfR1结合的重要性。然而,结合功能研究的结构分析显示,c末端片段也需要形成功能结合位点。在n端区域针对3个表位的单克隆抗体抑制了PvRBP2b与TfR1的结合。
入侵检测
除了研究配体与受体分子结合的实验外,研究人员还进行了实验,以确定这种结合是否参与了网状细胞的入侵过程。获得了表达TfR1较低表面水平的jkRBCs的突变克隆,并与间日疟原虫和恶性疟原虫merozoites孵育。在突变体细胞中,间日疟原虫的侵袭减少了10倍,这说明了转铁蛋白受体TfR1在侵袭过程中的重要性。相比之下,恶性疟原虫的入侵不受可用TfR1减少的影响。
最后,将针对PvRBP2b n端3个表位的单克隆抗体加入到巴西和泰国的间日疟原虫分离株中,可以抑制红细胞的侵袭。
因此,如果TfR1不可用或PvRBP2b分子上必要的表位被阻断,则不会发生侵袭。
结论
这项综合研究很好地揭示了一种附加元素在间日疟原虫入侵红细胞过程中的重要作用。本文作者认为,PvRBP2b/TR1结合对红细胞的初始识别和入侵承诺具有重要意义。其次是PvDBP与DARC受体之间的相互作用、紧密结合的形成和侵袭。
确认第二种受体/配体相互作用的重要性,强调了进一步分子相互作用的可能性,并确定了更多可能的疫苗靶点。