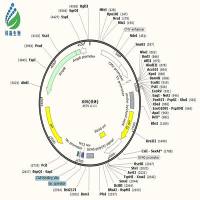
灵长类哺乳动物感染模型-肠出血性大肠埃希菌动物模型
相关实验:肠出血性大肠埃希菌动物模型
别名:Animal models of Infection disease,baboon,macaque
最新修订时间:
简介
灵长类哺乳动物感染模型,狒狒和恒河猴的遗传背景与人更相似,具体表现在志贺毒素受体 Gh3 在肾脏、小肠等脏器的分布与人的高度一致性,所以这两种动物特别是狒狒是较为理想的研究毒素以及溶血尿毒综合征的模型 C 研究发现引起拂拂肾衰竭及 HUS 典型症状的毒素用拭与人休用量一致,再次证实了二者的高度相似性, 除了毒素效应外,A/E 损伤及肠炎也能在恒河猴感染模型中稳定地观察到。该模型的最大不足就是实验动物购买、饲养及管理成本较高,几乎无法推广。
原理
灵长类哺乳动物感染模型的基本原理主要由 Stx 毒素介导。将纯化的毒素直接通过静脉或腹腔注射,毒素入血后与动物肾脏内皮细胞 Gh3 受体结合并导致细胞死亡,最终引起肾衰竭及溶血尿毒综合征。
用途
广泛应用于 EHEC 致病机制的研究,特别是 EHEC 介导的宿主上皮细胞 A/E 损伤的信号分子转导的研究。由其衍生的猪肠组织体外培养已经被公认为 A/E 损伤研究 ex vivo 模型的标准之一。此外,该模型还用于毒素的致病机制以及以毒素为靶点的治疗药物评价等方面。
材料与仪器
步骤
A. 毒素的纯化:
B. 毒素攻毒:
实验开始时狒狒需禁食 24 小时,在次日恢复供水后肌内注射凯特明 [ (14 士 0.5) mg/kg]
C. 模型观察:
攻毒 48 小时内观察狒狒死亡情况,可以处死动物,取肾脏、大肠、小肠、心脏、肺、脾、脑等组织切片进行 HE 染色或电镜观察 HUS 相关的脏器病例改变,如需测定血压、中心静脉压、心电图等指标,可以通过手术植入遥测芯片,动态实时监测毒素导致的病例改变。
来源:丁香实验