单细胞测序技术之肝细胞相关实验方案策略
烈冰生物
肝细胞癌(HCC)是肝癌的主要组织学亚型,占原发性肝癌的 90%,是全世界癌症相关死亡率的第三大常见原因。肝癌的诱因诸多,譬如遗传、表观遗传改变、慢性乙型肝炎、肥胖和糖尿病等都是肝癌的主要危险因素,而且肝癌预后差,复发率和转移率高。因此本篇应用单细胞测序技术研究案例分享以孙倍成教授带领其研究团队发表在国际免疫学顶级期刊 Immunity 上的肝癌(HCC)炎癌转化调控新机制说起!
1.文章介绍
论著题目:The zinc finger protein Miz1 suppresses liver tumorigenesis by restricting hepatocyte-driven macrophage activation and inflammation
发表期刊:Immunity
影响因子:43.474(2022 年最新数据)
2.实验基础信息
样本信息:
对照组:WT 小鼠
实验组:除 WT(untreated)外,其它组小鼠(雄性)均出生后两周开始注射 DEN,后期每周注射 CCl4 以诱导肝癌的发生。
单细胞捕获平台:10X Genomics
单细胞实验分组:Miz1∆hep:Miz1F/F=2:2
捕获细胞数:
总细胞数 24802 个(Miz1∆hep:13753 个,Miz1F/F:11049 个)
其中,肝细胞 1343 个(9.5% total cell,Miz1∆hep:1343 个,Miz1F/F:1022 个)
巨噬细胞 4277 个(17.2% total cell,Miz1∆hep:2934 个,Miz1F/F:1343 个)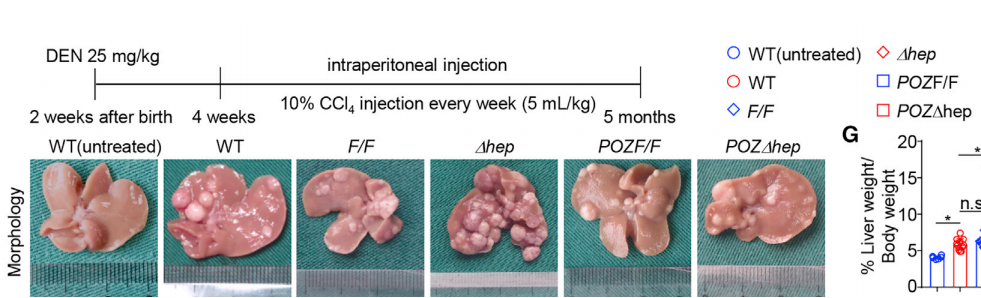
技术手段
磁共振成像(MRI)、HE 染色、免疫荧光、免疫组化、免疫印迹分析、单细胞转录组测序、FACS 分选验证
分析工具应用
t-SNE 分析、细胞类型鉴定、细胞类型细分鉴定、差异基因表达分析、Pseudo-time 分析、Qusage 分析、细胞通讯分析
3.结果解析
(1) Miz1 缺失促进肝细胞增殖和HCC敏感性
研究者在 DEN/CCl4 诱导肝癌的小鼠模型中,通过核磁共振,HE 染色成像和相关数据统计,发现 Miz1∆hep 小鼠的肝损伤并不是晚期肿瘤诱导的结果,但肝细胞转录因子 Miz1 的缺失促进了肝细胞的增殖和细胞凋亡减少,同时,Miz1∆hep 小鼠对化学物质或炎症相关的 HCC 的敏感性增加。
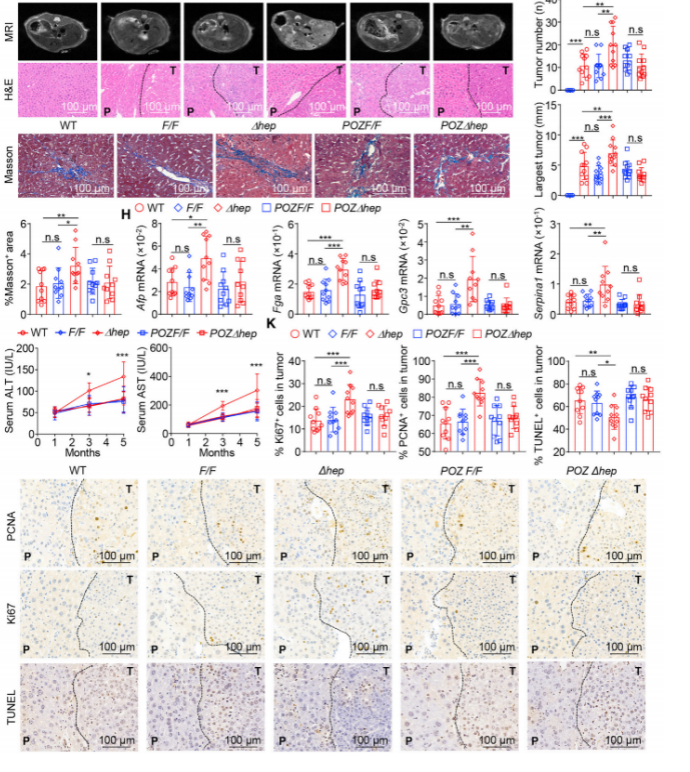
(2)Miz1 缺失促进核因子(NF-κB)激活
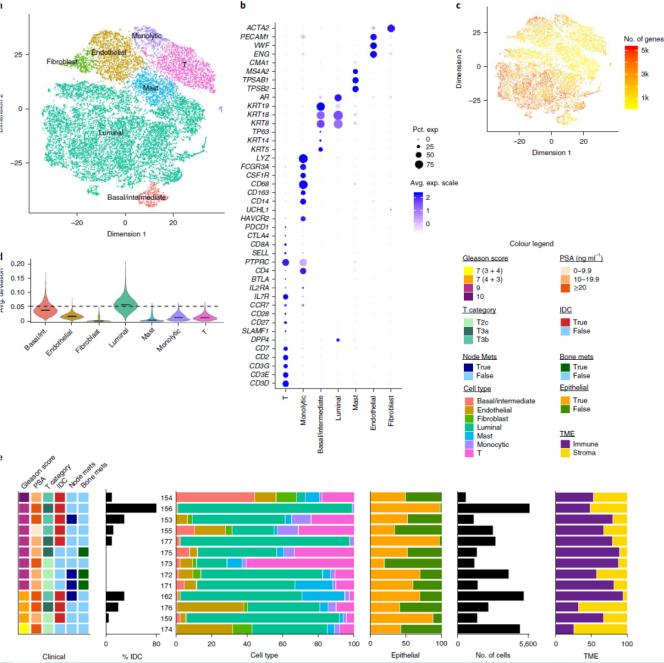
接着,研究者对 Miz1F/F 和 Miz1∆hep 两组小鼠样本进行了单细胞测序,共获得 24,802 个细胞,注释细胞类型主要包括肝实质细胞(2365 个,9.5% total cell),中性粒细胞,内皮细胞,树突状细胞,B 细胞,T 细胞和巨噬细胞(4277 个,17.2% total cell)。对肝细胞群体进一步进行 subCluster,拟时序分析,差异基因表达分析发现,Miz1∆hep 小鼠产生了独特的肿瘤肝细胞群体,该群细胞高度表达 NF-κB 下游的细胞因子和驱化因子。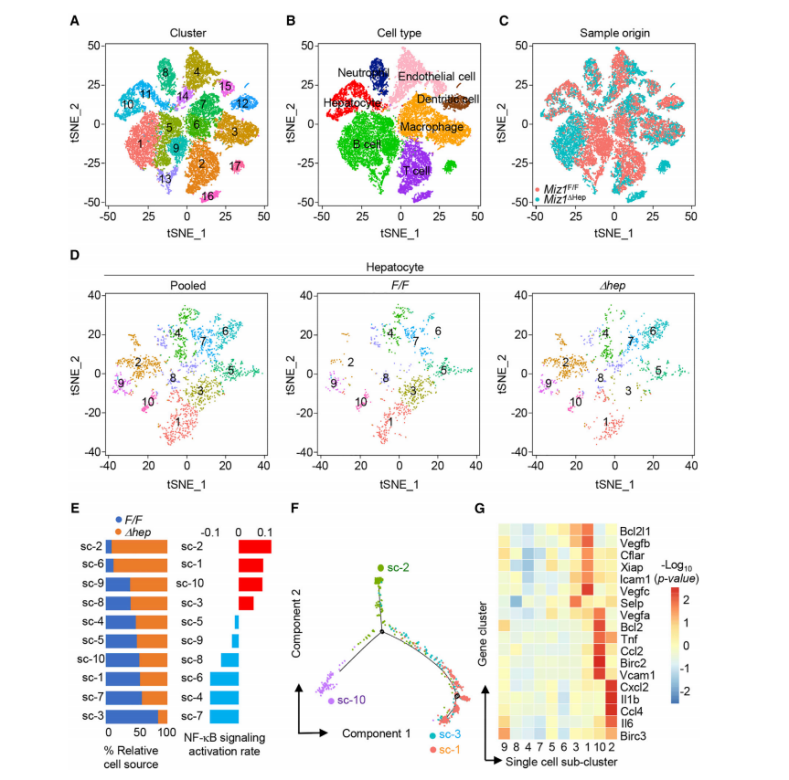
进一步,研究者通过免疫印迹和免疫组化分析证实,肝细胞 Miz1 的缺失促进 IKK 介导的 MTDH 的磷酸化,从而促进了 NF-κB 的激活和 NF-κB 下游炎症相关靶基因的表达。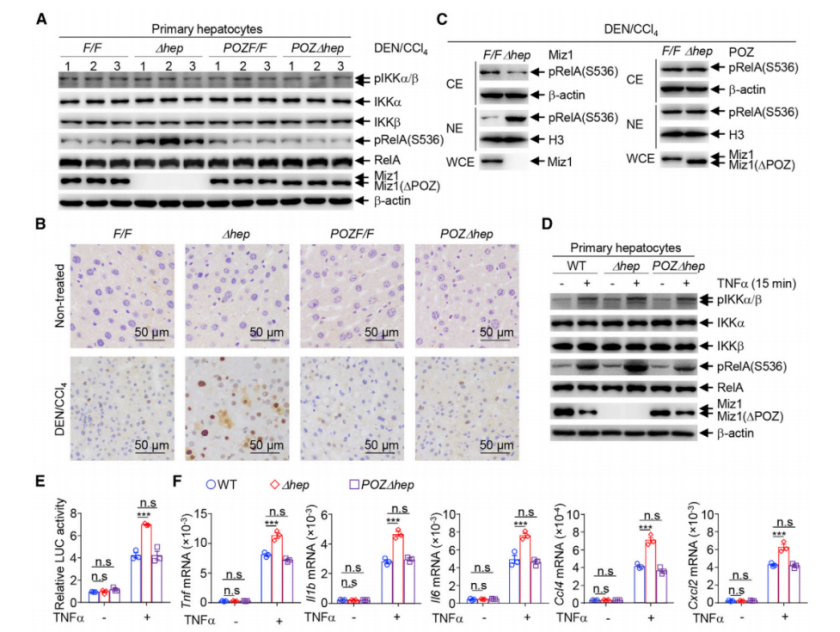
(3)肿瘤特有肝细胞分泌细胞因子促进肿瘤浸润巨噬细胞向促炎表型转化
对巨噬细胞亚群和肝脏特有巨噬细胞(Kupffer cell)进一步细分,并进行差异基因分析和 Qusage 分析,发现 Miz1∆hep 小鼠的肿瘤浸润巨噬细胞和 Kupffer 细胞的一些亚群 NF-κB 强烈激活,肿瘤浸润巨噬细胞向促炎表型转化。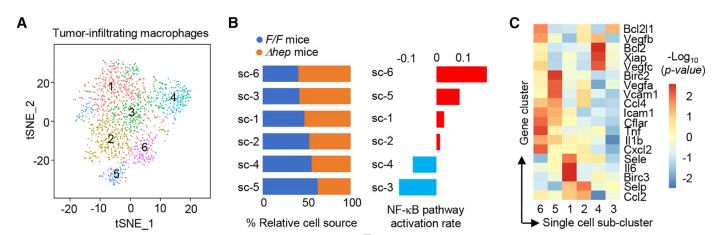
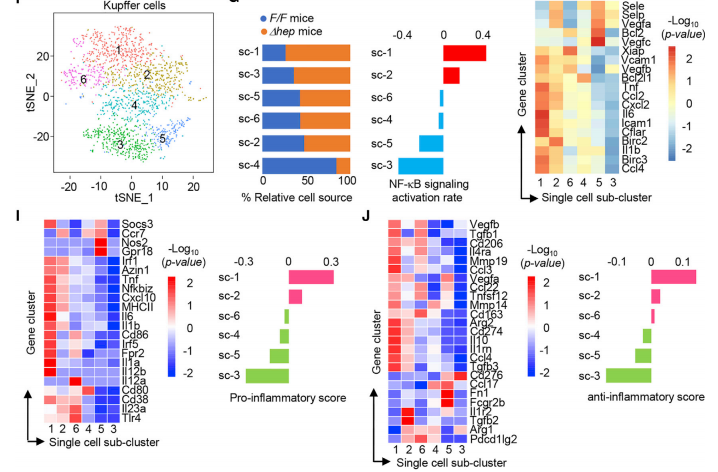
究其原因,研究者发现,肿瘤特有的肝细胞能促进炎性细胞因子分泌(TNF-α,IL-1β, IL-6 等)和相关基因表达,驱动肿瘤浸润的巨噬细胞向促炎表型倾斜,巨噬细胞受其驱动,IL-1β, IL-6 的基因表达上调,促炎性细胞因子增加并驱动了 HCC 中的炎症。对炎性巨噬细胞消除处理(GdCl3)后,小鼠肝脏/体重比、最大肿瘤直径有所恢复。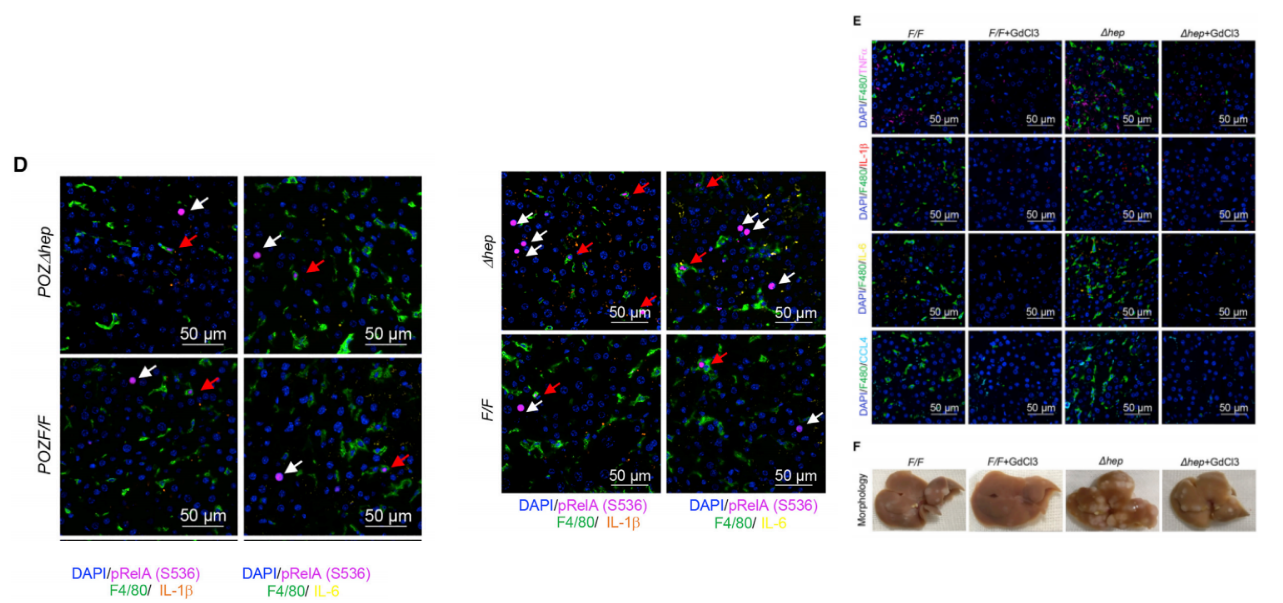
Miz1 抑制肿瘤发生机制在于:1.Miz1 与 RelA 竞争结合癌蛋白 MTDH。2.抑制IKK 酶活性降低 MTDH 磷酸化。相关临床试验也证实了 Miz1 在不同 HCC 患者中的表达与肝细胞 RelA 和 MTDH 的磷酸化呈反相关,与 HCC 患者复发和整体预后也密切相关。
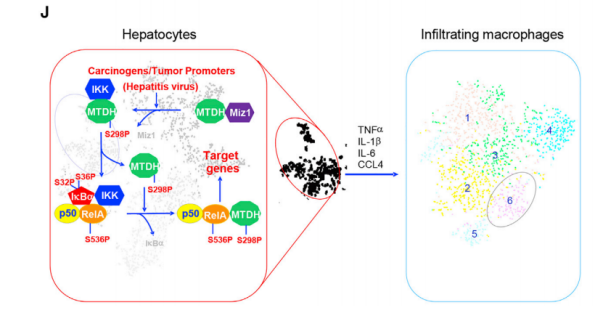
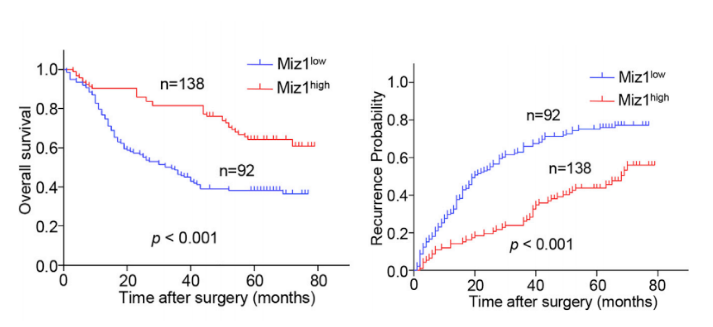
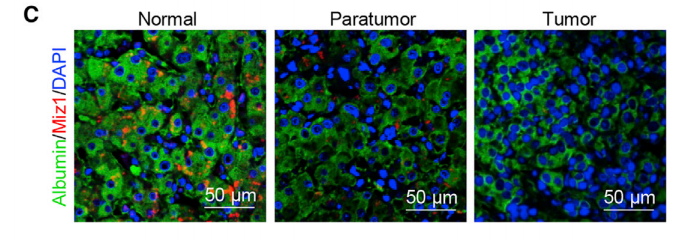
因此,整理一下思路:本研究基于单细胞测序和其它组学分析,结合多种体内、体外实验,发现小鼠肝细胞中转录因子 Miz1 缺失,产生了高表达 NF-κB 下游炎症因子的特异性“炎性”肝细胞亚群,激活肿瘤浸润巨噬细胞向促炎表型转化,增强肝脏炎症反应,促进肝癌的发生发展。
文章图文来源:烈冰生物