Nat Nanotechnol:T 细胞免疫活性的可视化调控研究进展
丁香学术
近日,厦门大学周子健研究员与新加坡国立大学陈小元教授和广州医科大学郭伟圣教授合作在国际顶级学术期刊 Nature Nanotechnology 上发表了题为 Targeting the activity of T cells by membrane surface redox regulation for cancer theranostics 的研究论文。该研究针对 T 细胞在活性氧微环境中发生免疫活性耗竭的关键科学问题,首次利用化学生物学手段靶向捕获 T 细胞膜表面活性氧,实现了 T 细胞免疫活性的在体可视化调控。
虽然免疫治疗策略在抗肿瘤研究中取得了令人鼓舞的成绩,但是由于免疫系统的复杂性以及肿瘤微环境的异质性,免疫治疗在临床肿瘤患者中的综合响应率仍然较低(不足 30%)。基于免疫激活策略的肿瘤治疗效果很大程度上依赖于免疫 T 细胞在肿瘤中的杀伤活性。然而,肿瘤中浸润的 T 细胞可能受到肿瘤微环境的影响,导致其降低或丧失活性(包括增殖和免疫活性等),这一现象被称为 T 细胞「耗竭」。例如,2019 年荷兰 Ton N. Schumacher 团队在肠癌和卵巢癌患者中对于肿瘤浸润 T 细胞的 TCR 受体进行了单细胞测序分析,结果显示,我们通常认为的起作用的效应 T 细胞,也就是 CD8+ T 细胞,仅有约 10% 具有识别肿瘤细胞的活性,其余 90% 均扮演着旁观者的角色。也就意味着,由于 T 细胞存在「耗竭」现象,我们通过传统方法认为的肿瘤中效应 T 细胞的数量,可能无法准确反映其免疫活性。因此,对于肿瘤中 T 细胞在体免疫活性的探索对于肿瘤治疗调控和预后评价具有重要意义。
研究表明,T 细胞的增殖、识别并杀伤肿瘤细胞的免疫活性受到多种因素的影响,比如物理温度、生物抗原刺激等,而肿瘤微环境中的活性氧 ROS 可以氧化 T 细胞膜表面的巯基-SH,使其变为双硫键 S-S,是介导 T 细胞免疫失活的重要机制之一(图 1)。瑞典 Gelderman 等人的研究发现:T 细胞的免疫活性与其膜表面还原性蛋白(例如 Trx)的自由巯基(-SH,还原态)数量成正比,而与双硫键(S-S,氧化态)数量成反比。因此,在肿瘤放疗实验中,放疗辐射产生的炎症反应一方面可以介导了 T 细胞的活化和肿瘤浸润,另一方面,炎症中的活性氧微环境也会通过氧化 T 细胞膜表面的自由巯基而影响浸润 T 细胞的免疫活性。因此,对于肿瘤微环境中的氧化还原状态的调控和监测具有很重要的意义。目前,针对 T 细胞活性的在体成像策略主要包括以下几种:直接细胞标记、抗体结合靶向、对受体或细胞因子等的标记和报告基因策略。然而,这些针对 T 细胞的活体成像方法主要是基于细胞特异性标志物的生物结合靶向策略,主要反映的是 T 细胞的数量和受体分布,难以准确揭示 T 细胞的免疫活性。传统地基于特异性标志物的生物结合靶向策略也难以靶向调控 T 细胞膜表面-SH 和 S-S 的化学平衡状态,针对肿瘤活性氧微环境中 T 细胞的在体免疫活性调控仍然存在挑战也鲜有报道。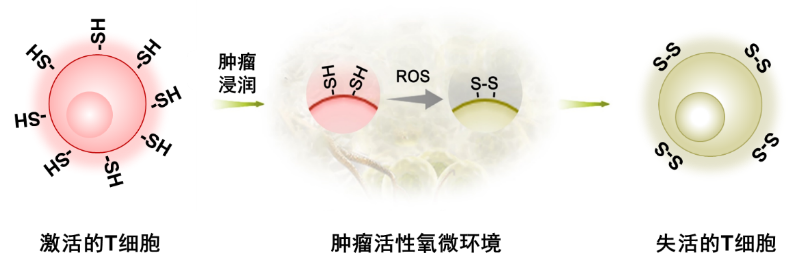
图 1:肿瘤浸润 T 细胞膜表面蛋白上的-SH 被氧化成 S-S 而失去活性的示意图
针对活性氧环境中 T 细胞耗竭而失去免疫活性的关键科学问题,我们构建了一种 T 细胞靶向的膜融合脂质体,T-Fulips(图 2)。它与 T 细胞靶向膜融合后,将一种经典的活性氧捕获剂 2,2,6,6-四甲基哌啶(TEMP)分子展示到 T 细胞的表面,捕获 T 细胞膜表面的活性氧,从而提升 T 细胞在活性氧环境中的免疫活性。同时,TEMP 分子本身由逆磁性被氧化为顺磁性的 TEMPO,激活磁共振成像,实现了 T 细胞免疫活性的可视化调控。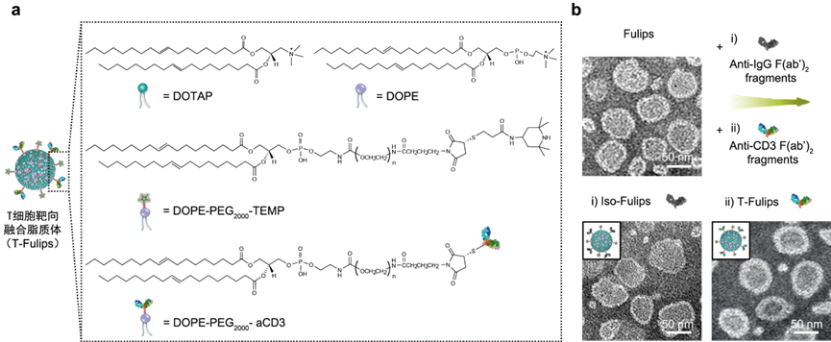
图 2:(a)T-Fulips 组分及结构示意图;(b)T-Fulips 及同型对照 Iso-Fulips 透射电镜图
本研究中,T 细胞膜上的 TEMP 基团可充当活性氧「诱饵」,使 T 细胞免受氧化引起的表面自由-SH 基团变为 S-S 基团,反之,-SH 基团被氧化降低 T 细胞的活性。与此同时,逆磁性 TEMP 基团向顺磁性的 TEMPO 自由基转变,使纵向弛豫时间(T1)以「0」到「1」的方式发生显著变化,可用于磁共振成像(MRI)对于 T 细胞的免疫活性的定性和定量评价(图 3a)。在小鼠肿瘤放疗(RT)模型中,靶向 T 细胞的融合脂质体 T-Fulips 显示出比对照组(Iso-Fulips)更高的 T 细胞活化率和肿瘤抑制率。更重要的是,TEMPO 展现出的纵向弛豫时间 T1 的变化,实现了 T 细胞活性及放疗疗效的早期预测。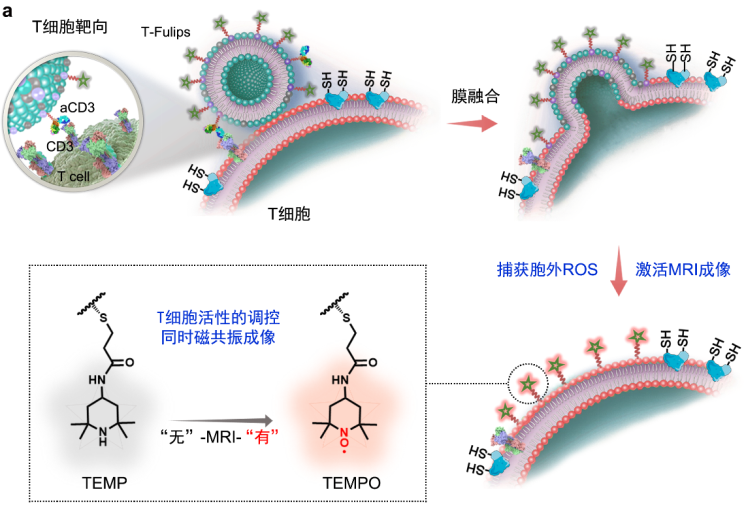
图 3:(a)本研究的设计思路示意图。
该研究利用化学生物学策略来调控并量化 T 细胞在肿瘤治疗中的原位活性,解析了炎症活性氧反应对浸润 T 细胞免疫活性影响的动态过程,为肿瘤治疗的免疫响应调控和影像预后评价研究提供了新思路。虽然该工作主要提到的是效应 T 细胞,但是通过化学生物学手段靶向氧化还原代谢可能同样适用于其它免疫细胞的调控,如 B 细胞、树突状细胞、自然杀伤细胞、巨噬细胞和中性粒细胞等。更重要的是,针对免疫细胞的功能和活性可能有望为其它免疫激活相关疾病的诊疗研究提供新思路,如病毒感染(如 COVID-19)、慢性炎症性疾病和类风湿性关节炎等。
厦门大学博士后石昌荣、硕士生张倩玉为该论文的共同第一作者,该研究得到国家自然科学基金、中国博士后科学基金、福建省科技厅中央引导地方科技发展专项和厦门大学「南强青年拔尖人才」计划项目的资助。


![十二烷基二甲基(3-磺丙基)氢氧化铵内盐 [用于生化研究],14933-08-5,≥98%,阿拉丁](https://img1.dxycdn.com/p/s14/2024/0619/475/6370229598169633081.jpg!wh200)