Cell Rep Med:李振斐 / 吴登龙 / 唐惠儒团队发现黄体酮是前列腺癌的促癌代谢物,提出晚期治疗新策略
丁香学术
随着人口老龄化社会的到来,我国前列腺癌的发病率和死亡率增长迅猛[1]。在上海等地区,前列腺癌的发病率已经超过肝癌,是男性高发癌症之一。
然而前列腺癌早期筛查尚未普及,我国初诊患者多为晚期前列腺癌,因此我国前列腺癌死亡率远高于西方发达国家。2022 年相关统计数据显示,我国每年新增前列腺癌患者 125,646 人,而美国每年新增患者 216,900 人;但是我国因前列腺癌去世的患者每年高达 56,239 人,远高于美国的死亡人数(34,611)[2]。开发晚期前列腺癌治疗的新策略是前列腺癌基础研究和临床研究共同关注的重要问题。
雄激素是驱动前列腺癌进展的重要促癌因子。人体内的雄激素主要源于睾丸分泌的睾酮(testosterone)和肾上腺分泌的脱氢表雄酮(dehydroepiandrosterone,DHEA)[3]。在临床实践中,去势治疗能够抑制睾酮产生;药物阿比特龙(abiraterone)能够抑制 DHEA 产生,然而治疗耐受依然不可避免。寻找驱动前列腺癌持续进展的新促癌代谢物、解析前列腺癌适应机体代谢重塑的机制研究将为晚期前列腺癌治疗提供潜在的新靶点。
2022 年 3 月 15 日,中科院分子细胞科学卓越创新中心李振斐课题组、同济大学附属同济医院泌尿外科吴登龙课题组和复旦大学人类表型组研究院唐惠儒课题组在 Cell Reports Medicine 在线发表了题为 Inhibiting 3βHSD1 to eliminate the oncogenic effects of progesterone in prostate cancer 的研究论文。
该研究结合临床样本和代谢组学检测技术,发现黄体酮(progesterone)是促进前列腺癌进展的新促癌代谢物;基于黄体酮的代谢和功能研究,研究人员发现小分子化合物 biochanin-A(BCA)能够靶向抑制代谢酶 3βHSD1,进而抑制黄体酮合成、克服药物耐受;并指出患者血液中黄体酮的丰度是阿比特龙疗效的潜在预测型生物标志物。
去势治疗联合药物阿比特龙能够将患者体内的雄激素控制在非常低的水平,这为寻找独立于雄激素的新促癌代谢物提供了可行性。研究人员利用接受阿比特龙和去势治疗的患者样本进行代谢组学研究。在 6625 个代谢物中,代谢物黄体酮在阿比特龙治疗后显著升高。
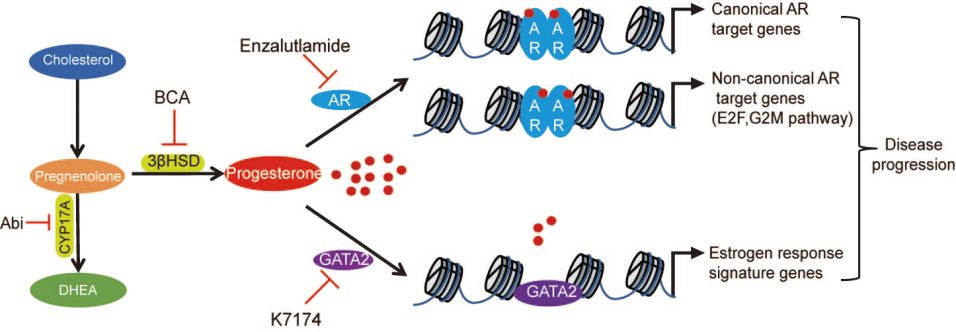
进一步的机制研究发现,高浓度的黄体酮能够结合雄激素受体(androgen receptor,AR),调控 AR 信号通路、cell cycle 信号通路、MYC 信号通路等促癌通路。该促癌效应一方面需要较高的黄体酮浓度(10~100 nM),另一方面需要较高的 AR 丰度或特定的 AR 点突变(H875Y、T878A)。
然而在临床患者中,能够同时满足这两点的患者比例不高。研究人员进一步发现,低剂量的黄体酮(~5nM)长期刺激前列腺癌细胞后,能够上调转录因子 GATA2 的丰度,进而改变癌细胞的转录组特征,激活雌激素相关信号通路,促进细胞生长。该机制研究指出不适合阿比特龙治疗的患者特征(黄体酮血液丰度显著上升、AR 丰度高或者存在突变),同时指出靶向 GATA2 克服阿比特龙耐受的治疗新策略。
随后,研究人员解析了黄体酮在前列腺癌细胞中的代谢通路及其生理功能。结合不同的研究体系,研究人员最终确认了黄体酮及其下游代谢物能够发挥促癌代谢物的功能;而其上游底物孕烯醇酮(pregnenolone)不能激活 AR 信号通路。代谢酶 3βHSD1 介导了孕烯醇酮向黄体酮的转化,因此是前列腺癌治疗的潜在靶点。
通过药物筛选,研究人员发现小分子化合物 BCA 能够抑制代谢酶 3βHSD1 活性,阻止黄体酮的产生,进而抑制前列腺癌生长。值得注意的是,代谢酶 3βHSD1 是一个重要的甾体代谢酶,其与前列腺癌疾病进展的临床相关性目前得到了多个人群队列的证实[4,5]。而目前尚无有临床应用潜能的 3βHSD1 抑制剂。BCA 是目前发现的抑制 3βHSD1 活性最强的小分子化合物,同时其广泛存在于豆类食物和保健品中,为后续患者膳食管理、开发临床可用的先导化合物奠定基础。
进一步的临床研究发现,患者血液中黄体酮含量在服用阿比特龙三个月后即出现明显上升;而此时患者血液中黄体酮丰度与患者治疗响应、治疗耐受存在相关性。在临床实践中,目前有多种药物用于晚期前列腺癌的治疗(阿比特龙,恩杂鲁胺,阿帕鲁胺等);对于同一种药物,仅有 ~30% 患者对药物有良好且持续的反应。如何筛选药物的适用人群、指导患者选择合适的治疗方案一直困扰着临床医生。黄体酮有可能成为一个可行的生物标志物来预测患者对阿比特龙的治疗响应,进而用于指导患者进行合适的药物选择。后续临床研究正在由同济大学附属同济医院泌尿科吴登龙团队推进中。
综上所述,该研究发现了黄体酮是促进晚期前列腺癌进展的新促癌代谢物。小分子化合物 BCA 能够靶向抑制代谢酶 3βHSD1,通过阻止黄体酮的合成来抑制前列腺癌疾病进展。该研究成果为晚期前列腺癌治疗提供了新的靶点和先导化合物,为病人分层(patient stratification)提供了潜在的预测型生物标志物。