施一公团队再获新进展!Mol Cell:完善人类剪接体结构「地图」,揭示外显子连接机制
生物学霸
真核生物细胞中,基因编码区(exon)由内含子(intron)隔断,在转录翻译过程中,内含子需要经过 pre-mRNA 剪接来去除。RNA 剪接是真核生物「中心法则」的关键步骤之一,是蛋白质多样性、复杂性的分子基础。RNA 剪接体缺陷是导致人类疾病的重要原因之一,据估计可能超过 60% 的疾病与 Pre-mRNA 剪接有关。[1,2]
西湖大学施一公课题组十多年来聚焦酵母及人源剪接体结构解析及分子机制研究,取得了丰硕的成果。其中包括 10 篇 Science、4 篇 Cell、1 篇 Nature、3 篇 Cell Research 等超过 18 篇研究论文,构建了剪接体研究领域的一个闭环,对于人们认识真核生物剪接体的组成和它与相应内含子的识别机制有着重要意义,对于药物靶点设计应用具有不可估量的作用。
图片来源:Molecular Cell
2022 年 6 月 14 日,西湖大学施一公团队在 Molecular Cell 在线发表研究论文 Mechanism of exon ligation by human spliceosome,利用冷冻电镜技术解析了人类剪接体复合物两种中间体 pre-undefined-I 和 pre-undefined-II 结构,整体分辨率高达 3.6 埃。该研究揭示了外显子连接前剪接体复合物 C 到 undefined 的转换,增进了人们对外显子连接机制的认识。
图片来源:Molecular Cell
pre-undefined-I 和 pre-undefined-II 复合物冷冻电镜结构
Pre-mRNA 剪接涉及两个顺序反应:分支和外显子连接。分支后的 C 复合物经过重塑成为 undefined 复合物,执行外显子连接。本文报道了两种人类剪接体中间复合物 pre-undefined-I 和 pre-undefined-II 在 3.6 埃下的冷冻电镜结构。
该研究是继施一公课题组 2017 年(Cell)解析第一个高分辨率人源剪接体 undefined 复合物结构[3]、2018 年(Science)在近原子分辨率尺度观察到人源剪接体第一部反应后的催化状态 C 复合物结构 [4] 之后,进一步揭示 C-undefined 转换的中间体结构,为理解 RNA 剪接时外显子连接过程提供了重要基础。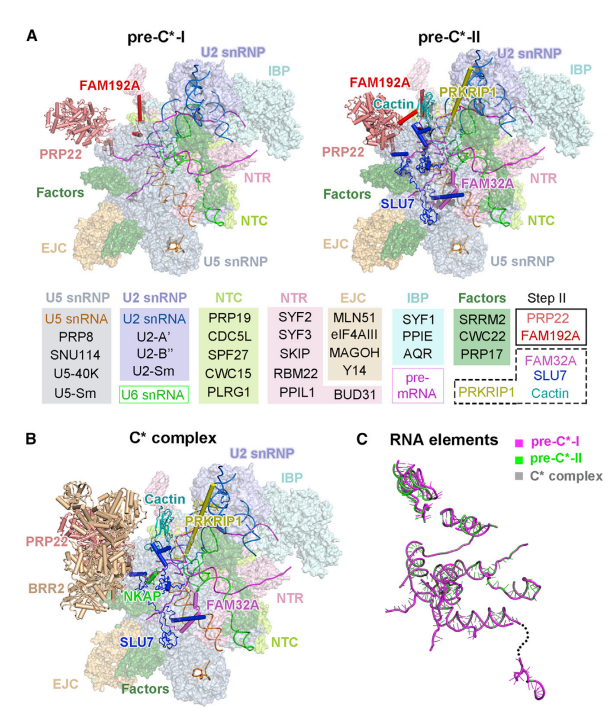
图片来源:Molecular Cell
pre-undefined-I 和 pre-undefined-II 复合物中的 3' 剪接位点与 3' 外显子识别
在这两种结构中,3' 剪接位点(SS)已经与活性位点对接,以保证 3' 外显子序列锚定在 PRP8 上。步骤 II 因子 FAM192A 则与 U2 snRNA 和分支位点二联体相接触。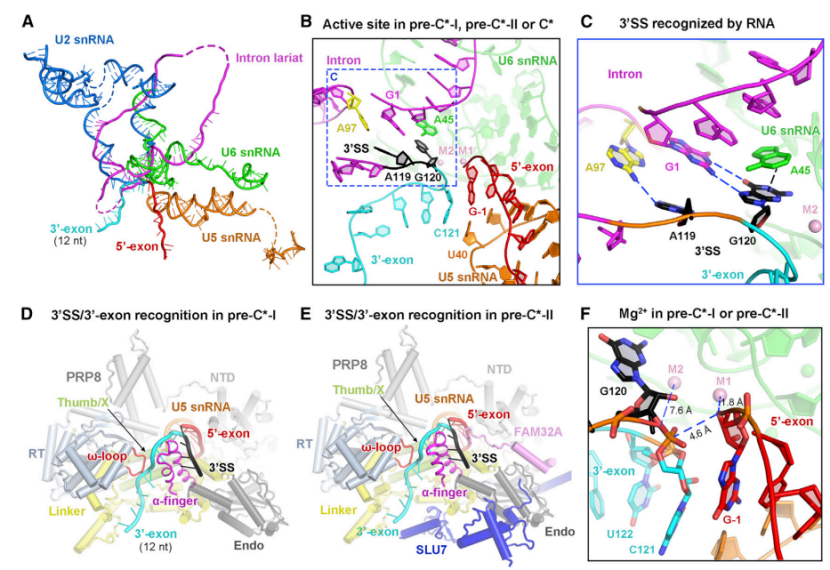
图片来源:Molecular Cell
在 pre-undefined-I 向 pre-undefined-II 过渡过程中,对步骤 II 因子 Cactin、FAM32A、PRKRIP1 和 SLU7 进行招募。值得注意的是,RNA 解旋酶 PRP22 在 pre-undefined-I、pre-undefined-II 和 undefined 复合物中的位置截然不同,提示其在 3' 外显子结合和校对中发挥作用。 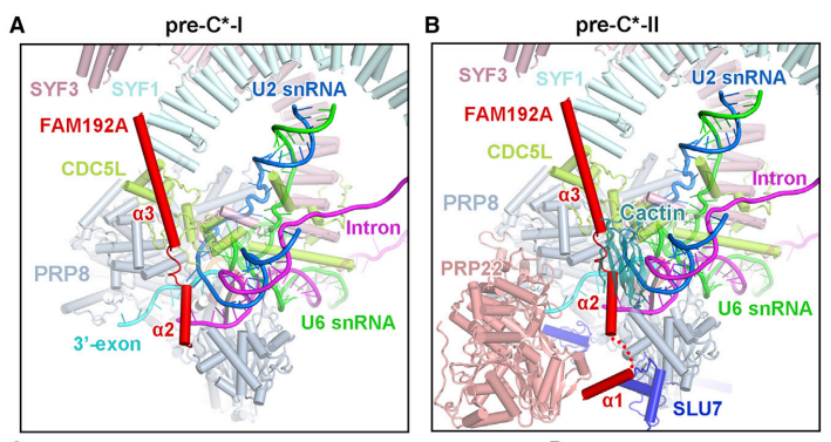
图片来源:Molecular Cell
研究总结
这项研究通过解析人类剪接体复合物两种中间体 pre-undefined-I 和 pre-undefined-II 结构,揭示了外显子连接前剪接体复合物 C 到 undefined 的转换,作者同时提出了外显子连接机制的相应工作模型。
在这个模型中,PRP16 触发剪接体复合物 C 到 undefined 的转换,导致两个第一步因子(CCDC49、CCDC94)和 5 个剪接因子(CIR1、FRG1、PPIG、PPWD1、WDR70)的相互解离。这些变化引起第二步因子 FAM192A 和 RNA 解旋酶 PRP22 的招募,最终形成 pre-undefined-I 复合物。
在 pre-undefined-I 复合物中,3' 剪接位点(SS)与 3' 外显子与活性位点对接。PRP22 在招募 Cactin、FAM32A、PRKRIP1、SLU7 等第二步因子后发生显著的位移,以准备在 pre-undefined-II 中连接 3' 末端序列和 3' 外显子。而在 pre-undefined-II 到 undefined 复合物的转换过程中,PRP22 位移到与 pre-undefined-I 中相近的位置。
以上这种 C 复合物到 undefined 复合物转换过程中,一步一步的分子组成和构象变化显示出剪接体重塑过程中动态的「分子编排」(molecular choreography )现象。

图片来源:Molecular Cell
延伸阅读
真核生物 RNA 剪接由剪接体(spliceosome)执行,是 pre-mRNA 前体成熟、去除内含子的必经过程。剪接体是细胞中已知的最复杂的分子机器,是由蛋白质-核酸形成的复合物组装形成,具有高度动态的特点,结构解析难度极大。
施一公课题组在剪接体结构及分子机制领域深耕多年,对 pre-mRNA 与剪接体的识别、组装、激活、催化等一系列过程及中间态进行了系统研究。根据剪接体的组成与构象不同,剪接体可分为 E、A、B、Bact、undefined、C、undefined、P 等状态,如下图示[5]。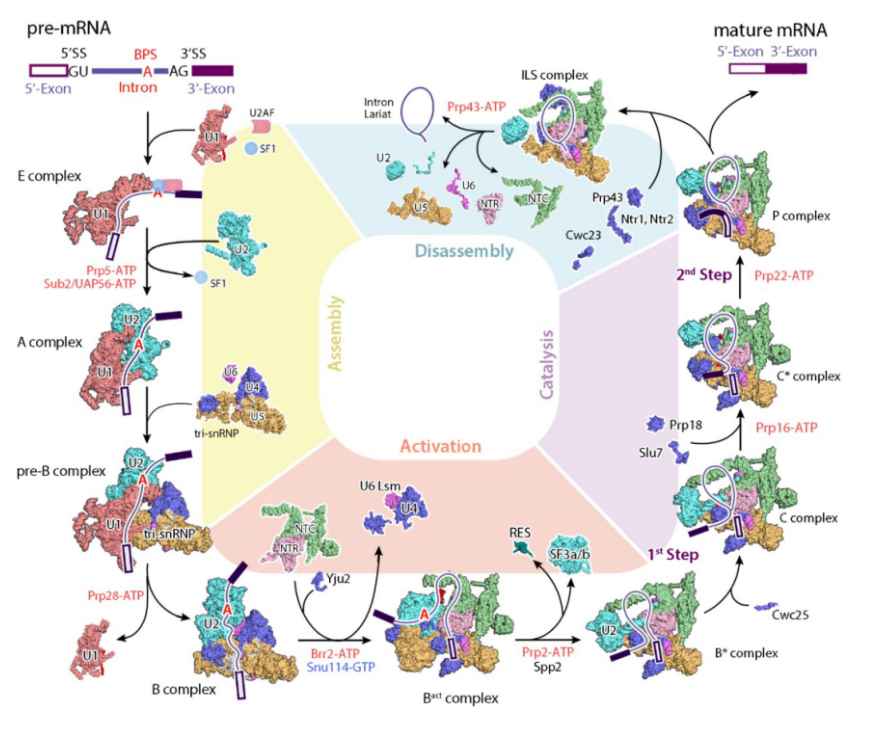
施一公研究组解析的剪接体结构汇总
图片来源: Annu Rev Biochem
本次 Molecular Cell 的研究进一步补足了高度动态的 C 复合物到 undefined 复合物的转换中间体结构,体外重建了外显子连接前的「分子编排」(molecular choreography ),但 RNA 解旋酶 PRP16 和 PRP22 的构象和组成变化仍需进一步探索。此外,FAM192A 在 RNA 剪接过程中的具体功能也仍需确认。