【资源】蛋白组学----ITRAQ技术简述
丁香园论坛
1824
蛋白组学----ITRAQ技术简述
1994年,Marc Wilkins在Siena双向凝胶电泳(two-dimensional electrophoresis,2-DE)会议上最早提出了蛋白质组(proteome)概念,并于1995年7月的Electrophoresis杂志上发表。随着高通量、高灵敏度、高分辨率生物质谱技术的出现,蛋白质组学技术取得飞速发展,人们不再满足于对一个细胞或组织的蛋白质进行定性研究,而是着眼于蛋白质量的研究,于是蛋白质组学概念就被提出,并得到了广泛的应用。
蛋白质组学(Proteomics)是蛋白质(protein)与基因组学(genomics)两个词的组合体,表示“一种基因组所表达的全套蛋白质”,即包括一种细胞乃至一种生物所表达的全部蛋白质。蛋白质组学研究,就是要把一个基因组表达的绝大多数蛋白质或一个复杂的混合体系中绝大多数蛋白质进行精确的定量和鉴定。
蛋白质组本质上指的是在大规模水平上研究蛋白质的特征,包括蛋白质的表达水平,翻译后的修饰,蛋白与蛋白相互作用等,由此获得蛋白质水平上的关于疾病发生,细胞代谢等过程的整体而全面的认识。蛋白质组学是一门以全面的蛋白质性质研究为基础,在蛋白质水平对疾病机理、细胞模式、功能联系等方面进行探索的科学。目前最新的iTRAQ蛋白定量分析技术在此基础上被提出,并被得到广泛应用。
仅仅知道蛋白质的身份并不足以对蛋白质给出最终定论,因为蛋白质的浓度对于实现其在细胞中的功能来说极其重要,一种特殊蛋白质在浓度上的变化,就能预示细胞的突变过程。因此,科学家能够对蛋白质的相对和绝对浓度进行测量,是很重要的事情。过去,科学家通常先进行二维(2D)凝较电泳,切断条带,再用质谱方法测量条带中的蛋白质。可是,这种方法不是很理想:既不是非常敏感,也不是非常精确。
新泽西医学及牙科大学的蛋白组学研究中心主任Hong Li说:“当我们开始蛋白组学研究时,就采用2D凝胶技术,但得出的信息量却让大伙很失望,因为许多蛋白质已经改变了自身的代谢过程,如热休克蛋白或者是管家蛋白。”
蛋白组学中的方法一直在不断提高。基于高度敏感性和精确性的串联质谱方法,不需要凝胶,就可以获得相对和绝对定量的蛋白质结果。iTRAQ和iCAT是这些新进展中的两大主力,但是,新技术也有不尽如人意的地方,需要不断改进。
iTRAQ技术是由美国应用生物系统公司(Applied Biosystems Incorporation,ABI)2004年开发的同位素标记相对和绝对定量(isobaric tags for relative and absolute quantitation,iTRAQ)技术,是一种新的、功能强大的可同时对四种样品进行绝对和相对定量研究的方法,这种方法是建立在iTRAQ试剂的基础上。
上海舜田生物公司目前所采用的就是这种iTRAQ技术。该技术的主要特点在于:1.分离能力强、分析范围广;2.定性分析结果可靠,可以同时给出每一个组分的分子量和丰富的结构信息;3.MS具备高灵敏度、检测限低;4.分析时间快,分离效果好;5.自动化程度高;6.iTRAQ技术不仅可发现胞浆蛋白,还有膜蛋白、核蛋白、胞外蛋白。iTRAQ技术可检测出低丰度蛋白、强碱性蛋白、小于10KD或大于200KD的蛋白。
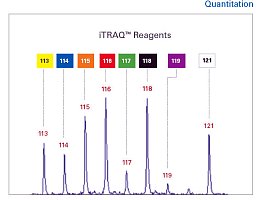
上海舜田生物使用的液相色谱仪是型号是日本岛津公司2D-nano-HPLC,质谱仪型号是美国ABI公司的MALDI-TOF-TOF 4700,标记试剂盒是美国ABI公司的ITRAQ标记试剂盒。舜田生物所采用的iTRAQ试剂是一种小分子同重元素化学物质,包括三部分:一端是报告部分(reporter group ),另一端是肽反应部分(peptide reactive group),中间部分是平衡部分(balance group)。其中,reporter group:质量为114Da、115 Da、116 Da、117 Da,因此iTRAQ试剂共四种。peptide reactive group:将reporter group与肽N端及赖氨酸侧链连接,几乎可以标记样本中所有蛋白质。balance group:质量为31 Da、30 Da、29 Da、28 Da,使得四种iTRAQ试剂分子量均为145 Da,保证iTRAQ标记的同一肽段m/z相同。
舜田生物公司iTRAQ的操作程序如下:
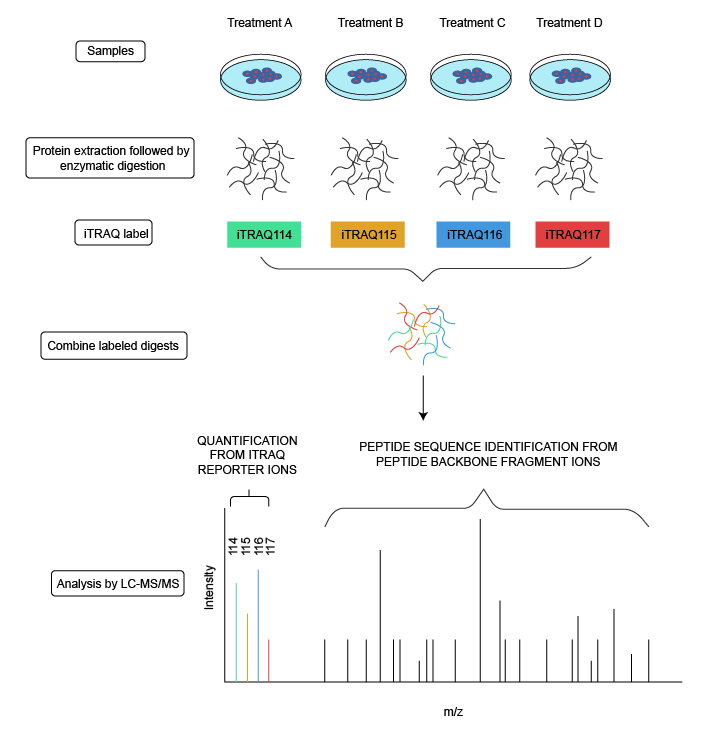
将蛋白质裂解为肽段,然后用iTRAQ试剂进行差异标记。再将标记的样本相混合,这样就可以对其进行比较。与样本结合后,通常用MudPIT多维蛋白质鉴定技术进行下一步的操作,用2D液相色谱串联质谱进行分析。在质谱分析鉴定特殊肽离子片断结构的基础上,采用美国应用生物系统公司的软件包MASCOT和Protein Pilot对每一个肽段进行鉴定。其具体操作如下图所示:
iTRAQ技术对检测标本也有一定要求。舜田生物要求检测蛋白量最低不少于50ug,浓度最低不少于5ug/uL,否则同位素无法标记。而对蛋白提取试剂也要求使用普通的组织、细胞裂解液即可,切忌不要使用二维电泳试剂提取。
iTRAQ技术区别与以往二维电泳技术具有更明显的优势,两者比较如下:
1、二维电泳所检测的发生表达变化的蛋白都位于细胞浆内,而iTRAQ可检测到蛋白有胞浆蛋白外,还有线粒体蛋白、膜蛋白和核蛋白。
2、二维电泳观察到的蛋白变化在2倍以上,而用iTRAQ计算出的蛋白变化在1.3-1.6倍之间。
3、iTRAQ技术在鉴定大分子和小分子蛋白方面也有优势。
4、二维电泳是通过切断条带,再用质谱方法测量条带中的蛋白质,但该方法既不是非常敏感,也不是非常精确,获取的信息量很少。而itraq技术是基于高度敏感性和精确性的串联质谱方法,不需要凝胶,就可以获得相对和绝对定量的蛋白质结果。
5、iTRAQ可以对任何类型的蛋白质进行鉴定,包括高分子量蛋白质、酸性蛋白质和碱性蛋白质,而二维电泳对这些蛋白质都束手无策。
由此,舜田生物得出结论:iTRAQ技术比二维电泳技术能发现更多数量和种类的蛋白,但在比较胞浆蛋白及蛋白量的变化方面,二维电泳技术有一定长处,对iTRAQ的实验结果有互补作用。
1994年,Marc Wilkins在Siena双向凝胶电泳(two-dimensional electrophoresis,2-DE)会议上最早提出了蛋白质组(proteome)概念,并于1995年7月的Electrophoresis杂志上发表。随着高通量、高灵敏度、高分辨率生物质谱技术的出现,蛋白质组学技术取得飞速发展,人们不再满足于对一个细胞或组织的蛋白质进行定性研究,而是着眼于蛋白质量的研究,于是蛋白质组学概念就被提出,并得到了广泛的应用。
蛋白质组学(Proteomics)是蛋白质(protein)与基因组学(genomics)两个词的组合体,表示“一种基因组所表达的全套蛋白质”,即包括一种细胞乃至一种生物所表达的全部蛋白质。蛋白质组学研究,就是要把一个基因组表达的绝大多数蛋白质或一个复杂的混合体系中绝大多数蛋白质进行精确的定量和鉴定。
蛋白质组本质上指的是在大规模水平上研究蛋白质的特征,包括蛋白质的表达水平,翻译后的修饰,蛋白与蛋白相互作用等,由此获得蛋白质水平上的关于疾病发生,细胞代谢等过程的整体而全面的认识。蛋白质组学是一门以全面的蛋白质性质研究为基础,在蛋白质水平对疾病机理、细胞模式、功能联系等方面进行探索的科学。目前最新的iTRAQ蛋白定量分析技术在此基础上被提出,并被得到广泛应用。
仅仅知道蛋白质的身份并不足以对蛋白质给出最终定论,因为蛋白质的浓度对于实现其在细胞中的功能来说极其重要,一种特殊蛋白质在浓度上的变化,就能预示细胞的突变过程。因此,科学家能够对蛋白质的相对和绝对浓度进行测量,是很重要的事情。过去,科学家通常先进行二维(2D)凝较电泳,切断条带,再用质谱方法测量条带中的蛋白质。可是,这种方法不是很理想:既不是非常敏感,也不是非常精确。
新泽西医学及牙科大学的蛋白组学研究中心主任Hong Li说:“当我们开始蛋白组学研究时,就采用2D凝胶技术,但得出的信息量却让大伙很失望,因为许多蛋白质已经改变了自身的代谢过程,如热休克蛋白或者是管家蛋白。”
蛋白组学中的方法一直在不断提高。基于高度敏感性和精确性的串联质谱方法,不需要凝胶,就可以获得相对和绝对定量的蛋白质结果。iTRAQ和iCAT是这些新进展中的两大主力,但是,新技术也有不尽如人意的地方,需要不断改进。
iTRAQ技术是由美国应用生物系统公司(Applied Biosystems Incorporation,ABI)2004年开发的同位素标记相对和绝对定量(isobaric tags for relative and absolute quantitation,iTRAQ)技术,是一种新的、功能强大的可同时对四种样品进行绝对和相对定量研究的方法,这种方法是建立在iTRAQ试剂的基础上。
上海舜田生物公司目前所采用的就是这种iTRAQ技术。该技术的主要特点在于:1.分离能力强、分析范围广;2.定性分析结果可靠,可以同时给出每一个组分的分子量和丰富的结构信息;3.MS具备高灵敏度、检测限低;4.分析时间快,分离效果好;5.自动化程度高;6.iTRAQ技术不仅可发现胞浆蛋白,还有膜蛋白、核蛋白、胞外蛋白。iTRAQ技术可检测出低丰度蛋白、强碱性蛋白、小于10KD或大于200KD的蛋白。
上海舜田生物使用的液相色谱仪是型号是日本岛津公司2D-nano-HPLC,质谱仪型号是美国ABI公司的MALDI-TOF-TOF 4700,标记试剂盒是美国ABI公司的ITRAQ标记试剂盒。舜田生物所采用的iTRAQ试剂是一种小分子同重元素化学物质,包括三部分:一端是报告部分(reporter group ),另一端是肽反应部分(peptide reactive group),中间部分是平衡部分(balance group)。其中,reporter group:质量为114Da、115 Da、116 Da、117 Da,因此iTRAQ试剂共四种。peptide reactive group:将reporter group与肽N端及赖氨酸侧链连接,几乎可以标记样本中所有蛋白质。balance group:质量为31 Da、30 Da、29 Da、28 Da,使得四种iTRAQ试剂分子量均为145 Da,保证iTRAQ标记的同一肽段m/z相同。
舜田生物公司iTRAQ的操作程序如下:
将蛋白质裂解为肽段,然后用iTRAQ试剂进行差异标记。再将标记的样本相混合,这样就可以对其进行比较。与样本结合后,通常用MudPIT多维蛋白质鉴定技术进行下一步的操作,用2D液相色谱串联质谱进行分析。在质谱分析鉴定特殊肽离子片断结构的基础上,采用美国应用生物系统公司的软件包MASCOT和Protein Pilot对每一个肽段进行鉴定。其具体操作如下图所示:
iTRAQ技术对检测标本也有一定要求。舜田生物要求检测蛋白量最低不少于50ug,浓度最低不少于5ug/uL,否则同位素无法标记。而对蛋白提取试剂也要求使用普通的组织、细胞裂解液即可,切忌不要使用二维电泳试剂提取。
iTRAQ技术区别与以往二维电泳技术具有更明显的优势,两者比较如下:
1、二维电泳所检测的发生表达变化的蛋白都位于细胞浆内,而iTRAQ可检测到蛋白有胞浆蛋白外,还有线粒体蛋白、膜蛋白和核蛋白。
2、二维电泳观察到的蛋白变化在2倍以上,而用iTRAQ计算出的蛋白变化在1.3-1.6倍之间。
3、iTRAQ技术在鉴定大分子和小分子蛋白方面也有优势。
4、二维电泳是通过切断条带,再用质谱方法测量条带中的蛋白质,但该方法既不是非常敏感,也不是非常精确,获取的信息量很少。而itraq技术是基于高度敏感性和精确性的串联质谱方法,不需要凝胶,就可以获得相对和绝对定量的蛋白质结果。
5、iTRAQ可以对任何类型的蛋白质进行鉴定,包括高分子量蛋白质、酸性蛋白质和碱性蛋白质,而二维电泳对这些蛋白质都束手无策。
由此,舜田生物得出结论:iTRAQ技术比二维电泳技术能发现更多数量和种类的蛋白,但在比较胞浆蛋白及蛋白量的变化方面,二维电泳技术有一定长处,对iTRAQ的实验结果有互补作用。