【共享】RNA干扰:让致病基因沉默
丁香园论坛
2074
Andrew Z. Fire 生于1959年,1983年于美国麻省理工学院获生物学博士学位,现任美国斯坦福大学医学院病理与遗传学教授。
Craig C. Mello 生于1960年,1990年于美国哈佛大学获生物学博士学位,现任美国马萨诸塞大学医学院分子医学教授。
2006年10月2日,瑞典卡罗琳斯卡研究院颁发了本年度诺贝尔生理学或医学奖,美国斯坦福大学医学院的Andrew Z. Fire和马萨诸塞大学医学院的Craig C. Mello因发现一种全新的基因调控方式——RNA干扰(RNAi)而获此殊荣。
他们发现,双链RNA会使与之同源的基因沉默,并将这种作用命名为RNAi。这种生化机制在细胞的基本活动中扮演着重要角色,植物、动物和人体组织中均可见到RNAi这种特殊的基因表达控制方式。RNAi可抵抗RNA病毒感染(尤其是在植物和无脊椎动物中),并可削弱跳跃基因[(jumping gene)即转座子(transponson)]对基因组的影响。现在该技术已经被广泛用于对基因功能的研究,并可能在未来发展成为一种新的治疗方法。
细胞中的信息流:DNA→mRNA→蛋白质
众所周知,DNA是多数生物的遗传物质,DNA中所包含的遗传信息首先将被准确无误地转录为mRNA,后者再通过核糖体将特定遗传信息翻译为相应的蛋白质,这种DNA→mRNA→蛋白质的基因信息流即为分子生物学的中心法则(图1)。
人类的基因组由约3万个基因组成,但对每个细胞而言,仅部分基因是有用的,换言之,仅部分基因需要表达。DNA→mRNA的转录过程是控制基因表达的关键步骤,此外,该过程还受到多种细胞因子的调控。在从细菌到人的漫长进化过程中,各种生物的基因表达均遵循了同样的原则,这个原则也是基因技术的根本,人们根据这项原理,将特定DNA导入细胞,以使细胞表达相应的产物。
上世纪90年代,部分植物学家试图向牵牛花的基因组中引入红色素基因,以使花瓣的颜色加深,结果却发现,花瓣的颜色非但没有加深,反而全部消失并变为白色。当时无人能解释这种现象的原因,直至Fire和Mello有了新的发现。为此,他们获得了今年的诺贝尔奖。
RNAi的发现
mRNA的编码链被称作“正义”链,与之互补的mRNA链则被称作“反义”链。Fire和Mello给秀丽隐杆线虫分别注射编码一种肌肉蛋白质mRNA分子的正义或反义链后,线虫的行为均未受任何影响,而当他们同时给线虫注射正义和反义mRNA时,线虫出现了奇特的颤搐运动,这种运动与完全缺乏肌肉蛋白功能基因的线虫相同,这说明什么呢?
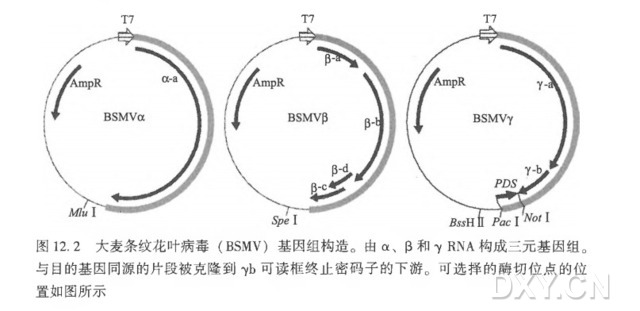
正义和反义RNA分子会结合在一起形成双链RNA分子。通过一系列简单而巧妙的实验,Fire和Mello推论,双链RNA分子确可导致基因沉默,他们将这种现象命名为RNAi。RNAi仅能使与外源RNA分子编码相匹配的基因沉默,且这种作用可在细胞间传播,甚至被遗传(图2)。
RNAi机制——基因沉默
RNAi机制已被初步阐明:双链RNA会首先结合到一种蛋白质复合体(Dicer)上,后者会将其切割成片段,此后,另外一种蛋白质复合体(RISC)会与这些片段结合。有一条RNA链会被清除,而另外一条仍与RISC复合体结合的RNA链即成为探测mRNA分子的探针。当一条mRNA分子与RISC复合体上的RNA片段通过碱基配对的形式结合时,该mRNA分子便会被剪切并降解,其对应的基因也就沉默了(图3)。
RNAi——对抗病毒和跳跃基因的防线
RNAi可有效对抗双链RNA病毒,当这种病毒感染细胞时,只要将编码它们基因组RNA序列的双链RNA分子注入细胞,病毒RNA便会被降解,从而使细胞得以存活。现已证实,植物、蠕虫和果蝇体内均存在这种抗病毒机制,但尚未在脊椎动物(包括人)体内发现这种抗病毒机制。
跳跃基因是可在基因组中移动的DNA序列,所有生物体中均有跳跃基因的存在,当它们插入特定基因序列时即会直接影响该基因表达。很多转座子首先将他们的DNA序列转录为RNA,再反转录为DNA并插入基因组的任意位置,这些RNA分子通常部分形成双链,因此可因RNAi被遏制。从这个角度讲,RNAi保护了基因组。
RNAi调控基因表达
RNAi不仅是线虫基因调控机制的重要组成部分,也是人类基因表达调控的重要因素。人类基因组中有数百种基因编码一种被称作microRNA的小RNA分子,microRNA的序列中包含其他基因的编码片段,这些microRNA分子可形成双链结构,并通过激活RNAi来阻断特定蛋白质的合成。现已证实,microRNA介导的基因调控在生物体发育和细胞功能调控过程中均发挥着重要作用。
RNAi在医学领域的应用前景
RNAi技术开辟了基因研究的新篇章,研究者可设计双链RNA分子使特定基因沉默。已有研究者用RNAi技术成功使实验动物的一种可致血胆固醇水平升高的基因沉默,另有很多利用该技术治疗病毒感染、心血管疾病、肿瘤、内分泌疾病等多种疾病的计划正在酝酿之中。
Craig C. Mello 生于1960年,1990年于美国哈佛大学获生物学博士学位,现任美国马萨诸塞大学医学院分子医学教授。
2006年10月2日,瑞典卡罗琳斯卡研究院颁发了本年度诺贝尔生理学或医学奖,美国斯坦福大学医学院的Andrew Z. Fire和马萨诸塞大学医学院的Craig C. Mello因发现一种全新的基因调控方式——RNA干扰(RNAi)而获此殊荣。
他们发现,双链RNA会使与之同源的基因沉默,并将这种作用命名为RNAi。这种生化机制在细胞的基本活动中扮演着重要角色,植物、动物和人体组织中均可见到RNAi这种特殊的基因表达控制方式。RNAi可抵抗RNA病毒感染(尤其是在植物和无脊椎动物中),并可削弱跳跃基因[(jumping gene)即转座子(transponson)]对基因组的影响。现在该技术已经被广泛用于对基因功能的研究,并可能在未来发展成为一种新的治疗方法。
细胞中的信息流:DNA→mRNA→蛋白质
众所周知,DNA是多数生物的遗传物质,DNA中所包含的遗传信息首先将被准确无误地转录为mRNA,后者再通过核糖体将特定遗传信息翻译为相应的蛋白质,这种DNA→mRNA→蛋白质的基因信息流即为分子生物学的中心法则(图1)。
人类的基因组由约3万个基因组成,但对每个细胞而言,仅部分基因是有用的,换言之,仅部分基因需要表达。DNA→mRNA的转录过程是控制基因表达的关键步骤,此外,该过程还受到多种细胞因子的调控。在从细菌到人的漫长进化过程中,各种生物的基因表达均遵循了同样的原则,这个原则也是基因技术的根本,人们根据这项原理,将特定DNA导入细胞,以使细胞表达相应的产物。
上世纪90年代,部分植物学家试图向牵牛花的基因组中引入红色素基因,以使花瓣的颜色加深,结果却发现,花瓣的颜色非但没有加深,反而全部消失并变为白色。当时无人能解释这种现象的原因,直至Fire和Mello有了新的发现。为此,他们获得了今年的诺贝尔奖。
RNAi的发现
mRNA的编码链被称作“正义”链,与之互补的mRNA链则被称作“反义”链。Fire和Mello给秀丽隐杆线虫分别注射编码一种肌肉蛋白质mRNA分子的正义或反义链后,线虫的行为均未受任何影响,而当他们同时给线虫注射正义和反义mRNA时,线虫出现了奇特的颤搐运动,这种运动与完全缺乏肌肉蛋白功能基因的线虫相同,这说明什么呢?
正义和反义RNA分子会结合在一起形成双链RNA分子。通过一系列简单而巧妙的实验,Fire和Mello推论,双链RNA分子确可导致基因沉默,他们将这种现象命名为RNAi。RNAi仅能使与外源RNA分子编码相匹配的基因沉默,且这种作用可在细胞间传播,甚至被遗传(图2)。
RNAi机制——基因沉默
RNAi机制已被初步阐明:双链RNA会首先结合到一种蛋白质复合体(Dicer)上,后者会将其切割成片段,此后,另外一种蛋白质复合体(RISC)会与这些片段结合。有一条RNA链会被清除,而另外一条仍与RISC复合体结合的RNA链即成为探测mRNA分子的探针。当一条mRNA分子与RISC复合体上的RNA片段通过碱基配对的形式结合时,该mRNA分子便会被剪切并降解,其对应的基因也就沉默了(图3)。
RNAi——对抗病毒和跳跃基因的防线
RNAi可有效对抗双链RNA病毒,当这种病毒感染细胞时,只要将编码它们基因组RNA序列的双链RNA分子注入细胞,病毒RNA便会被降解,从而使细胞得以存活。现已证实,植物、蠕虫和果蝇体内均存在这种抗病毒机制,但尚未在脊椎动物(包括人)体内发现这种抗病毒机制。
跳跃基因是可在基因组中移动的DNA序列,所有生物体中均有跳跃基因的存在,当它们插入特定基因序列时即会直接影响该基因表达。很多转座子首先将他们的DNA序列转录为RNA,再反转录为DNA并插入基因组的任意位置,这些RNA分子通常部分形成双链,因此可因RNAi被遏制。从这个角度讲,RNAi保护了基因组。
RNAi调控基因表达
RNAi不仅是线虫基因调控机制的重要组成部分,也是人类基因表达调控的重要因素。人类基因组中有数百种基因编码一种被称作microRNA的小RNA分子,microRNA的序列中包含其他基因的编码片段,这些microRNA分子可形成双链结构,并通过激活RNAi来阻断特定蛋白质的合成。现已证实,microRNA介导的基因调控在生物体发育和细胞功能调控过程中均发挥着重要作用。
RNAi在医学领域的应用前景
RNAi技术开辟了基因研究的新篇章,研究者可设计双链RNA分子使特定基因沉默。已有研究者用RNAi技术成功使实验动物的一种可致血胆固醇水平升高的基因沉默,另有很多利用该技术治疗病毒感染、心血管疾病、肿瘤、内分泌疾病等多种疾病的计划正在酝酿之中。