离子交换层析
互联网
简介
离子交换层析(Ion Exchange Chromatography简称为IEC)是以离子交换剂为固定相,依据流动相中的组分离子与交换剂上的平衡离子进行可逆交换时的结合力大小的差别而进行分离的一种层析方法。1848年,Thompson等人在研究土壤碱性物质交换过程中发现离子交换现象。本世纪40年代,出现了具有稳定交换特性的聚苯乙烯离子交换树脂。50年代,离子交换层析进入生物化学领域,应用于氨基酸的分析。目前离子交换层析仍是生物化学领域中常用的一种层析方法,广泛的应用于各种生化物质如氨基酸、蛋白、糖类、核苷酸等的分离纯化。
基本原理
离子交换层析是依据各种离子或离子化合物与离子交换剂的结合力不同而进行分离纯化的。离子交换层析的固定相是离子交换剂,它是由一类不溶于水的惰性高分子聚合物基质通过一定的化学反应共价结合上某种电荷基团形成的。离子交换剂可以分为三部分:高分子聚合物基质、电荷基团和平衡离子。电荷基团与高分子聚合物共价结合,形成一个带电的可进行离子交换的基团。平衡离子是结合于电荷基团上的相反离子,它能与溶液中其它的离子基团发生可逆的交换反应。平衡离子带正电的离子交换剂能与带正电的离子基团发生交换作用,称为阳离子交换剂;平衡离子带负电的离子交换剂与带负电的离子基团发生交换作用,称为阴离子交换剂。
其中R代表离子交换剂的高分子聚合物基质,X- 和X+ 分别代表阳离子交换剂和阴离子交换剂中与高分子聚合物共价结合的电荷基团,Y+ 和Y- 分别代表阳离子交换剂和阴离子交换剂的平衡离子,A+ 和A- 分别代表溶液中的离子基团。
从上面的反应式中可以看出,如果A离子与离子交换剂的结合力强于Y离子,或者提高A离子的浓度,或者通过改变其它一些条件,可以使A离子将Y离子从离子交换剂上置换出来。也就是说,在一定条件下,溶液中的某种离子基团可以把平衡离子置换出来,并通过电荷基团结合到固定相上,而平衡离子则进入流动相,这就是离子交换层析的基本置换反应。通过在不同条件下的多次置换反应,就可以对溶液中不同的离子基团进行分离。下面以阴离子交换剂为例简单介绍离子交换层析的基本分离过程。
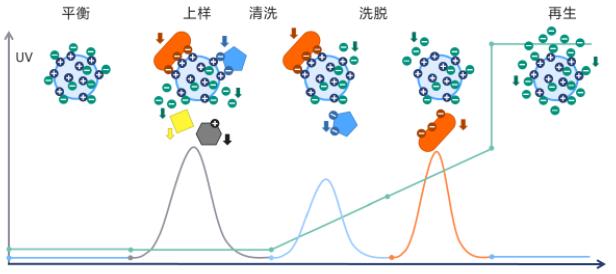
阴离子交换剂的电荷基团带正电,装柱平衡后,与缓冲溶液中的带负电的平衡离子结合。待分离溶液中可能有正电基团、负电基团和中性基团。加样后,负电基团可以与平衡离子进行可逆的置换反应,而结合到离子交换剂上。而正电基团和中性基团则不能与离子交换剂结合,随流动相流出而被去除。通过选择合适的洗脱方式和洗脱液,如增加离子强度的梯度洗脱。随着洗脱液离子强度的增加,洗脱液中的离子可以逐步与结合在离子交换剂上的各种负电基团进行交换,而将各种负电基团置换出来,随洗脱液流出。与离子交换剂结合力小的负电基团先被置换出来,而与离子交换剂结合力强的需要较高的离子强度才能被置换出来,这样各种负电基团就会按其与离子交换剂结合力从小到大的顺序逐步被洗脱下来,从而达到分离目的。
各种离子与离子交换剂上的电荷基团的结合是由静电力产生的,是一个可逆的过程。结合的强度与很多因素有关,包括离子交换剂的性质、离子本身的性质、离子强度、pH、温度、溶剂组成等等。离子交换层析就是利用各种离子本身与离子交换剂结合力的差异,并通过改变离子强度、pH等条件改变各种离子与离子交换剂的结合力而达到分离的目的。
离子交换剂的电荷基团对不同的离子有不同的结合力。一般来讲,离子价数越高,结合力越大;价数相同时,原子序数越高,结合力越大。如阳离子交换剂对离子的结合力顺序为:Li+ 蛋白质等生物大分子通常呈两性,它们与离子交换剂的结合与它们的性质及pH有较大关系。以用阳离子交换剂分离蛋白质为例,在一定的pH条件下,等电点pI pH的蛋白带正电,能与阳离子交换剂结合,一般pI越大的蛋白与离子交换剂结合力越强。但由于生物样品的复杂性以及其它因素影响,一般生物大分子与离子交换剂的结合情况较难估计,往往要通过实验进行摸索。
离子交换剂的种类和性质
1.离子交换剂的基质
离子交换剂的大分子聚合物基质可以由多种材料制成,聚苯乙烯离子交换剂(又称为聚苯乙烯树脂)是以苯乙烯和二乙烯苯合成的具有多孔网状结构的聚苯乙烯为基质。聚苯乙烯离子交换剂机械强度大、流速快。但它与水的亲和力较小,具有较强的疏水性,容易引起蛋白的变性。
故一般常用于分离小分子物质,如无机离子、氨基酸、核苷酸等。以纤维素(Cellulose)、球状纤维素(Sephacel)、葡聚糖(Sephadex)、琼脂糖(Sepharose)为基质的离子交换剂都与水有较强的亲和力,适合于分离蛋白质等大分子物质,葡聚糖离子交换剂一般以Sephadex G-25和G-50为基质,琼脂糖离子交换剂一般以Sepharose CL-6B为基质。关于这些离子交换剂的性质可以参阅相应的产品介绍。
2.离子交换剂的电荷基团
根据与基质共价结合的电荷基团的性质,可以将离子交换剂分为阳离子交换剂和阴离子交换剂。
阳离子交换剂的电荷基团带负电,可以交换阳离子物质。根据电荷基团的解离度不同,又可以分为强酸型、中等酸型和弱酸型三类。它们的区别在于它们电荷基团完全解离的pH范围,强酸型离子交换剂在较大的pH范围内电荷基团完全解离,而弱酸型完全解离的pH范围则较小,如羧甲基在pH小于6时就失去了交换能力。
一般结合磺酸基团(-SO3H),如磺酸甲基(简写为SM)、磺酸乙基(SE)等为强酸型离子交换剂,结合磷酸基团(-PO3H2)和亚磷酸基团(-PO2H)为中等酸型离子交换剂,结合酚羟基(-OH )或羧基(-COOH),如羧甲基(CM)为弱酸型离子交换剂。一般来讲强酸型离子交换剂对H离子的结合力比Na+离子小,弱酸型离子交换剂对H离子的结合力比Na+离子大。
阴离子交换剂的电荷基团带正电,可以交换阴离子物质。同样根据电荷基团的解离度不同,可以分为强碱型、中等碱型和弱碱型三类。一般结合季胺基团(-N(CH3)3),如季胺乙基(QAE)为强碱型离子交换剂,结合叔胺(-N(CH3)2)、仲胺(-NHCH3)、伯胺(-NH2)等为中等或弱碱型离子交换剂,如结合二乙基氨基乙基(DEAE)为弱碱型离子交换剂。一般来讲强碱型离子交换剂对OH?离子的结合力比Cl?离子小,弱酸型离子交换剂对OH?离子的结合力比Cl?离子大。
3.交换容量
交换容量是指离子交换剂能提供交换离子的量,它反映离子交换剂与溶液中离子进行交换的能力。通常所说的离子交换剂的交换容量是指离子交换剂所能提供交换离子的总量,又称为总交换容量,它只和离子交换剂本身的性质有关。在实际实验中关心的是层析柱与样品中各个待分离组分进行交换时的交换容量,它不仅与所用的离子交换剂有关,还与实验条件有很大的关系,一般又称为有效交换容量。后面提到的交换容量如未经说明都是指有效交换容量。
影响交换容量的因素很多,主要可以分为两个方面,一方面是离子交换剂颗粒大小、颗粒内孔隙大小以及所分离的样品组分的大小等的影响。这些因素主要影响离子交换剂中能与样品组分进行作用的有效表面积。样品组分与离子交换剂作用的表面积越大当然交换容量越高。一般离子交换剂的孔隙应尽量能够让样品组分进入,这样样品组分与离子交换剂作用面积大。分离小分子样品,可以选择较小孔隙的交换剂,因为小分子可以自由的进入孔隙,而小孔隙离子交换剂的表面积大于大孔隙的离子交换剂。对于较大分子样品,可以选择小颗粒交换剂,因为对于很大的分子,一般不能进入孔隙内部,交换只限于颗粒表面,而小颗粒的离子交换剂表面积大。
另一些影响因素如实验中的离子强度、pH值等主要影响样品中组分和离子交换剂的带电性质。一般pH对弱酸和弱碱型离子交换剂影响较大,如对于弱酸型离子交换剂在pH较高时,电荷基团充分解离,交换容量大,而在较低的pH时,电荷基团不易解离,交换容量小。同时pH也影响样品组分的带电性。尤其对于蛋白质等两性物质,在离子交换层析中要选择合适的pH以使样品组分能充分的与离子交换剂交换、结合。一般来说,离子强度增大,交换容量下降。实验中增大离子强度进行洗脱,就是要降低交换容量以将结合在离子交换剂上的样品组分洗脱下来。
离子交换剂的总交换容量通常以每毫克或每毫升交换剂含有可解离基团的毫克当量数(meq / mg或meq / ml)来表示。通常可以由滴定法测定。阳离子交换剂首先用HCl处理,使其平衡离子为H+。再用水洗至中性,对于强酸型离子交换剂,用NaCl充分置换出H+,再用标准浓度的NaOH滴定生成的HCl,就可以计算出离子交换剂的交换容量;对于弱酸型离子交换剂,用一定量的碱将H+充分置换出来,再用酸滴定,计算出离子交换剂消耗的碱量,就可以算出交换容量。阴离子交换剂的交换容量也可以用类似的方法测定。
对于一些常用于蛋白质分离的离子交换剂也通常用每毫克或每毫升交换剂能够吸附某种蛋白质的量来表示,一般这种表示方法对于分离蛋白质等生物大分子具有更大的参考价值。实验前可以参阅相应的产品介绍了解各种离子交换剂的交换容量。
离子交换剂的选择、处理和保存
1.离子交换剂的选择
离子交换剂的种类很多,离子交换层析要取得较好的效果首先要选择合适的离子交换剂。
首先是对离子交换剂电荷基团的选择,确定是选择阳离子交换剂还是选择阴离子交换剂。这要取决于被分离的物质在其稳定的pH下所带的电荷,如果带正电,则选择阳离子交换剂;如带负电,则选择阴离子交换剂。例如待分离的蛋白等电点为4,稳定的pH范围为6-9,由于这时蛋白带负电,故应选择阴离子交换剂进行分离。强酸或强碱型离子交换剂适用的pH范围广,常用于分离一些小分子物质或在极端pH下的分离。由于弱酸型或弱碱型离子交换剂不易使蛋白质失活,故一般分离蛋白质等大分子物质常用弱酸型或弱碱型离子交换剂。
其次是对离子交换剂基质的选择。前面已经介绍了,聚苯乙烯离子交换剂等疏水性较强的离子交换剂一般常用于分离小分子物质,如无机离子、氨基酸、核苷酸等。而纤维素、葡聚糖、琼脂糖等离子交换剂亲水性较强,适合于分离蛋白质等大分子物质。一般纤维素离子交换剂价格较低,但分辨率和稳定性都较低,适于初步分离和大量制备。葡聚糖离子交换剂的分辨率和价格适中,但受外界影响较大,体积可能随离子强度和pH变化有较大改变,影响分辨率。琼脂糖离子交换剂机械稳定性较好,分辨率也较高,但价格较贵。
另外离子交换剂颗粒大小也会影响分离的效果。离子交换剂颗粒一般呈球形,颗粒的大小通常以目数(mesh)或者颗粒直径(mm)来表示,目数越大表示直径越小。前面在介绍交换容量时提到了一些关于交换剂颗粒大小、孔隙的选择。另外离子交换层析柱的分辨率和流速也都与所用的离子交换剂颗粒大小有关。一般来说颗粒小,分辨率高,但平衡离子的平衡时间长,流速慢;颗粒大则相反。所以大颗粒的离子交换剂适合于对分辨率要求不高的大规模制备性分离,而小颗粒的离子交换剂适于需要高分辨率的分析或分离。
这里特别要提到的是,离子交换纤维素目前种类很多,其中以DEAE-纤维素(二乙基氨基纤维素)和CM-纤维素(羧甲基纤维素)最常用,它们在生物大分子物质(蛋白质,酶,核酸等)的分离方面显示很大的优越性。一是它具有开放性长链和松散的网状结构,有较大的表面积,大分子可自由通过,使它的实际交换容量要比离子交换树脂大的多;二是它具有亲水性,对蛋白质等生物大分子物质吸附的不太牢,用较温和的洗脱条件就可达到分离的目的,因此不致引起生物大分子物质的变性和失活。三是它的回收率高。所以离子交换纤维素已成为非常重要的一类离子交换剂。
2.离子交换剂的处理和保存
离子交换剂使用前一般要进行处理。干粉状的离子交换剂首先要进行膨化,将干粉在水中充分溶胀,以使离子交换剂颗粒的孔隙增大,具有交换活性的电荷基团充分暴露出来。而后用水悬浮去除杂质和细小颗粒。再用酸碱分别浸泡,每一种试剂处理后要用水洗至中性,再用另一种试剂处理,最后再用水洗至中性,这是为了进一步去除杂质,并使离子交换剂带上需要的平衡离子。市售的离子交换剂中通常阳离子交换剂为Na型(即平衡离子是Na离子),阴离子交换剂为Cl型,因为通常这样比较稳定。处理时一般阳离子交换剂最后用碱处理,阴离子交换剂最后用酸处理。常用的酸是HCl,碱是NaOH或再加一定的NaCl,这样处理后阳离子交换剂为Na型,阴离子交换剂为Cl型。使用的酸碱浓度一般小于0.5 mol / L,浸泡时间一般30 min。处理时应注意酸碱浓度不宜过高、处理时间不宜过长、温度不宜过高,以免离子交换剂被破坏。另外要注意的是离子交换剂使用前要排除气泡,否则会影响分离效果。
离子交换剂的再生是指对使用过的离子交换剂进行处理,使其恢复原来性状的过程。前面介绍的酸碱交替浸泡的处理方法就可以使离子交换剂再生。离子交换剂的转型是指离子交换剂由一种平衡离子转为另一种平衡离子的过程。如对阴离子交换剂用HCl处理可将其转为Cl型,用NaOH处理可转为OH型,用甲酸钠处理可转为甲酸型等等。对离子交换剂的处理、再生和转型的目的是一致的,都是为了使离子交换剂带上所需的平衡离子。
前面已经介绍了,离子交换层析就是通过离子交换剂上的平衡离子与样品中的组分离子进行可逆的交换而实现分离的目的,因此在离子交换层析前要注意使离子交换剂带上合适的平衡离子,使平衡离子能与样品中的组分离子进行有效的交换。如果平衡离子与离子交换剂结合力过强,会造成组分离子难以与交换剂结合而使交换容量降低。另外还要保证平衡离子不对样品组分有明显影响。因为在分离过程中,平衡离子被置换到流动相中,它不能对样品组分有污染或破坏。如在制备过程中用到的离子交换剂的平衡离子是H或OH离子,因为其它离子都会对纯水有污染。但是在分离蛋白质时,一般不能使用H或OH型离子交换剂,因为分离过程中H或OH离子被置换出来都会改变层析柱内pH值,影响分离效果,甚至引起蛋白质的变性。
离子交换剂保存时应首先处理洗净蛋白等杂质,并加入适当的防腐剂,一般加入0.02 %的叠氮钠,4℃下保存。
离子交换层析的基本操作
离子交换层析的基本装置及操作步骤与前面介绍的柱层析类似,这里就不再重复了。下面主要介绍离子交换层析操作中应注意的一些具体问题。
1.层析柱
离子交换层析要根据分离的样品量选择合适的层析柱,离子交换用的层析柱一般粗而短,不宜过长。直径和柱长比一般为1:10到1:50之间,层析柱安装要垂直。装柱时要均匀平整,不能有气泡。
2.平衡缓冲液
离子交换层析的基本反应过程就是离子交换剂平衡离子与待分离物质、缓冲液中离子间的交换,所以在离子交换层析中平衡缓冲液和洗脱缓冲液的离子强度和pH的选择对于分离效果有很大的影响。
平衡缓冲液是指装柱后及上样后用于平衡离子交换柱的缓冲液。平衡缓冲液的离子强度和pH的选择首先要保证各个待分离物质如蛋白质的稳定。其次是要使各个待分离物质与离子交换剂有适当的结合,并尽量使待分离样品和杂质与离子交换剂的结合有较大的差别。一般是使待分离样品与离子交换剂有较稳定的结合。而尽量使杂质不与离子交换剂结合或结合不稳定。在一些情况下(如污水处理)可以使杂质与离子交换剂有牢固的结合,而样品与离子交换剂结合不稳定,也可以达到分离的目的。另外注意平衡缓冲液中不能有与离子交换剂结合力强的离子,否则会大大降低交换容量,影响分离效果。选择合适的平衡缓冲液,直接就可以去除大量的杂质。并使得后面的洗脱有很好的效果。如果平衡缓冲液选择不合适,可能会对后面的洗脱带来困难,无法得到好的分离效果。
3.上样
离子交换层析的上样时应注意样品液的离子强度和pH值,上样量也不宜过大,一般为柱床体积的1-5%为宜,以使样品能吸附在层析柱的上层,得到较好的分离效果。
4.洗脱缓冲液
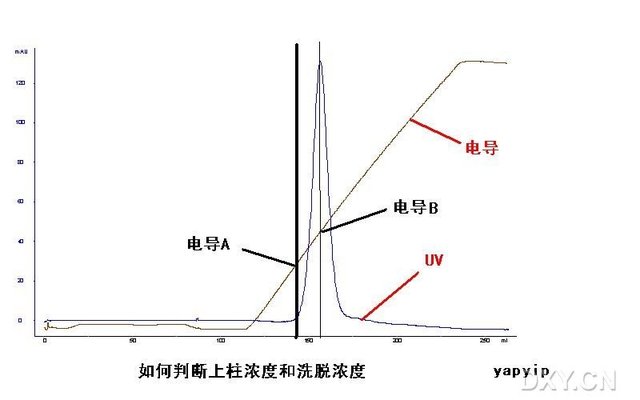
在离子交换层析中一般常用梯度洗脱,通常有改变离子强度和改变pH两种方式。改变离子强度通常是在洗脱过程中逐步增大离子强度,从而使与离子交换剂结合的各个组分被洗脱下来;而改变pH的洗脱,对于阳离子交换剂一般是pH从低到高洗脱,阴离子交换剂一般是pH从高到低。由于pH可能对蛋白的稳定性有较大的影响,故一般通常采用改变离子强度的梯度洗脱。梯度洗脱的装置前面已经介绍了,可以有线性梯度、凹形梯度、凸形梯度以及分级梯度等洗脱方式。一般线性梯度洗脱分离效果较好,故通常采用线性梯度进行洗脱。
洗脱液的选择首先也是要保证在整个洗脱液梯度范围内,所有待分离组分都是稳定的。其次是要使结合在离子交换剂上的所有待分离组分在洗脱液梯度范围内都能够被洗脱下来。另外可以使梯度范围尽量小一些,以提高分辨率。
5.洗脱速度
洗脱液的流速也会影响离子交换层析分离效果,洗脱速度通常要保持恒定。一般来说洗脱速度慢比快的分辨率要好,但洗脱速度过慢会造成分离时间长、样品扩散、谱峰变宽、分辨率降低等副作用,所以要根据实际情况选择合适的洗脱速度。如果洗脱峰相对集中某个区域造成重叠,则应适当缩小梯度范围或降低洗脱速度来提高分辨率;如果分辨率较好,但洗脱峰过宽,则可适当提高洗脱速度。
6.样品的浓缩、脱盐
离子交换层析得到的样品往往盐浓度较高,而且体积较大,样品浓度较低。所以一般离子交换层析得到的样品要进行浓缩、脱盐处理。
离子交换层析的应用
离子交换层析的应用范围很广,主要有以下几个方面。
1.水处理
离子交换层析是一种简单而有效的去除水中的杂质及各种离子的方法,聚苯乙烯树脂广泛的应用于高纯水的制备、硬水软化以及污水处理等方面。纯水的制备可以用蒸馏的方法,但要消耗大量的能源,而且制备量小、速度慢,也得不到高纯度。用离子交换层析方法可以大量、快速制备高纯水。一般是将水依次通过H+ 型强阳离子交换剂,去除各种阳离子及与阳离子交换剂吸附的杂质;再通过OH- 型强阴离子交换剂,去除各种阴离子及与阴离子交换剂吸附的杂质,即可得到纯水。再通过弱型阳离子和阴离子交换剂进一步纯化,就可以得到纯度较高的纯水。离子交换剂使用一段时间后可以通过再生处理重复使用。
2.分离纯化小分子物质
离子交换层析也广泛的应用于无机离子、有机酸、核苷酸、氨基酸、抗生素等小分子物质的分离纯化。例如对氨基酸的分析,使用强酸性阳离子聚苯乙烯树脂,将氨基酸混合液在pH 2~3上柱。这时氨基酸都结合在树脂上,再逐步提高洗脱液的的离子强度和pH,这样各种氨基酸将以不同的速度被洗脱下来,可以进行分离鉴定。目前已有全部自动的氨基酸分析仪。
3.分离纯化生物大分子物质
离子交换层析是依据物质的带电性质的不同来进行分离纯化的,是分离纯化蛋白质等生物大分子的一种重要手段。由于生物样品中蛋白的复杂性,一般很难只经过一次离子交换层析就达到高纯度,往往要与其它分离方法配合使用。使用离子交换层析分离样品要充分利用其按带电性质来分离的特性,只要选择合适的条件,通过离子交换层析可以得到较满意的分离效果。