免疫分析中,遭遇HAMA等干扰问题如何破?
青木生物技术(武汉)有限公司
4171
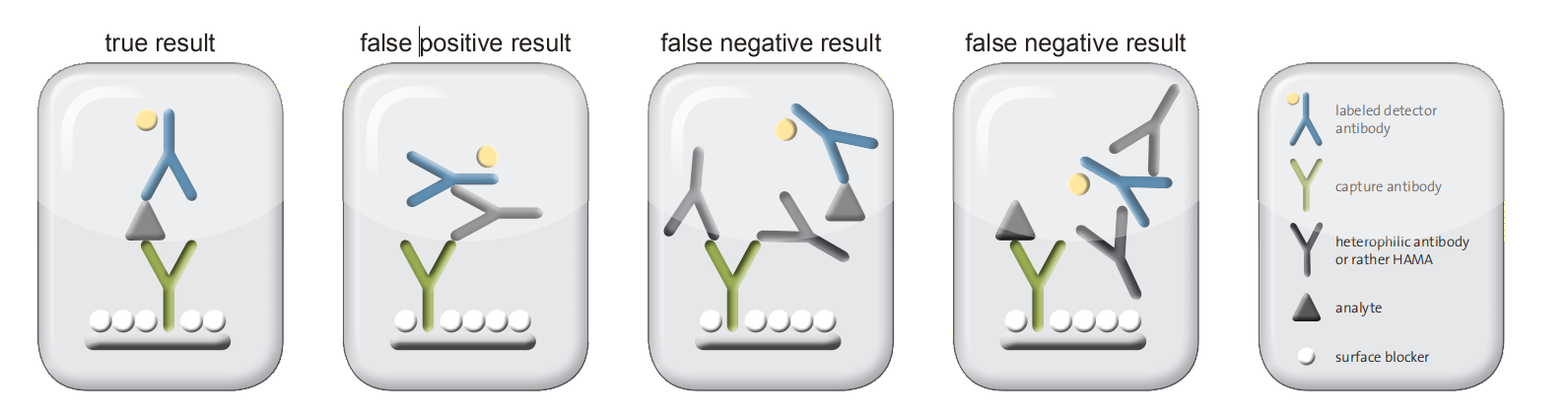
免疫分析中出现问题的一个常见原因是干扰性抗体,如众所周知的人抗鼠抗体(Human anti-mouse Antibodies,HAMA)、一般的抗动物抗体、嗜异性抗体(Id)或类风湿因子(rheumatoid factors,RF)。有趣的是,由于今天的治疗性单克隆抗体药物几乎完全是人源化的,所以真正的HAMA的流行率正在稳步下降。然而,随着近年来类风湿和过敏性疾病等发病率的上升,抗体引起的干扰在未来仍将具有高度的临床相关性,并且似乎进一步增加患病率。一般来说,这些抗体干扰主要发生在夹心法的免疫分析中,即基于捕获抗体和检测抗体(Fig.1)。干扰性抗体可以交联捕获抗体和检测抗体,导致分析中的高读数,从而导致假阳性结果。或者,它们可以阻止抗原与检测抗体的结合,甚至引起检测抗体的聚集,导致假阴性结果。
SARS-CoV-2抗体检测通常使用Antigen-down模式(即间接法)联合抗人检测抗体进行分析,因此不受影响。相比之下,SARS-CoV-2抗原的免疫分析通常使用夹心法模式,容易受到干扰性抗体的影响。
判定干扰性抗体是否是导致错误结果的原因,可以使用市面上商业化的ELISA试剂盒进行检测,这些试剂盒设计用于鉴别嗜异性抗体、HAMA和RF(通常简称为HAMA-ELISA)。鉴定后,常使用HAMA阻断剂来解决干扰问题。该解决方案的缺点是更多的生物活性成分-抗体-被添加到分析中,这可能会导致新的干扰。一般情况,多数生产商会提供几种不同的HAMA阻断剂,因为没有特定的阻断剂可以适用于所有的分析。每次检测时,HAMA阻断剂的最有效浓度也必须仔细滴定。对于给定的分析和干扰样品组合,必须进行非常严格的测试,才能找到合适的HAMA阻断剂。
此外,尽管干扰性抗体在相关文献中占主导地位,但在免疫分析中通常也会观察到许多其他类型的与抗体无关的干扰。除抗体干扰外,干扰也可能由样品中的内源性物质引起,例如由于分析物被封闭、交叉反应或一般基质效应,如高脂和高盐浓度、高粘度,这些类型的干扰在SARS-CoV-2免疫分析中也密切相关。许多内源性物质,如白蛋白、补体因子、溶血酶、α-1抗胰蛋白酶或纤维蛋白原等高度丰富的血清蛋白都会干扰免疫分析。此外,标记检测抗体或示踪剂分析物是免疫分析中的常见做法。标签可以是酶(如碱性磷酸酶(AP)或辣根过氧化物酶(HRP))、荧光染料、放射性同位素、亲和力标签,如生物素,或者DNA(immuno-PCR中采用)。这些标签也会改变标记对象的属性,并带来新的干扰。
亲和力鉴别法消除干扰
以上提到的这些干扰有一个共同点:它们是由中低亲和力结合问题引起的。相反,一个好的抗体与其表位之间的特异性相互作用具有很高的亲和力。然而,即使足够数量的低亲和力结合也会导致高分析读数,产生特定的假阳性结果,或者高背景和坏的信噪比。一种潜在的方法是使用高浓度的分析稀释剂来减少这些有问题的中低亲和力相互作用的影响。然而,这些高浓度的条件也会对高亲和力结合产生负面影响,从而影响分析的正确信号。因此,高浓度缓冲液不是一个有用的选择。
减少低亲和力和中亲和力结合作用而不影响高亲和力结合的唯一方法是亲和力鉴别。15年前,CANDOR BIOSCIENCE的LowCross Buffer®产品成功引入了这种作用模式,此后消除了数百万样本中的干扰。如果用于样品和抗体稀释,这些亲和力鉴别溶液可以消除基于低或中等亲和力结合的所有干扰,同时保持特定信号。因此,它们大大减少了背景,提高了信噪比,并提高了结果的再现性(Fig.2)。与仅防止干扰性抗体干扰的HAMA阻断剂不同,LowCross Buffer®能够消除上述各种干扰。因此,这种基于亲和力鉴别的稀释剂可用于任何受到干扰的免疫分析。无需对分子基础进行耗时的更深入的研究,也无需仔细选择和滴定不同的HAMA阻断剂。在分析过程中,所有的结合反应都必须在亲和选择性条件下进行。由于许多诊断试剂盒需要长时间储存检测抗体,CANDOR还提供LowCross HRP®,它即包含了亲和力鉴别的优点,也具有维持过氧化物酶标记的检测抗体的长期稳定的功能。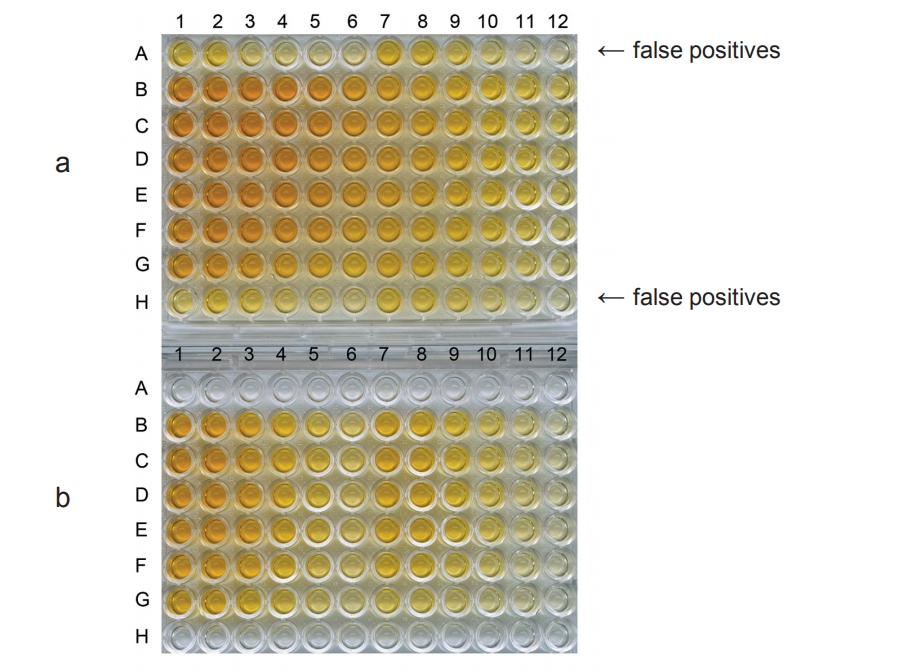
进行针对SARS-CoV-2 RBD抗体的通用的Antigen-down检测抗体分析,一种采用标准稀释液PBS-T/BSA,另一种采用CANDOR的特色产品(包括LowCross Buffer®作为实验稀释剂)的增强方案,两者进行比较,可以发现亲和力鉴别的积极效果。在阳性样品的最大信号几乎不变的情况下,阴性样品的背景和样品间的变化大大改善,从而获得了更好的检测限。减少背景和阴性样本的变化,同时改善信噪比可以防止许多假阳性结果。如上所述,在SARS-CoV-2抗体检测中,应不惜一切代价避免出现假阳性,例如来自相关冠状病毒抗体的假阳性。此外,用亲和力鉴别稀释液制备的优良抗体检测方法也有助于指导SARS-CoV-2疫苗的研制。
抗原检测通常由于粘液和唾液的复杂基质以及检测涉及完整和破碎病毒颗粒的混合物而变得复杂。此外,分析方法多样,从经典的夹心法分析到基于ACE2的双重分析都有。假阴性结果必须减少到最低限度,以防止感染者因“确认无病毒”而变得粗心。许多潜在的致命感染可以通过这种方式传播。不论样品基质效应和存在的类型如何,亲和力鉴别都能够提高分析性能,防止各种未知干扰源。因此,在开发早期,LowCross Buffer®可以防止分析开发和验证过程中的许多障碍。这不仅为开发人员节省了时间和金钱,而且析更快地将可靠的抗原分析方法提供给公众。
亲和力鉴别主要通过创建亲和力截止值来工作。相互作用中亲和力低于截止值的减少,而高亲和力结合不变。因此,当检测抗体对目标分析物有很高的亲和力时,这个概念最有效,并且可以设置较高的截止值。对于这些高亲和力抗体,CANDOR提供了LowCross Buffer®STRONG,与经典变体相比,它能防止更多不必要的相互作用。相反,某些检测模式,如自身免疫检测,必须依赖于较低亲和力的相互作用,不能使用经典LowCross Buffer®设置的截止值进行。对于这些分析,LowCross Buffer®MILD可能是有益的。尽管如此,对于大多数应用,LowCross Buffer®的经典配方可完美平衡干扰抑制和真正信号保护。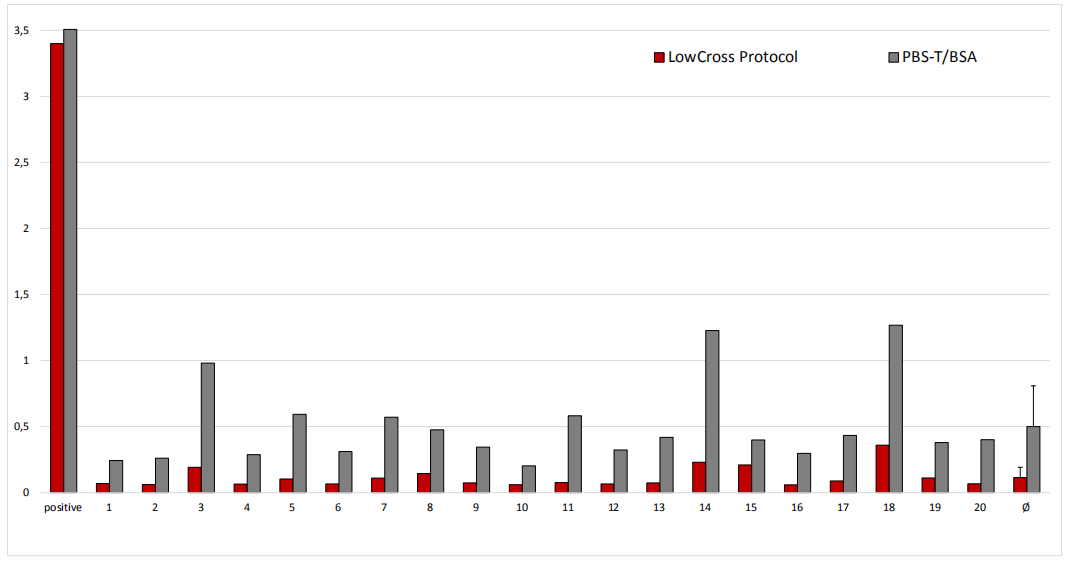 Figure 3: Improving an RBD-based SARS-CoV-2 antibody ELISA using LowCross-Buffer. Comparison of negative samples (# 1-20; Ø is arithmetic mean of 1-20) LowCross protocol vs. the standard diluent PBS/Tween/BSA (PBS-T/BSA). Samples were analyzed either using the CANDOR solutions, including LowCross-Buffer, or a standard PBS-T/BSA protocol. The LowCross protocol allows for less average background, less sample-to-sample variation, a better signal-to-noise-ratio, and a better detection limit due to a decreased cut-off. (Samples provided by in.vent Diagnostica GmbH, Henningsdorf, Germany.)
Figure 3: Improving an RBD-based SARS-CoV-2 antibody ELISA using LowCross-Buffer. Comparison of negative samples (# 1-20; Ø is arithmetic mean of 1-20) LowCross protocol vs. the standard diluent PBS/Tween/BSA (PBS-T/BSA). Samples were analyzed either using the CANDOR solutions, including LowCross-Buffer, or a standard PBS-T/BSA protocol. The LowCross protocol allows for less average background, less sample-to-sample variation, a better signal-to-noise-ratio, and a better detection limit due to a decreased cut-off. (Samples provided by in.vent Diagnostica GmbH, Henningsdorf, Germany.)
结论
亲和力鉴别缓冲液具有处理多种不同干扰的潜力,而不需要关于其分子起源的详细信息。无需额外的处理步骤,提供了分析性能和可靠性。这些改进不仅在SARS-CoV-2免疫检测的高度关键性背景下至关重要,而且在根据欧盟体外诊断法规(IVDR)验证诊断试剂盒时,也将有助于节省时间和成本,该法规将于2022年5月全面生效。每种样品只需几美分的成本,亲和力鉴别稀释剂无论是在SARS-CoV-2流行病的背景下开发的研究,还是用于人类或兽医诊断、食品测试或生物分析的其他目的,都可以极大地促进免疫分析的改进。CANDOR保持所有产品的最高质量标准,这些产品在EN ISO 9001和EN ISO 13485认证的生产设施中“德国制造”。
参考文献
1: Richter, SM et al. (2020) The challenges of serology - towards reliable SARS-CoV-2 antibody assays. www.biocompare.
com/Future-Lab/Diagnostics
2: Richter, SM (2020). Specificity, positive predictive value and validation statistics in the context of CoViD-19. Free for
download on www.candor-bioscience.de; 4-2020
3: Kroll, MH and Elin, RJ (1994) Interference with Clinical Laboratory Analyses. Clinical Chemistry
4: Klee, GG (2000) Human Anti-Mouse Antibodies. Archives of Pathology & Laboratory Medicine
5: Polifke, T and Rauch, P (2009) Affinity discrimination to avoid interference in assays. IVD Technology
6: Selby, C (1999) Interference in Immunoassays. Annals of Clinical Biochemistry
7: Wood, WG (1991) Matrix Effects in Immunoassays. Scandinavian Journal for Clinical Laboratory Investigations
8: Miller, JJ (2004) Interference in Immunoassays: Avoiding Erroneous Results. Clinical Laboratory International
相关产品
LowCross-Buffer®
LowCross® HRP-Stab

Figure 1: Interfering antibodies, like HAMA or rheumatoid factors, can result in false positives or false negatives
SARS-CoV-2抗体检测通常使用Antigen-down模式(即间接法)联合抗人检测抗体进行分析,因此不受影响。相比之下,SARS-CoV-2抗原的免疫分析通常使用夹心法模式,容易受到干扰性抗体的影响。
判定干扰性抗体是否是导致错误结果的原因,可以使用市面上商业化的ELISA试剂盒进行检测,这些试剂盒设计用于鉴别嗜异性抗体、HAMA和RF(通常简称为HAMA-ELISA)。鉴定后,常使用HAMA阻断剂来解决干扰问题。该解决方案的缺点是更多的生物活性成分-抗体-被添加到分析中,这可能会导致新的干扰。一般情况,多数生产商会提供几种不同的HAMA阻断剂,因为没有特定的阻断剂可以适用于所有的分析。每次检测时,HAMA阻断剂的最有效浓度也必须仔细滴定。对于给定的分析和干扰样品组合,必须进行非常严格的测试,才能找到合适的HAMA阻断剂。
此外,尽管干扰性抗体在相关文献中占主导地位,但在免疫分析中通常也会观察到许多其他类型的与抗体无关的干扰。除抗体干扰外,干扰也可能由样品中的内源性物质引起,例如由于分析物被封闭、交叉反应或一般基质效应,如高脂和高盐浓度、高粘度,这些类型的干扰在SARS-CoV-2免疫分析中也密切相关。许多内源性物质,如白蛋白、补体因子、溶血酶、α-1抗胰蛋白酶或纤维蛋白原等高度丰富的血清蛋白都会干扰免疫分析。此外,标记检测抗体或示踪剂分析物是免疫分析中的常见做法。标签可以是酶(如碱性磷酸酶(AP)或辣根过氧化物酶(HRP))、荧光染料、放射性同位素、亲和力标签,如生物素,或者DNA(immuno-PCR中采用)。这些标签也会改变标记对象的属性,并带来新的干扰。
亲和力鉴别法消除干扰
以上提到的这些干扰有一个共同点:它们是由中低亲和力结合问题引起的。相反,一个好的抗体与其表位之间的特异性相互作用具有很高的亲和力。然而,即使足够数量的低亲和力结合也会导致高分析读数,产生特定的假阳性结果,或者高背景和坏的信噪比。一种潜在的方法是使用高浓度的分析稀释剂来减少这些有问题的中低亲和力相互作用的影响。然而,这些高浓度的条件也会对高亲和力结合产生负面影响,从而影响分析的正确信号。因此,高浓度缓冲液不是一个有用的选择。
减少低亲和力和中亲和力结合作用而不影响高亲和力结合的唯一方法是亲和力鉴别。15年前,CANDOR BIOSCIENCE的LowCross Buffer®产品成功引入了这种作用模式,此后消除了数百万样本中的干扰。如果用于样品和抗体稀释,这些亲和力鉴别溶液可以消除基于低或中等亲和力结合的所有干扰,同时保持特定信号。因此,它们大大减少了背景,提高了信噪比,并提高了结果的再现性(Fig.2)。与仅防止干扰性抗体干扰的HAMA阻断剂不同,LowCross Buffer®能够消除上述各种干扰。因此,这种基于亲和力鉴别的稀释剂可用于任何受到干扰的免疫分析。无需对分子基础进行耗时的更深入的研究,也无需仔细选择和滴定不同的HAMA阻断剂。在分析过程中,所有的结合反应都必须在亲和选择性条件下进行。由于许多诊断试剂盒需要长时间储存检测抗体,CANDOR还提供LowCross HRP®,它即包含了亲和力鉴别的优点,也具有维持过氧化物酶标记的检测抗体的长期稳定的功能。

Figure 2: Prevention of false-positive binding using LowCross-Buffer® in an ELISA against guinea-pig IgG. With the standard assay buffer (a), false positives in the specificity control (row A) and in the blank values (row H) spoiled the interpretations and evaluation. The use of LowCross-Buffer® (b) prevented all false-positive signals. Assay performed by Dr. C. Specht (PARA Bioscience GmbH (now vivo Science GmbH), Gronau, Germany)
进行针对SARS-CoV-2 RBD抗体的通用的Antigen-down检测抗体分析,一种采用标准稀释液PBS-T/BSA,另一种采用CANDOR的特色产品(包括LowCross Buffer®作为实验稀释剂)的增强方案,两者进行比较,可以发现亲和力鉴别的积极效果。在阳性样品的最大信号几乎不变的情况下,阴性样品的背景和样品间的变化大大改善,从而获得了更好的检测限。减少背景和阴性样本的变化,同时改善信噪比可以防止许多假阳性结果。如上所述,在SARS-CoV-2抗体检测中,应不惜一切代价避免出现假阳性,例如来自相关冠状病毒抗体的假阳性。此外,用亲和力鉴别稀释液制备的优良抗体检测方法也有助于指导SARS-CoV-2疫苗的研制。
抗原检测通常由于粘液和唾液的复杂基质以及检测涉及完整和破碎病毒颗粒的混合物而变得复杂。此外,分析方法多样,从经典的夹心法分析到基于ACE2的双重分析都有。假阴性结果必须减少到最低限度,以防止感染者因“确认无病毒”而变得粗心。许多潜在的致命感染可以通过这种方式传播。不论样品基质效应和存在的类型如何,亲和力鉴别都能够提高分析性能,防止各种未知干扰源。因此,在开发早期,LowCross Buffer®可以防止分析开发和验证过程中的许多障碍。这不仅为开发人员节省了时间和金钱,而且析更快地将可靠的抗原分析方法提供给公众。
亲和力鉴别主要通过创建亲和力截止值来工作。相互作用中亲和力低于截止值的减少,而高亲和力结合不变。因此,当检测抗体对目标分析物有很高的亲和力时,这个概念最有效,并且可以设置较高的截止值。对于这些高亲和力抗体,CANDOR提供了LowCross Buffer®STRONG,与经典变体相比,它能防止更多不必要的相互作用。相反,某些检测模式,如自身免疫检测,必须依赖于较低亲和力的相互作用,不能使用经典LowCross Buffer®设置的截止值进行。对于这些分析,LowCross Buffer®MILD可能是有益的。尽管如此,对于大多数应用,LowCross Buffer®的经典配方可完美平衡干扰抑制和真正信号保护。

结论
亲和力鉴别缓冲液具有处理多种不同干扰的潜力,而不需要关于其分子起源的详细信息。无需额外的处理步骤,提供了分析性能和可靠性。这些改进不仅在SARS-CoV-2免疫检测的高度关键性背景下至关重要,而且在根据欧盟体外诊断法规(IVDR)验证诊断试剂盒时,也将有助于节省时间和成本,该法规将于2022年5月全面生效。每种样品只需几美分的成本,亲和力鉴别稀释剂无论是在SARS-CoV-2流行病的背景下开发的研究,还是用于人类或兽医诊断、食品测试或生物分析的其他目的,都可以极大地促进免疫分析的改进。CANDOR保持所有产品的最高质量标准,这些产品在EN ISO 9001和EN ISO 13485认证的生产设施中“德国制造”。
参考文献
1: Richter, SM et al. (2020) The challenges of serology - towards reliable SARS-CoV-2 antibody assays. www.biocompare.
com/Future-Lab/Diagnostics
2: Richter, SM (2020). Specificity, positive predictive value and validation statistics in the context of CoViD-19. Free for
download on www.candor-bioscience.de; 4-2020
3: Kroll, MH and Elin, RJ (1994) Interference with Clinical Laboratory Analyses. Clinical Chemistry
4: Klee, GG (2000) Human Anti-Mouse Antibodies. Archives of Pathology & Laboratory Medicine
5: Polifke, T and Rauch, P (2009) Affinity discrimination to avoid interference in assays. IVD Technology
6: Selby, C (1999) Interference in Immunoassays. Annals of Clinical Biochemistry
7: Wood, WG (1991) Matrix Effects in Immunoassays. Scandinavian Journal for Clinical Laboratory Investigations
8: Miller, JJ (2004) Interference in Immunoassays: Avoiding Erroneous Results. Clinical Laboratory International
相关产品
LowCross-Buffer®
LowCross® HRP-Stab