重大突破!李铭团队 Nature 「背靠背」开发靶向 TGF-β 的肿瘤环境免疫疗法
随着肿瘤免疫疗法的不断发展,越来越多的新药物能够直接或间接促进免疫系统靶向杀伤癌症,从而成为了癌症治疗的焦点。在该领域内,不同形式的免疫疗法(immunotherapy)—— 例如检查点抑制剂疗法(checkpoint blockers)、溶瘤病毒疗法(Oncolytic virus)和嵌合抗原受体 T - 细胞疗法 (CAR T cells)—— 在缩小或清除特定类型癌症以及延长癌症患者的寿命方面取得了前所未有的成功。
然而,大量的实际临床试验发现,仅部分非小细胞肺癌以及黑色素瘤等类别的癌症患者受益于免疫检查点疗法,更多的患者对这种疗法没有很好的应答。因此,生命科学界以及医药界都在积极探寻新的肿瘤免疫疗法。
2020 年 10 月 21 日,美国纪念斯隆凯特琳癌症研究中心(Memorial Sloan Kettering Cancer Center,MSKCC)的免疫学家李铭(Ming O. Li)教授在 Nature 杂志上「背靠背」发表两篇文章 TGF-β suppresses type 2 immunity to cancer 以及 Caner immunotherapy via targeted TGF-β signaling blockade in TH Cells。其中,前者是基础性研究,为后者的转化应用研究提供了扎实的理论基础。
在此,我们分别对两篇文章进行简要介绍,希望能够启发更多的科研临床思路。
TGF-β 抑制对肿瘤的 II 型免疫反应

众所周知,宿主免疫系统使用两种不同的防御策略来对抗感染:其一是以直接杀伤病原微生物为目的的 I 型免疫反应,以及以修复组织,从而避免或降低感染程度为目的的 II 型免疫反应。
与传染病相似,癌症逐步发展也会因癌细胞的不断自我繁殖而对宿主组织造成损害。此前研究已经充分揭示了靶向杀伤癌细胞的免疫反应机制,并以此为基础开发了许多癌症免疫疗法,但是能否诱导通过限制癌细胞存活及增殖而起到治疗目的的免疫反应目前仍知之甚少。
在这项研究中,李铭课题组揭示了通过抑制 CD4 T 细胞中转化因子生长受体 2(TGFBR2)的表达,能够促进组织愈合以及血管系统的重构,从而有效阻止癌症的进展,并进一步导致缺乏血管组织的区域内癌细胞因缺氧而死亡。
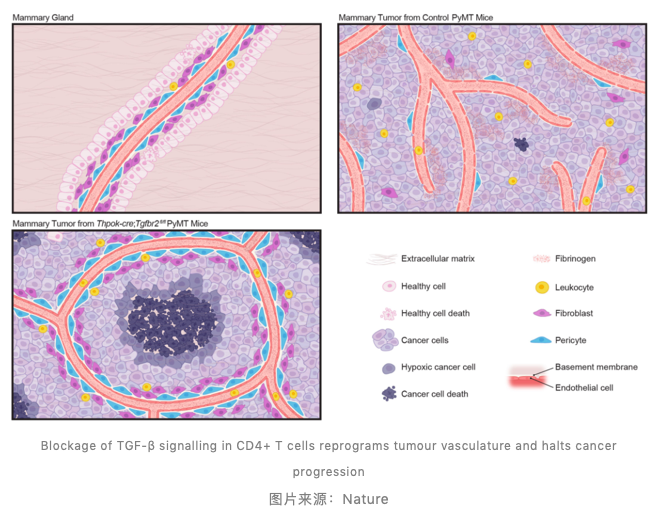
进一步,作者揭示了 Th2 细胞分泌的 IL-4 信号(而非 Th1 细胞分泌的 IFN-gamma)在这一过程中的积极作用。
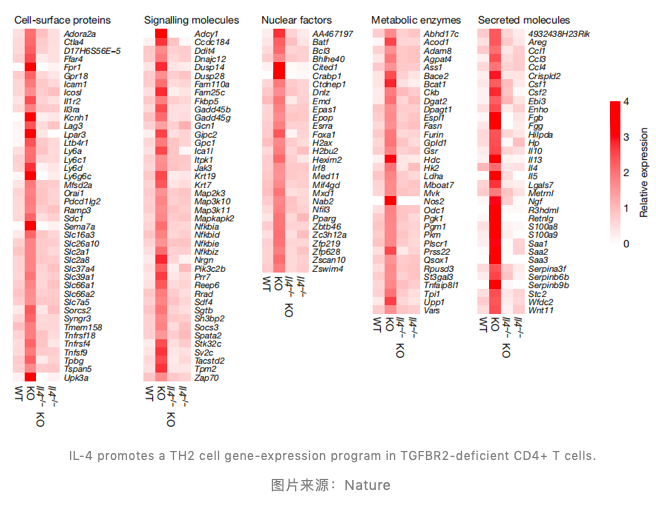
总之,这项研究表明,在激活特定免疫细胞直接杀伤肿瘤之外,可以通过调动宿主 II 型免疫反应作为治疗癌症的新策略。
靶向 Th 细胞中 TGF-β 信号通路的癌症环境免疫疗法 (Cancer Environment Immunotherapy)

癌症的形成源自于发生恶性突变的细胞与宿主多层级的相互作用。目前癌症治疗的主流方向之一在于对癌细胞造成直接杀伤,其中包括以癌基因为靶点的靶向疗法以及试图激活肿瘤相关细胞毒性 T 细胞的免疫检查点疗法。虽然上述疗法在一些患者中取得了积极的效果,但是往往同时会在部分患者中产生耐药性。
另外,还有一些疗法旨在矫正宿主的组织病理学特征,包括一些导致癌症恶化的脉管系统异常现象,其中包括对促血管生成因子(例如 VEGF-A)的中和。然而这些疗法的临床效果也十分有效。
上一篇文章中,李铭教授团队已经介绍了 Th2 介导的 II 型免疫反应对于治疗肿瘤的潜力,而这一篇文章则更为直接地测试了这一理论的可行性。
在这一研究中,作者发现 TGF- β 参与抑制了由 Th2 细胞介导的宿主对抗癌症的免疫反应。作者发现,CD4 T 细胞中 TGF-β 信号的阻断能够重新塑造肿瘤微环境并且抑制癌症的进一步恶化。
在免疫检查点疗法以及抗 VEGF-A 疗法的小鼠乳腺癌模型试验中,作者发现 CD4 T 细胞中 TGF-β 受体 II(TGFBR2)的缺陷会导致肿瘤生长受到抑制。
作者通过将 TGFBR2 胞外结构域与 CD4 抗体 ibalizumab 进行重组,得到了能够同时识别体内 TGF-β 与 CD4 的「双特异性」抗体,并将其命名为 CD4TGF-βTrap(4T-Trap)。与对照抗体相比,4T-Trap 能够选择性地抑制肿瘤引流淋巴结中的 Th 细胞内的 TGF-β 信号传导,从而导致肿瘤脉管系统重组和癌细胞死亡,这一过程依赖于 IL-4 信号传递。
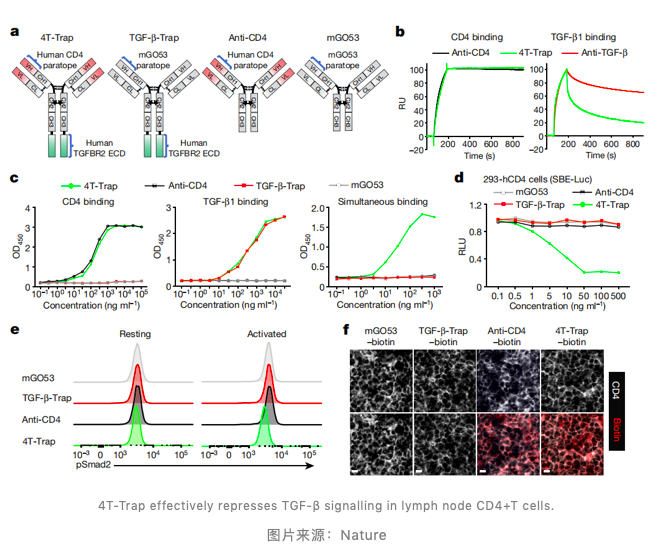
另外,作者发现 4T-Trap 诱导的肿瘤组织缺氧会导致 VEGF-A 表达量增加,而对 VEGFA 的抑制则进一步增强了由饥饿出发的癌细胞死亡的发生,最终增强了 4T-Trap 的抗肿瘤作用。
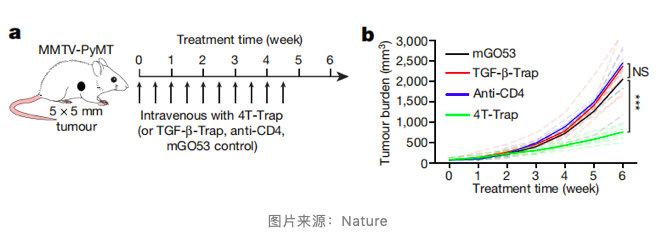
李铭教授指出,他们研究中关于肿瘤与伤口愈合的关系并非是完全首创。事实上,在 1980 年中期,癌症学家 Harold Dvorak 就在著名的 NEJM 上发表论文且指出肿瘤实质上就是「不能愈合的伤口」, 这与他们的发现不谋而合。
肿瘤通过组织损伤早期引发的炎症反应和血管新生来促进其生长,而当血管完整扩张到损伤组织时,肿瘤却永远不会进入到伤口愈合的后期。而通过阻断辅助性 T 细胞上的 TGF-β 信号通路,我们可以让肿瘤完整地完成伤口愈合过程。通过回顾前人的研究,他们的发现回应了之前的猜想,这也是一项令人激动的回归性研究。
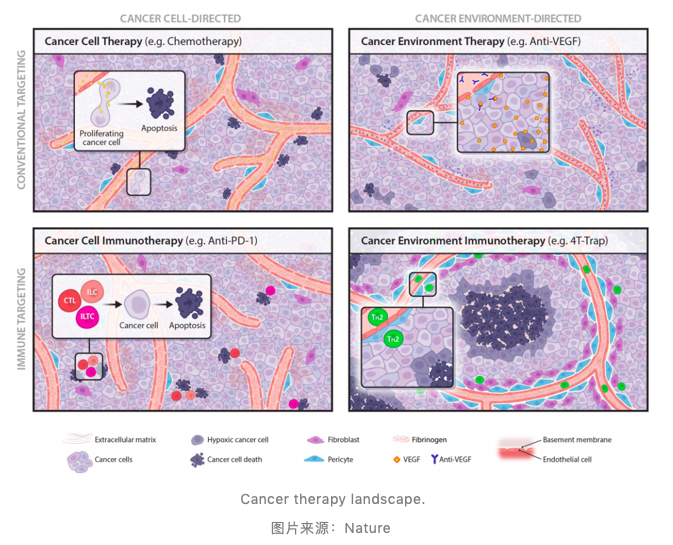
李铭教授指出,这种癌症环境免疫疗法,很可能是一类新型的癌症疗法,是对现有癌症疗法的一种重要补充。目前,他正在联合纪念斯隆凯特琳癌症中心的医生们一同将这种疗法推向临床。
总之,对辅助性 T 细胞中的 TGF-β 信号进行靶向性阻断能够引起有效的,组织水平的癌症宿主防御反应,从而能够为针对癌症微环境的疗法提供新的开发思路。









