节食减肥为啥容易体重反弹?Cell Metab 研究揭示:原因可能藏在大脑里!
丁香学术


图片来源:Cell Metabolism
主要研究内容
体重减轻对 AgRP 神经元的影响
为了表征体重减轻对 AgRP 神经元离散谷氨酸传入的可塑性变化,他们使用光遗传学检测了禁食或自由喂养小鼠的突触传递。ChR2 在 PVHTRH 或 DMHVglut2 神经元中表达,这是两个不同的神经元种群,以前发现它们为 AgRP 神经元提供单突触谷氨酸输入。先前的报道表明,禁食会引起 AgRP 神经元中自发性兴奋性突触后电流(sEPSCs)频率的增加,而不是振幅的增加。这种谷氨酸驱动的上调与突触前末端神经递质释放的增加以及突触数量的突触后适应有关。
当他们检查 PVHTRH→AgRP 神经元突触之间的传递时,他们发现禁食引起 blue-light-evoked EPSCs(le-qEPSCs)的频率增加了 2 倍,但对振幅没有影响。此外,喂食小鼠和禁食小鼠的谷氨酸释放概率没有变化,并且在 PVHTRH 输入时,突触后离子电导没有变化。因此,在谷氨酸释放概率或离子电导没有变化的情况下,le-qEPSCS 频率的增加表明禁食增加了功能突触位点的数量。
接下来,他们还确定了谷氨酸 DMHVglut2→AgRP 突触传递的改变。他们观察到 le-qEPSCs 振幅的增加,这表明与 PVHTRH→AgRP 突触不同,DMHVglut2→AgRP 突触之间的传递通过突触后离子电导的增加而增强。与此一致的是,禁食增加了 DMHVglut2 输入时 le-EPSCs 的振幅,但 PVHTRH 输入时没有。
图片来源:Cell Metabolism
PVHTRH 神经元的活动是体重反弹所必需的
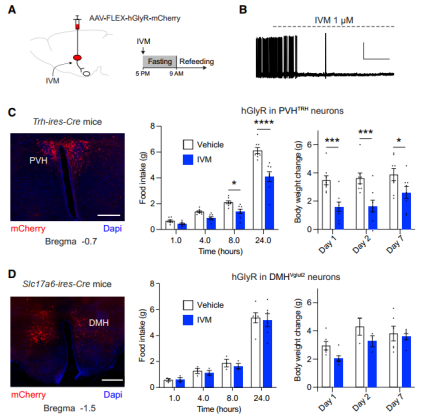
谷氨酸能 PVHTRH 和 DMHVglut2 输入的突触变化显著不同,这表明任一兴奋性输入活动的增加可能有助于 AgRP 神经元的激活,进而驱动减肥后的进食行为。为了探索这种可能性,研究人员在禁食期间沉默 PVHTRH 或 DMHVglut2 神经元。当抑制 PVHTRH 神经元时,在重新进食后的 8 小时和 24 小时时间点上,大大减少了食物摄入量的增加。与食物摄入量的减少一致,在接下来的几天里,体重反弹也减少了。
因此,PVHTRH 神经元活动对于食物摄入和长时间的体重变化特别重要。相比之下,沉默 DMHVglut2 神经元对食物摄入和体重反弹没有显著影响。
图片来源:Cell Metabolism
短暂的高频发作增强 PVHTRH→AgRP 突触并促进进食
NMDARs 的激活在介导谷氨酸能突触的活动依赖性可塑性中具有公认的作用,并与禁食诱导的 sEPSC 频率和 AgRP 神经元棘的增加以及禁食后食物摄入量的增加有关。为了探究 PVHTRH→AgRP 突触在响应电路激活时传递的增加是否需要 NMDAR 激活,研究人员采用了离体光遗传学的方法,发现对 ARC 内 PVHTRH 神经元轴突末端进行短暂 10 分钟的高频光刺激(HFpS)可增加 le-qEPSCs 的频率,但振幅不增加。这种通过 PVHTRH→AgRP 突触传递的加强可以在光刺激后数小时内被检测到。重要的是,当 NMDAR 拮抗剂 D-AP5 在刺激期间存在时,高频光刺激未能增加 le-qEPSCs 的频率。因此,电路刺激过程中 NMDAR 的激活是触发 PVHTRH→AgRP 突触传递的活动依赖增强所必需的。
为了评估活动依赖性突触强化对摄食行为的影响,他们通过植入光纤和体内光遗传学方法,对在光遗传刺激后 4 小时制备的脑切片记录进行评估,确认了简短的光刺激方案应用于体内 PVHTRH→AgRP 突触的放大传输。他们发现,在 10 分钟的光刺激后,食物摄入量随着时间的推移略有增加,并在刺激后 24 小时显著增加。当小鼠在光刺激之前接受 NMDAR 拮抗剂 MK-801 时,24 小时的食物摄入量则没有改变。因此,短回路光刺激足以引发 NMDA 依赖的长期摄食增加。
图片来源:Cell Metabolism
激活 PVHTRH→AgRP 电路后体重持续增加
上述的研究结果表明,体重减轻增加了 PVHTRH 神经元的活动,从而以活动依赖的方式增强了 PVHTRH→AgRP 突触,并增加了伴随的食物摄入量,以促进体重增加。
为了直接验证这一点,他们评估了 PVHTRH 神经元化学活化对体重发育的影响。与 24 小时食物摄入量的大幅增加一致,小鼠在注射 N-氧化氯氮平(clozapine N-oxide, CNO)1 天后体重增加了约 5%。CNO 和 MK-801 的联合使用则消除了体重的增加,证明了在电路激活过程中 NMDAR 的激活是必要的。
对食物摄入量的进一步分析显示,注射 CNO 后 1 天,仍可检测到因化学反应激活回路而增加的摄食,并在第 3 天恢复到对照水平。值得注意的是,小鼠在注射一次 CNO 后的一周内体重增加了约 10%,这表明持续的体重增加是由增加的热量摄入引起的。与此一致的是,2 周和 4 周后单次注射 CNO 也会导致体重进一步增加。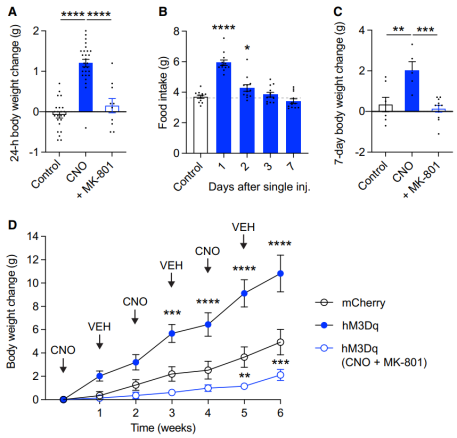
图片来源:Cell Metabolism
结语
综上所述,在该研究中,他们结合特异性电生理、光遗传学和化学遗传学方法,探索了在离散谷氨酸输入中,突触可塑性对摄食行为和体重调节的贡献。他们发现了一组关键的上游神经元——PVHTRH 神经元,能够激发控制饥饿感的 AgRP 神经元。它们之间的物理神经递质连接会随着节食和减肥大大增加,触发更强的饥饿信号,进而导致节食后摄食量增加和体重反弹。
本研究通讯作者马克斯-普朗克研究所 Henning Fenselau 教授说到:「人们主要关注节食后的短期影响,而我们则想看看大脑在长期内发生了什么变化。通过选择性抑制激活的 AgRP 神经元,会使得节食后体重增加反弹显著减少,这可能给我们制定合理的减肥方案提供了新的思路。从长远来看,我们的目标是为人类提供合理的节食方案,帮助他们在节食后仍保持体重减轻。为了实现这一目标,我们将继续探索如何阻断调节人类神经通路加强的机制。」