Science 子刊封面:浙江大学顾臻团队等开发智能调控血糖的透皮贴剂,降低低血糖发生风险
丁香学术
目前全球已有超过 5.37 亿人患有糖尿病,患者不单需要忍受长期治疗所带来的痛苦,并且还面临血糖失衡所引起的各类并发症。在健康人体内,胰岛细胞能够精准调控日常血糖水平波动。餐后血糖水平的升高会刺激胰岛 β 细胞分泌更多的胰岛素用于降低血糖。而随着血糖的下降,胰岛素的分泌速度随之减缓,并通过胰岛 α 细胞分泌的胰高血糖素促进糖原分解进一步维持血糖平衡。因此,在不同情况下动态调节胰岛素和胰高血糖素之间的平衡,对血糖管理至关重要。
尽管在过去的几十年间,人们通过模拟胰腺分泌机制,开发了多种葡萄糖响应型递送系统用于糖尿病的治疗。但实现胰岛素和胰高血糖素两者的动态释放仍面临很多挑战,如何实现血糖长期稳态控制并降低低血糖发生的风险仍是胰岛素临床使用的难点。
近日,浙江大学药学院、金华研究院团队开发了一种用于胰岛素和胰高血糖素闭路递送的葡萄糖响应性透皮微针贴剂,以同通过方便的手段实现更优的血糖调控。通过将胰岛素和胰高血糖素共混载入高分子基的微针针体中,能够模拟胰腺中葡萄糖依赖性的胰岛素和胰高血糖素的分泌行为。研究团队在小鼠和猪的动物模型上验证了该贴剂在快速降低高血糖的同时,可有效减少低血糖发生风险。
相关研究以 Glucose-Responsive Microneedle Patch for Closed-Loop Dual-Hormone Delivery in Mice and Pigs 为题发表于最新期的 Science Advances 上,并被遴选为当期的封面文章(图 1)。论文第一作者是浙江大学药学院硕士研究生杨昌伟和博士研究生盛涛,通讯作者为浙江大学顾臻教授、俞计成研究员和张宇琪研究员。

图 1 Science Advances 最新期封面:智能贴剂的微针阵列的电镜图片
葡萄糖响应性双激素微针(Glucose-Responsive Dual-Hormone Microneedle, GRD-MN)的闭路释放机制依赖于聚合物微针针体所带电荷的转变和激素分子自身所携带的电荷。葡萄糖分子与针体基质所含的苯硼酸基团之间的可逆结合作用会导致微针针体净电荷在不同血糖水平下的正负转变,利用针体与带负电的胰岛素以及带正电的胰高血糖素类似物间的静电相互作用,能够动态调节 GRD-MN 贴片中胰岛素和胰高血糖素的释放速率(图 2)(高葡萄糖时促进胰岛素释放,低葡萄糖时促进胰高血糖素释放)。GRD-MN 贴片的制备通过将同时含有胰岛素和胰高血糖素的聚合物单体混合溶液灌入微针模具并通过原位光固化方式聚合,整个过程简单快捷,有利于规模化生产。制得的微针长度为 900 微米,使用方便,疼痛度较皮下注射的传统方法显著减轻。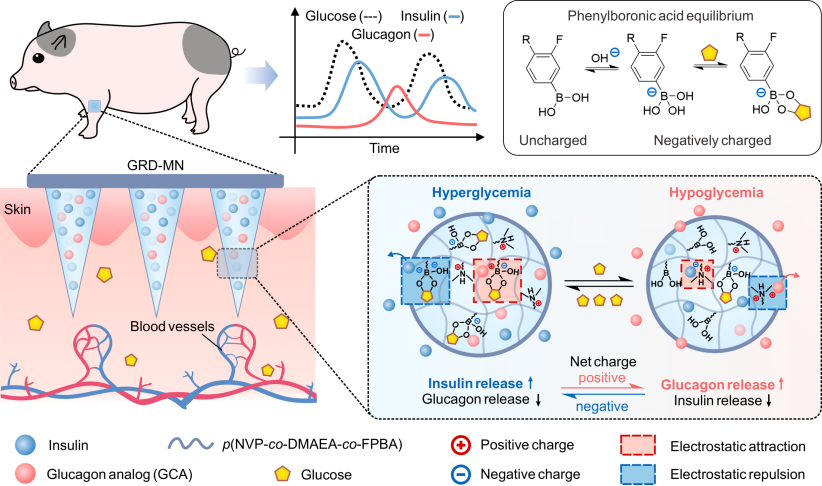
图 2 葡萄糖触发的胰岛素和胰高血糖素从双激素微针贴片中释放的机制示意图(glucose:葡萄糖;insulin:胰岛素;glucagon analog:胰高血糖素类似物)
在 1 型糖尿病小鼠模型中的研究证实,GRD-MN 贴片可以模拟胰腺功能,实现血糖的持续控制,并能有效预防胰岛素过量注射或延迟进食等极端情况下低血糖的发生。此外,在小猪模型中,该团队进一步验证了 GRD-MN 贴片在治疗糖尿病和预防低血糖等方面的有效性和安全性(图 3)。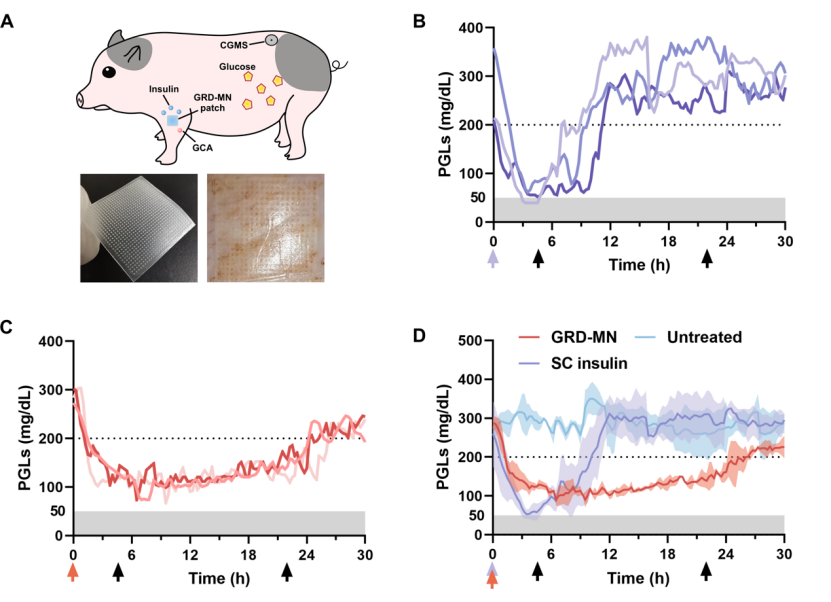
图 3 在 STZ 诱导的糖尿病小猪模型中对 GRD-MN 贴片的体内评价。A) 用 GRD-MN 在腿部治疗的小猪的示意图,用连续血糖检测仪进行监测。GRD-MN 在小猪腿上贴上之前后的照片。B-D) 不同处理的糖尿病小猪的平均血糖水平(橙色箭头、紫色箭头和黑色箭头分别表示微针贴片给药、胰岛素皮下注射和喂食的时间点)。
这种基于生理、病理信号响应性的释放体系与具有相反作用药物相结合的策略还有望应用于其他代谢失衡疾病的治疗。目前,该团队已申请了相关发明专利,并正推动临床试验的申请。







