重大突破!西湖大学蔡尚团队首次证实细菌是乳腺癌转移的「重要帮凶」
丁香学术
导读
除了众所周知的遗传、表观和微环境因素,宿主微生物群,作为机体不可忽视的组成部分,也是调节肿瘤易感性和疾病进展的重要媒介,这些微生物主要通过间接途径,包括代谢物和免疫调控等对远端或近端肿瘤组织发挥作用。
近年来,有新的研究证据表明,微生物也是肿瘤组织本身的组成部分,这在结直肠癌、胰腺癌、肺癌、乳腺癌中均得到证实,这类细菌绝大多数以较低的生物量存在于细胞质内,称之为「胞内菌」。
尽管越来越多的证据表明胞内菌的重要性,然而其生物量很低,如此低量的胞内菌是否在肿瘤发生发展中发挥重要的生物学作用仍是一个悬而未决的问题。
2022 年 4 月 8 日,西湖大学生命科学学院蔡尚课题组在 Cell 在线发表了题为 Tumor Resident Intracellular Microbiota Promotes Metastatic Colonization in Breast Cancer 的研究论文,基于经典的 MMTV-PyMT 小鼠自发乳腺癌模型(Breast Tumor, BT),他们首次证明生理状况下乳腺癌组织中独特的胞内菌在肿瘤转移定植过程中所起的关键作用。在机制层面上,他们发现胞内菌能够调节宿主细胞的肌动蛋白网络,以此增强细胞对抗循环中的流体剪切压力。
总之,该研究鉴定了肿瘤微环境中长期被忽视的新成分,并揭示了其可直接调节肿瘤转移过程中细胞的生存能力,开拓了肿瘤研究的新方向,这可能对未来的癌症治疗有很强的指导意义。
图片来源:Cell
主要研究内容
自发乳腺癌小鼠的肿瘤组织含有大量的活细菌
基于经典的 MMTV-PyMT 小鼠自发乳腺癌模型,他们对肿瘤内微生物群进行了表征。由于肿瘤内微生物群落生物量很低,他们首先在多个关键步骤中优化了检测流程,使其灵敏度大大提升。借助该方法,他们的确发现了肿瘤中细菌的存在,并且细菌密度相对稳定,不会随着肿瘤体积的增大而增多。同时,这些肿瘤内细菌也可通过各种方法进行培养。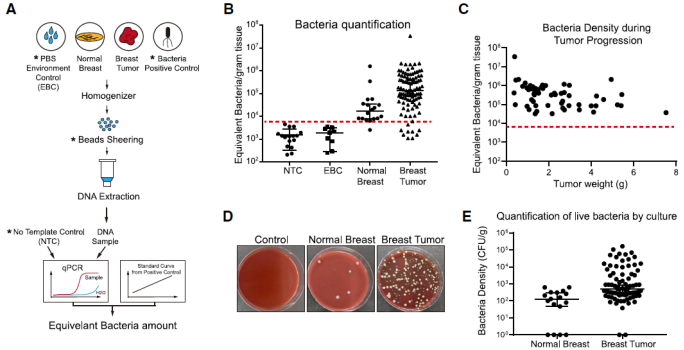
图片来源:Cell
他们进一步通过 16S rRNA 测序技术全面解析了肿瘤组织驻留菌群的组成。在排除污染后,他们发现 BT 组织与正常乳腺组织相比 alpha 多样性显著降低,表明某些微生物的选择性扩张,另外也检测到了前期实验培养分离出的菌种。
更加有趣的是,BT 组织中厌氧菌数量急剧减少,兼性厌氧菌数量显著增加,这表明肿瘤内存在动态有氧微环境。这些数据共同表明乳腺肿瘤中含有大量的活菌。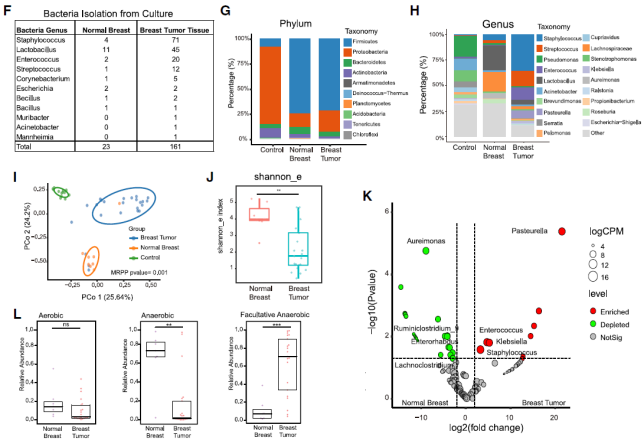
图片来源:Cell
肿瘤微生物主要存在于细胞质中
在确定了细菌存在的基础上,他们又通过 FISH 分析、革兰氏染色以及免疫荧光等方法发现细菌主要存在于核周区域。同时,高分辨率电子显微镜(EM)分析结果也表明,细菌样结构主要存在于胞浆中,而非胞外间隙中。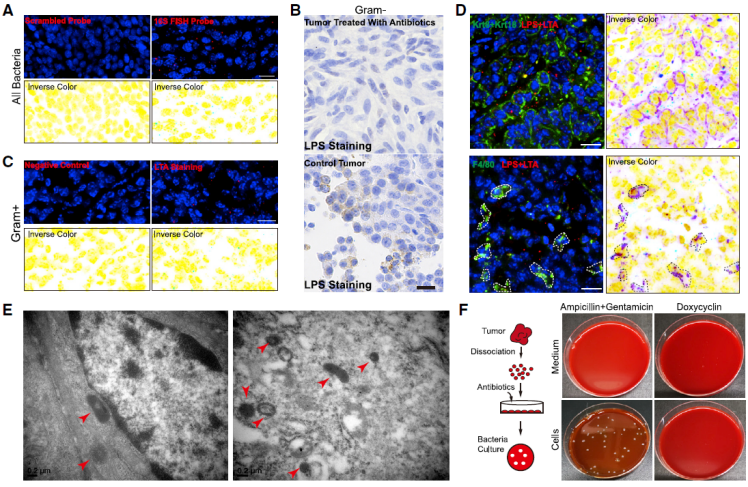
图片来源:Cell
清除肿瘤内的微生物会阻碍肿瘤的转移
虽然前期的研究表明,肠道微生物群会影响各种肿瘤的进展,但是肿瘤内微生物群的生物学意义仍在很大程度上是未知的。该团队创新性地开发了一种不同的抗生素组合和给药途径的方法来特异性清除肿瘤菌群。通过这些不同的抗生素治疗策略,他们探讨了肠道菌群和肿瘤菌群在肿瘤进展中的不同功能。结果发现,肠道菌群的确在肿瘤生长中起着重要作用,而肿瘤菌群则不然。那么肿瘤菌群的存在究竟有何意义?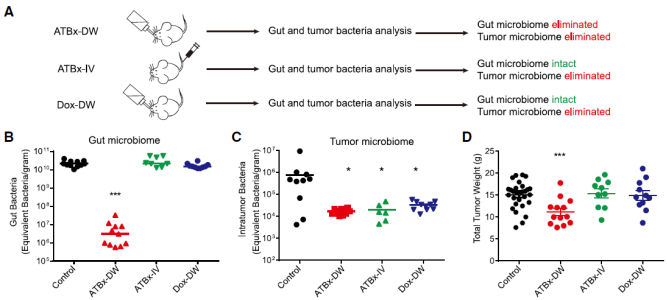
图片来源:Cell
研究人员发现,在肿瘤发展的晚期,大多数荷瘤小鼠发生了肺转移。有趣的是,原发肿瘤中的微生物群与肺转移灶的相关性较弱,而转移细胞内的细菌数量与转移灶的相关性较强,这提示细胞内的微生物群可能参与了肿瘤的转移。然后他们分析了不同抗生素治疗策略下的肺转移情况,结果发现特异性清除肿瘤菌群可使肺转移减少 3 倍以上,尽管其对原发肿瘤的生长无明显影响。
因此,这些数据共同表明,肿瘤内细菌在乳腺癌转移中是必不可少的。后续的多种模型和分析也均证实了这一结论,即肿瘤菌群虽然不影响肿瘤原位生长,但显著促进了肿瘤转移,甚至让那些很少转移的肿瘤类型也开始了大量转移。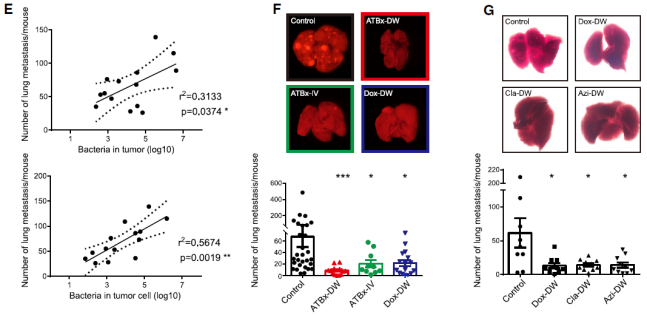
图片来源:Cell
胞内菌可增强肿瘤细胞在机械压力下的生存能力
接下来,研究人员进一步探讨了肿瘤菌群对于促进肿瘤细胞转移的机制。
利用单细胞转录组测序技术,他们发现各种细菌侵袭肿瘤细胞后并没有改变肿瘤细胞的异质性,不过信号通路分析结果显示,被细菌入侵的肿瘤细胞开启了许多与免疫相关的信号。更加有趣的是,细菌入侵肿瘤细胞之后还会使肿瘤细胞特异性触发液流剪切压力通路。
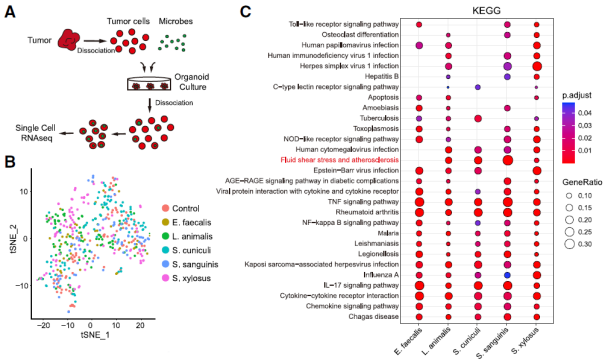
图片来源:Cell
事实上,对于转移的肿瘤细胞,其在循环系统中会经历流体剪切压力,这经常能够触发细胞凋亡,这也可能是机体的一种自发保护措施。那么上述细菌入侵的肿瘤细胞特异性上调参与流体剪切压力的通路是否意味着胞内菌可以帮助肿瘤细胞调节应激反应,并增强转移中的肿瘤细胞的生存能力呢?
为了验证这一想法,他们建立了一个体外液流压力系统来模拟血管中的流体剪切压力。在这个模拟循环系统中,在生理范围内,肿瘤细胞随着压力的增加,细胞活力逐渐下降。但是,有细菌的细胞比没有细菌的细胞显示出更高的存活率。更重要的是,有细菌的活细胞在平板上粘附和扩散的更好,而且比对照组要大得多,这表明细菌的加入使细胞骨架和附着能力发生了显著改变,而这种改变可能是细菌的存在重塑了肿瘤的细胞骨架,以使其更好地生存。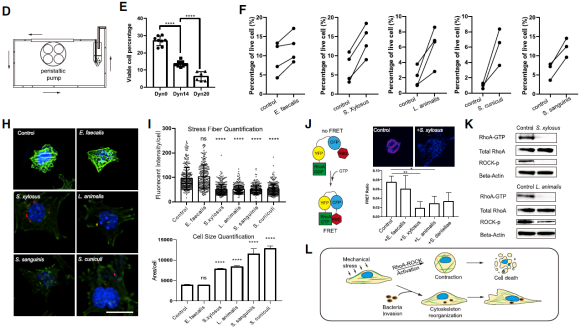
图片来源:Cell
人类乳腺癌组织中微生物群的表征
最后,他们还收集了乳腺癌病人的肿瘤组织、癌旁组织和淋巴结组织探究了原发肿瘤和转移部位之间的微生物群联系。通过 qPCR 检测,结合 16S 测序定量和定性地分析上述组织中菌群的组成。结果发现,小鼠和人类乳腺癌组织具有相似的微生物群落结构和动态变化特征,这表明人类乳腺癌组织的微生物群可能在人类癌症的发生发展中起着相似的作用。不过这部分仍然有待更加详尽的研究。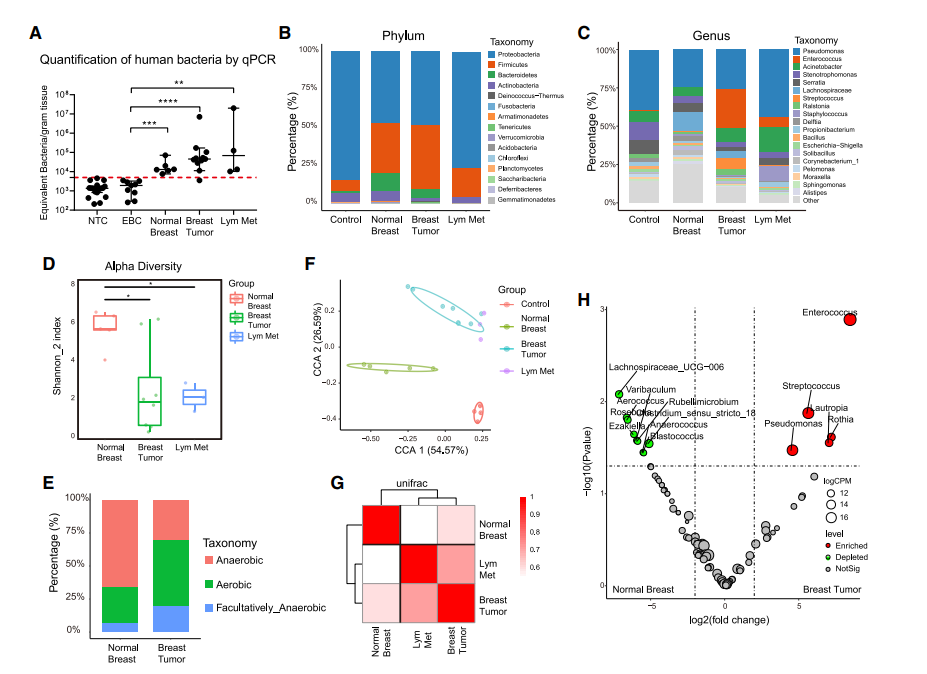
图片来源:Cell
结语
综上所述,该研究发现细胞内的微生物在肿瘤转移中起着至关重要的作用,其可在机械应激压力下调节细胞骨架和细胞活力,进而促进细胞的生存。这一关键现象被证实在人类乳腺癌患者中同样存在。这说明肿瘤内的微生物群更可能是肿瘤组织固有的、完整的组成部分,而不是由于致病性感染而偶然出现的。这不仅强调了微生物对于人体健康的重要性,而且还将开辟肿瘤微生物在肿瘤生物学和临床中的广泛研究。
在未来,需要进一步深入分析细菌如何入侵到肿瘤细胞,以及细胞内的细菌是如何整合到宿主细胞系统,同时也需要探讨包含细菌的肿瘤细胞与免疫系统之间存在怎样的相互作用,这种互作是否可以帮助实现利用抗生素助力癌症治疗的愿景。
正如本研究通讯作者蔡尚强调的那样:「这一领域刚刚兴起,还存在众多未解之谜,抗生素的临床使用也充满了复杂性,如何利用这一发现指导临床治疗仍是一个复杂而迫切的科学问题,需要更多科研工作者去做大量基础而扎实的工作。」