浙大靳津/东南柴人杰团队联合 cell 发文:阐明外周 CD4+ T 细胞代谢异常如何导致焦虑症状
恐惧,压力等情绪反应,是人们日常生活面对对积极和消极情境下正常的生理和心理活动。其中,频繁的急性情绪反应,被称为慢性应激,是一种增加抑郁和焦虑的病理状态。
现代社会生活节奏快,压力大,很多人处于慢性压力应激状态,而这种长期生理和心理上的压力应激,会增加抑郁和焦虑患病的风险。同时,也会导致免疫功能障碍,代谢异常,心血管系统疾病等多种疾病的发生。
而现阶段,针对焦虑及抑郁的临床治疗药物往往伴随着诸如性功能障碍,代谢异常及持续性高血压在内的多种副作用,因此,寻找更有效治疗方法成为医学界焦点之一。
2019 年 10 月 31 日,浙江大学生命科学研究院靳津实验室联合东南大学柴人杰实验室在 Cell 杂志发表题为《Stress-induced metabolic disorder in peripheral CD4+ T cells leads to anxiety-like behavior》的研究论文,创新性地提出了压力应激情况下,外周 CD4 +T 细胞嘌呤合成代谢功能异常与焦虑症之间的联系。同时,打破传统抗焦虑、抗抑郁症药物的治疗思路,提出靶向外周的药物治疗新思路。

图片来源:Cell
研究团队发现,CD4+ T 细胞在压力诱导的焦虑行为中发挥重要作用。其中,研究人员利用足底电击刺激(electronic foot shock)及束缚应激模型(Restraint stress model)等模型,通过检测矿场实验(Open-field test),高架十字迷宫实验(Elevated plus maze test)等多种行为学实验验证,发现体内缺少 CD4+ T 细胞的小鼠,可以避免外界慢性压力应激诱导产生的焦虑症状。
随后,研究团队通过转录组学和代谢组学分析发现,压力应激引发代谢异常及 CD4+ T 细胞线粒体裂变。其中,慢性应激条件下,小鼠体内 LTB4(白三烯 b4)水平显著提高,从而引起非炎性 CD4+ T 细胞线粒体裂变。
而 CD4+ T 细胞线粒体裂变引起血清嘌呤(腺嘌呤,次嘌呤和黄嘌呤)水平升高,同时,临床证据也证实,焦虑症患者相比于健康对照组,血清黄嘌呤水平显著升高。
此外,研究团队发现,过度的 CD4+ T 细胞线粒体裂变,促进转录因子 IRF1(干扰素调节因子- 1)累积,而 IRF1 与 Ada、Xdh 和 Pnp2 启动子区结合,促使葡萄糖更多的通过戊糖磷酸(PPP)途径代谢,进而从头合成黄嘌呤。
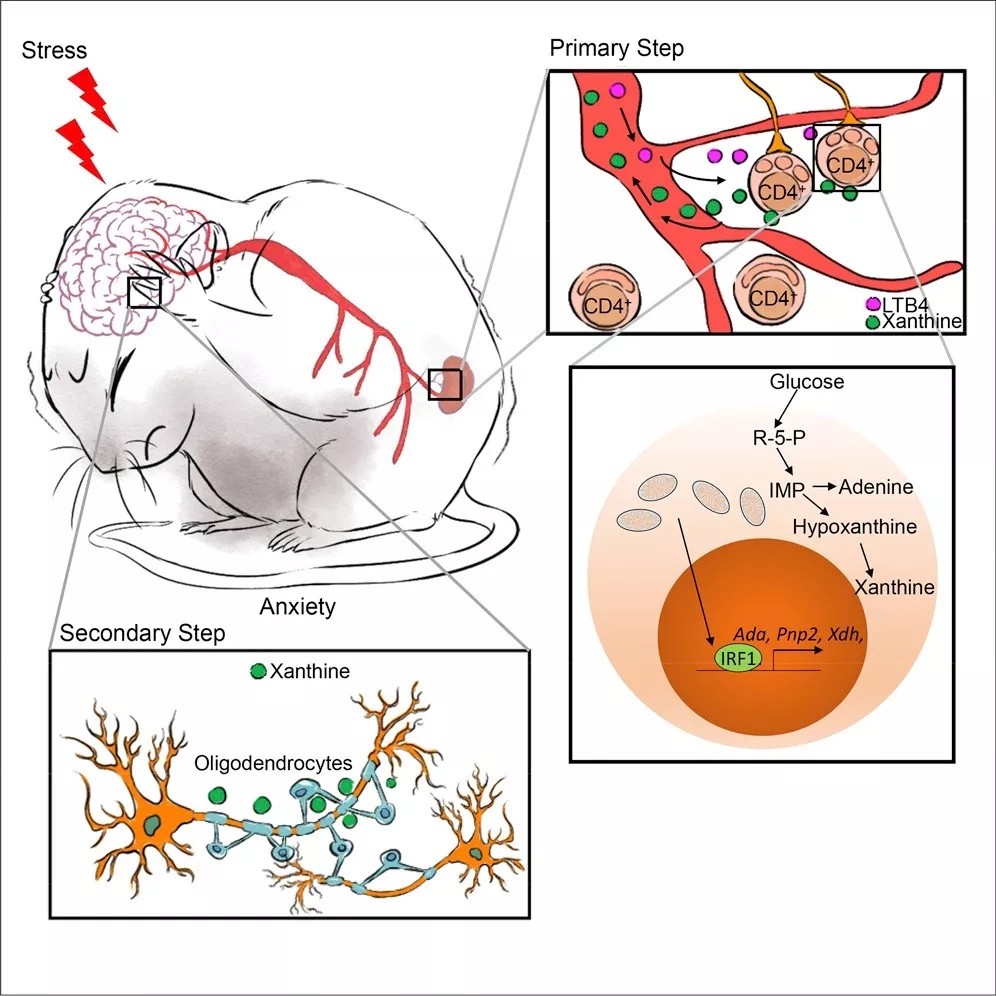
图片来源:Cell
而 CD4+ T 细胞线粒体分泌的过量嘌呤,通过血液循环进入中枢神经系统,与大脑杏仁核少突胶质细胞上的腺苷受体 A1 结合,显著激活少突胶质细胞,继而过度活化左侧杏仁核区域神经元,导致焦虑症状发生。
1950 年,Han Selye 就提出神经免疫概念,并开始探索免疫细胞和神经系统之间的联系,而近 70 年的研究,尚未准确地定义情绪控制及焦虑发病中免疫系统的作用和机制。
该团队研究成果揭示,慢性压力应激情况下,如何影响外周 CD4+ T 细胞线粒体形态,进而如何导致焦虑症状的分子机制,为神经发育和神经疾病和神经精神病与免疫生理功能之间的联系提出了更进一步的见解,对抑郁症和焦虑症的发病提出新机制,并为临床治疗药物研发提供新思路。