高尿酸血症模型研究进展及模型推荐
集萃药康
Uox-KO 小鼠可自发出现高尿酸血症表型,适用于高尿酸血症、痛风、尿酸肾病研究。
高尿酸血症(hyperuricemia,HUA)由嘌呤代谢紊乱使血尿酸(UA)生成过多或 UA 排泄减少所致,是痛风的生化基础。研究表明,HUA 与肥胖、高血压、糖尿病和心血管疾病等有着密切的关系。近年来,随着人们生活水平的提高,饮食结构和生活习惯的改变,高尿酸血症的患病率逐年增高,重视对高尿酸血症的治疗已引起临床的关注。
目前对于高尿酸血症的治疗,临床上常用的药物包括别嘌呤醇和苯溴马隆等,但这些药物均有一定的毒副作用,如别嘌呤醇会导致体内脂质过氧化损伤,对肾脏、肝脏及皮肤黏膜都有较大的损害。因此,对高尿酸血症治疗新靶点和新药物的研究获得了广泛的关注,而建立稳定持续的高尿酸血症模型则是研究的重要前提。
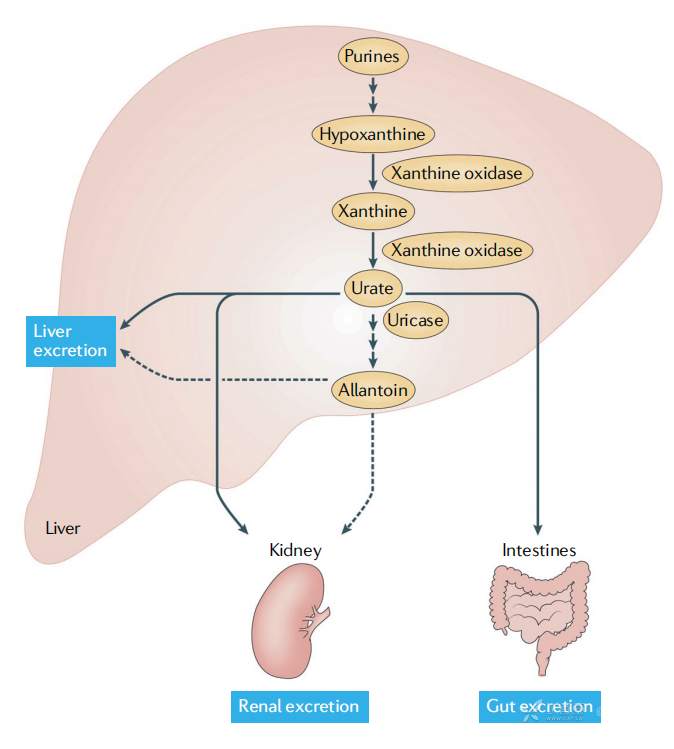
图 1. 尿酸代谢途径[1]
尿酸是大多数动物体内嘌呤代谢的终产物,由黄嘌呤氧化酶(xanthine oxidase,XOD)将次黄嘌呤(hypoxanthine,HX)、黄嘌呤(xanthine)等尿酸前体物质氧化而成。人体内 80% 的尿酸是由体内氨基酸等其他小分子化合物合成尿酸或分解代谢而来;20% 的尿酸从含嘌呤或核蛋白丰富的食物中分解得到。由于在人类中尿酸酶基因沉默不表达,因此患高尿酸血症的风险也大大增加。而在多数哺乳类动物中尿酸氧化酶基因正常表达,尿酸直接分解成尿囊素,随尿液排出体外。因此在动物模型中复制人类高尿酸血症具有一定困难。
高尿酸模型造模机制
常用的高尿酸血症动物模型主要分为两类:药物诱导模型和基因敲除模型。前者是根据尿酸的代谢途径使用药物,通过增加尿酸来源或减少尿酸排泄来实现,又分为三类:增加尿酸的摄入、抑制尿酸的排泄、抑制尿酸酶活性;后者主要涉及到尿酸酶 Uox 和转运体 ABCG2 基因的敲除[2-3]。
增加尿酸的摄入
尿酸前体物质或者富含嘌呤食物可以促进尿酸的产生,常用的药物或食物主要有黄嘌呤、次黄嘌呤、酵母及沙丁鱼等。在短时间内给予大量的外源性尿酸,也可引起血尿酸明显升高,尿酸的进一步积累可能导致痛风,并存在引发心血管疾病、肾脏疾病和代谢综合征等的风险。
抑制尿酸的排泄
体内的尿酸主要从肾脏清除,抑制肾脏排泄尿酸,可使血尿酸浓度增高,形成高尿酸血症。
通过给予烟酸、乙胺丁醇等抑制肾脏的排泄功能,增加尿酸在体内的蓄积,从而增加体内血尿酸水平。
抑制尿酸酶活性
尿酸酶可催化体内尿酸氧化成尿囊素或其他物质,因此可以通过抑制或者消除尿酸酶的活性建立高尿酸血症模型。氧嗪酸及氧嗪酸盐可抑制尿酸分解成尿囊素,从而使尿酸水平升高,目前应用较为广泛,多采用饲喂法、灌胃法以及腹腔注射法进行造模。
基因改造模型
利用基因工程技术使动物产生尿酸酶的基因缺失,获得尿酸酶缺乏的小鼠,造成高尿酸血症模型。Uox 是尿酸氧化酶基因,该基因确实导致尿酸分解严重受阻,造成严重的高尿酸血症;ABCG2 是一种跨膜转运蛋白/高容量尿酸分泌蛋白,主要影响尿酸排泄,该基因敲除会导致尿酸水平升高,但升高水平有限。
表 1. 高尿酸血症基因敲除模型动物[2]
![]()
Uox-KO 模型推荐
集萃药康通过 CRISP/Cas9 技术构建 Uox-KO 小鼠模型,纯合小鼠表现出严重的高尿酸血症和尿酸肾病,纯合小鼠在出生几周后会陆续出现死亡(文献报导~65%的纯合小鼠在 4 周龄时死亡[4])。因此,Uox-KO 小鼠出生后需别嘌呤醇等药物维持生存。
Uox-KO 小鼠
品系全称:B6/JGpt-Uoxem3Cd3501/Gpt
品系编号:T011801
应用领域:高尿酸血症、痛风、尿酸肾病研究
Uox-KO 小鼠表型及药效验证
1. 雄鼠和雌鼠都自发出现高尿酸血症,雌鼠的平均尿酸水平较雄鼠低,但个体均一性较雄鼠好,别嘌呤醇可以显著改善因 Uox 敲除引起的小鼠高尿酸血症。
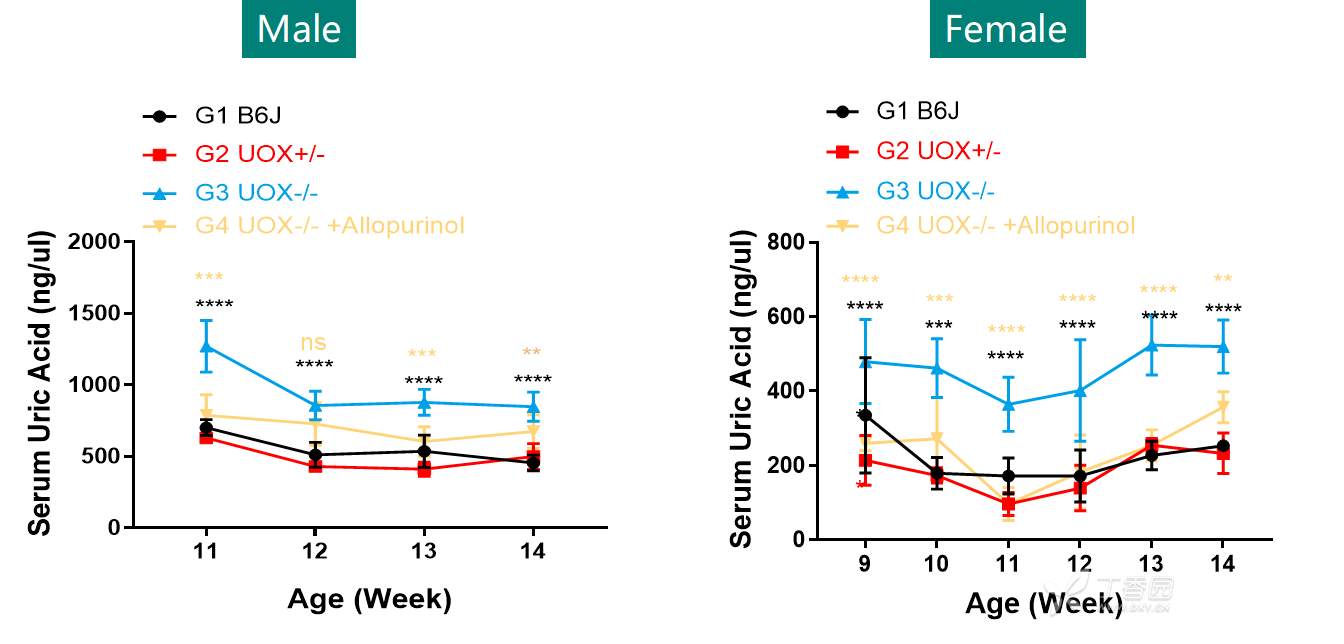
图 2. 图片来源:集萃药康
2. Uox-KO 雄鼠和雌鼠肌酐、尿素氮水平升高,提示出现肾损伤,且雄鼠肾脏损伤较雌鼠更加显著,别嘌呤醇(G4 组)无法改善 Uox-KO 引起小鼠的肾功能损伤。
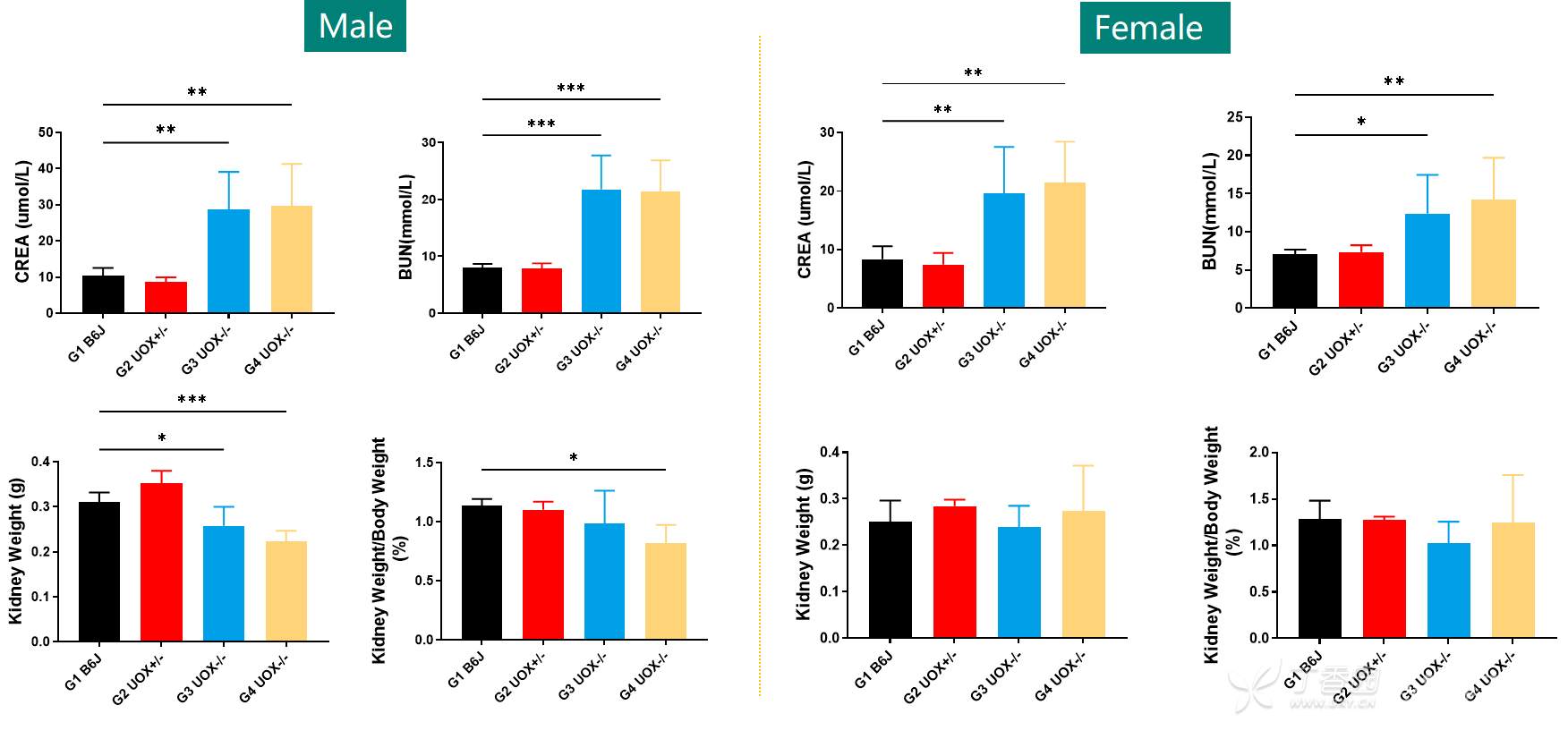
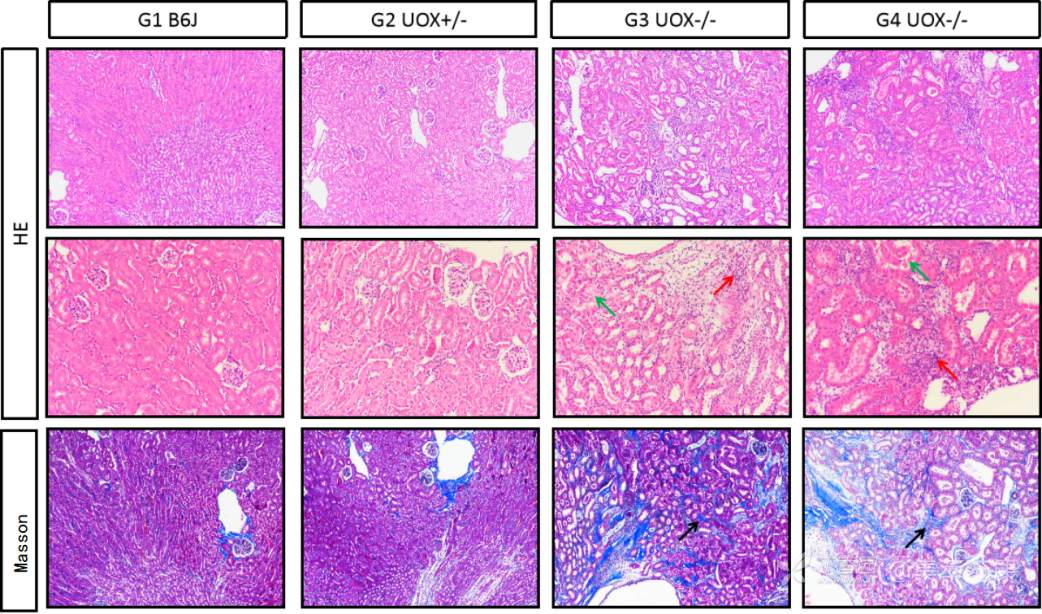
图 3. Uox-KO 小鼠肾脏组织病理染色观察(HE & Masson),出现间质纤维组织增生,炎细胞浸润;肾小球萎缩,系膜组织增生;血管壁增厚;肾小管扩张形成囊肿;肾小管管腔内可见均质红染物质渗出。别嘌呤醇(G4 组)无法改善 Uox-KO 引起小鼠的肾脏病变。图片来源:集萃药康。
参考文献:
1. Lu et al. Mouse models for human hyperuricaemia: a critical review. Nat Rev Rheumatol[J]. 2019.
2. 何宏明等,不同方法建立高尿酸血症动物模型研究进展[J]. 江西中医药,2015.
3. 张楠等,高尿酸血症动物模型的研究进展[J]. 昆明医科大学学报,2019.
4. Wuet al. Hyperuricemia and urate nephropathy in urate oxidase-deficient mice[J]. Proc Natl Acad Sci USA. 1994.
![十二烷基二甲基(3-磺丙基)氢氧化铵内盐 [用于生化研究],14933-08-5,≥98%,阿拉丁](https://img1.dxycdn.com/p/s14/2024/0619/475/6370229598169633081.jpg!wh200)







