新冠疫苗「管」多久?加强针应何时接种?PNAS 研究提醒:不同人群的接种间隔应不同
丁香学术
导读
COVID-19 给医疗系统和社会带来了前所未有的挑战。疫苗接种是对抗 SARS-CoV-2 感染和 COVID-19 发展的有效措施,但其有效性可能会随着时间的推移而减弱,并可能受到病毒或患者特异性因素的限制。其中,大量未接种疫苗的人群、免疫抑制患者的疫苗反应不完全以及接种疫苗后免疫力下降都导致了危机的持续。因此,了解疫苗诱导免疫的局限性对于应对 COVID-19 大流行至关重要。
目前,世界各地正在进行大量的临床研究,以评估 mRNA 和腺病毒载体疫苗随着时间的推移对 SARS-CoV-2 病毒和新变体的保护能力。基于这些研究,领域专家普遍认为需要加强剂量来维持足够的免疫水平,特别是在接受化疗或其他免疫抑制治疗的癌症患者或接受免疫调节药物的其他个体中。
这些发现已迅速被纳入公共卫生建议,但目前仍不确定加强剂量能在多长时间内保证免疫力,以及它们对新出现的变异有效性如何。在动态演变的大流行中,特别是对于最有可能遭受免疫力下降的有害后果的高危患者群体,目前还没有经过验证的数据来前瞻性预测最佳疫苗时间表。
2023 年 1 月 9 日,麻省总医院、哈佛医学院等单位的研究人员在 PNAS 发表了题为 Mechanistic model for booster doses effectiveness in healthy, cancer, and immunosuppressed patients infected with SARS-CoV-2 的文章,他们通过建立的数学模型来解释疫苗诱导的免疫,预测了疫苗有效性随时间的变化。
分析结果表明,mRNA 疫苗的增强剂量可以诱导抗体水平和相关类型的适应性免疫细胞数量的强劲增加,预计这将在健康患者中提供超过 1 年的保护。不过,他们的模型还表明,对于存在免疫抑制的人群或接受免疫抑制治疗的癌症患者,增强剂的作用可能会减弱,应该更频繁地给予增强剂。
总之,这一模型为未来的疫苗接种提出了可能的方案,并为高危人群提出了量身定制的策略。
图片来源:PNAS
主要研究内容
研究人员建立的数学模型涵盖了包括 mRNA 疫苗和 Ad26.COV2.S 病毒载体疫苗在健康、免疫抑制和癌症患者中的独立数据,结合疫苗诱导免疫、SARS-CoV-2 感染和 COVID-19 病理生理学的已知机制,以研究加强剂量对体液和细胞介导免疫的影响,以及感染原始病毒和变异病毒后临床病程的严重程度。此外,他们还模拟了接种疫苗 100 周内(700 天)的效果,包括第三剂 mRNA 疫苗和第二剂载体疫苗,并评估了刺突特异性抗体水平的长期稳健性。
该模型解释了病毒抗原的翻译、抗原的产生和树突状细胞的呈递、B 细胞和 T 细胞和随后激活产生的血浆 B 细胞以及 CD4+和 CD8+效应和记忆 T 细胞。此外,他们还考虑了各种抗癌疗法,包括化疗和 PD-L1/PD-1 免疫检查点封锁疗法。总之,该研究构建的这一数学模型可以用于预测健康和免疫抑制患者的疫苗诱导免疫的长期过程,并且超过了目前可用的临床数据的时间框架。

图片来源:PNAS
疫苗接种后的免疫反应
他们将模型预测与来自七项独立临床研究的额外数据进行了比较,这些研究涉及接种疫苗的健康参与者和接受化疗或 PD-L1/PD-1 免疫检查点封锁疗法的癌症患者的加强剂量。他们检测了同源疫苗接种(即不混合不同疫苗类型)对原始株和变异株感染 SARS-CoV-2 后免疫力和临床病程严重程度的影响。模型参数包括细胞对疫苗颗粒的亲和力及其摄取率、脱氧核糖核酸对信使核糖核酸的转录率、病毒抗原的产生和退化率以及疫苗的降解率等。
与临床研究一致,该模型预测,在接种所有类型的疫苗后 6 个月内,抗体将大幅减少,并在接种加强剂量后抗体水平迅速而强劲地增加。对于健康个体,在整个模拟期间(即从加强剂量开始的 78 至 80 周),mRNA 疫苗加强剂量后的抗体水平预计将保持在 10,000 U/mL 以上,而腺病毒载体疫苗加强剂量后的抗体水平预计将保持在 1,000 U/mL 以上,但对于癌症患者,特别是免疫抑制患者,抗体水平将达到较低的值。抗体水平高于 1,000 U/mL 已被认为与保护性免疫相关。
唯一的例外是接受 PD-L1/PD-1 抑制的癌症患者,根据该模型预测,他们表现出与健康个体相同的抗体水平。有趣的是,接受第三次 mRNA 疫苗接种的健康个体可以在 180 周内保持抗体水平高于 1,000 U/mL。尽管目前还没有来自加强剂量的长期数据,但模型预测与目前可用的抗体水平和 T 细胞免疫反应的有限数据一致,也与接受化疗、抗 cd20 治疗或 BTK 抑制剂的癌症患者在接受第三次 mRNA 疫苗接种后的临床数据所作的预测一致。
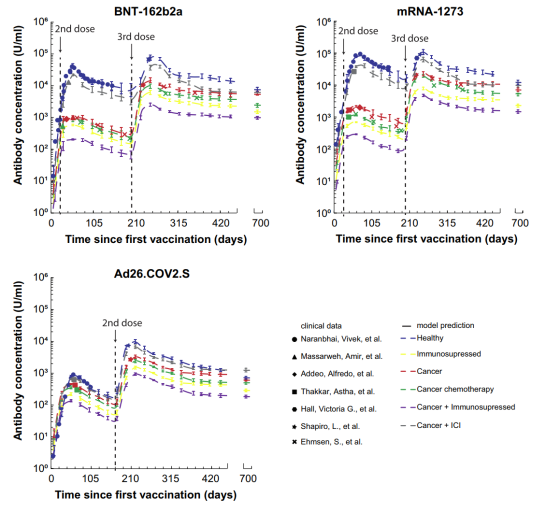
图片来源:PNAS
mRNA 疫苗接种后的优势
他们还记录了 mRNA 疫苗接种后 6 个月免疫反应下降的情况以及疫苗接种对影响病毒感染严重程度的免疫细胞水平的影响。在第二次 mRNA 接种后的 6 个月内,B 细胞、CD4+、CD8+ T 细胞和抗原呈递细胞下降高达 50%,与观察到的抗体水平下降相同。然而,在加强剂量后,所有免疫细胞都增加了,只有免疫抑制个体的所有免疫细胞增加不到 50%。
mRNA 疫苗的增强剂量可诱导抗体水平和相关类型的适应性免疫细胞数量的强劲增强,预计可在健康个体中提供超过 1 年的足够保护。
然而,他们的模型表明,对于免疫抑制的人或接受免疫抑制治疗的癌症患者,促进作用可能会减弱,也许应该考虑更频繁的疫苗加强接种。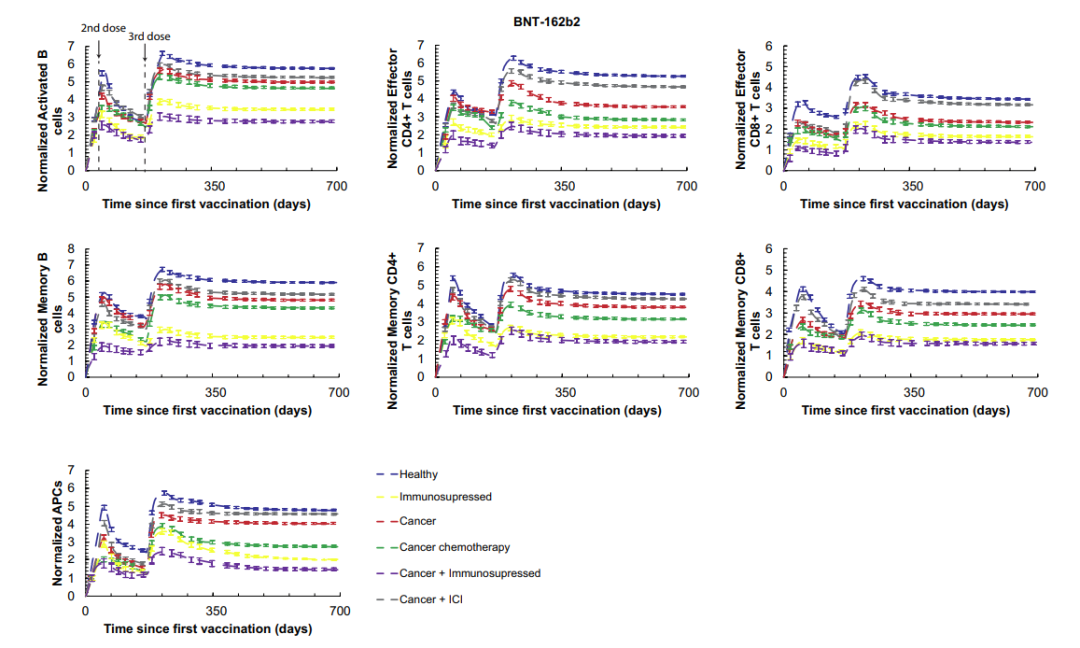
图片来源:PNAS
疫苗接种对特殊人群及突变体的效应
患有癌症或免疫抑制的患者因 COVID-19 发生严重后果的风险更高,并且无法清除病毒的风险明显更高。因此,确保在这一患者群体中得到保护是非常重要的。这一模型模拟表明,这些群体需要量身定制的疫苗接种方法,特别是考虑在第一次加强剂量之外的额外剂量,优先考虑下一代疫苗方法,并考虑额外的预防措施。一个有趣的发现是,在免疫检查点抑制的癌症患者中,疫苗介导的保护与健康个体相似,表现出相同的抗体水平。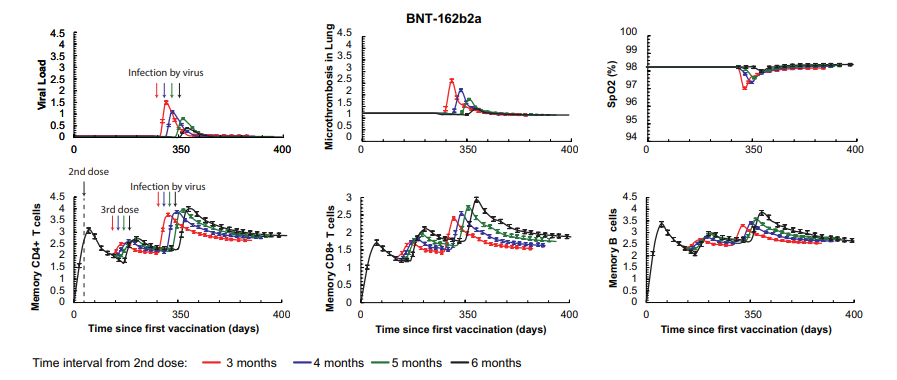
图片来源:PNAS
他们的模型还能够预测新的 SARS-CoV-2 变种对 COVID-19 感染的影响。模拟结果表明,靶细胞结合增强、抗体结合减少或抗原性/免疫原性降低的变异将带来最大的临床挑战,甚至会导致健康接种者严重感染。这种变异降低了现有疫苗提供的保护,需要额外的加强剂量或改进疫苗配方。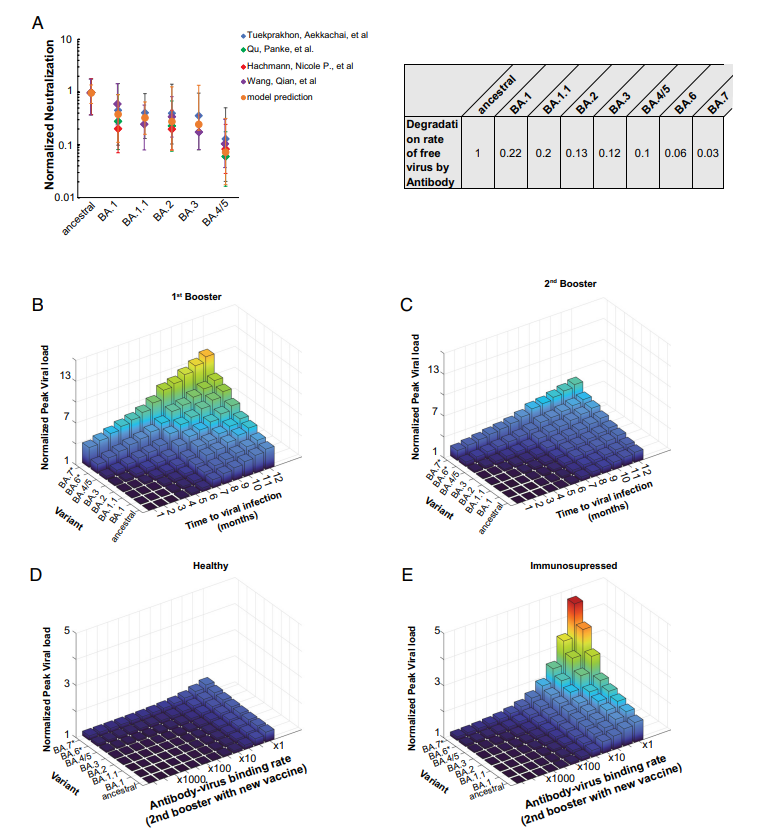
图片来源:PNAS
结语
综上所述,该研究通过模拟接种疫苗 6 个月后健康和免疫抑制患者的免疫反应下降,证实了 mRNA 疫苗相对于 Ad26.COV2.S 病毒载体疫苗的优势。该研究表明,在健康患者中,加强剂量的 mRNA 疫苗可诱导超过一年的保护。然而,对于免疫反应受到抑制的人或接受免疫抑制治疗的癌症患者,增强效应可能会很快减弱。因此,应更频繁地给这些患者接种加强疫苗。
本研究通讯作者,麻省总医院肿瘤生物学实验室主任 Rakesh K. Jain 教授说到:「我们使用这个模型来模拟病毒、患者和疫苗特征的差异如何影响 COVID-19 感染的结果,这可能有助于提醒具有不同特征和合并症的个体加强疫苗接种的时间,并有助于防止新变种的进一步爆发和发展。」