这个微量元素太重要!激活 T 细胞、增强机体免疫,助力抗癌抗感染……Cell 揭开其中奥秘
丁香学术
导读
镁,作为哺乳动物细胞内最重要的微量营养素之一,参与数百种的化学反应和生物学过程,例如,协助肌肉收缩,调控心脏正常的节律等。最新的研究还表明,镁在免疫系统发挥功能的过程中扮演着重要的角色,但其具体的分子机制尚未明确。
此外,低镁饮食或低镁血症与各种疾病的病理生理学相关,包括感染和癌症。当小鼠接受低镁饮食时,癌细胞在小鼠体内的扩散速度更快,而且它们对流感病毒的防御能力也受损。然而,到目前为止,关于这种矿物质究竟如何影响免疫系统的研究还很少。
2022 年 1 月 20 日,来自瑞士巴塞尔大学等单位的研究团队在 Cell 发表了题为 Magnesium sensing via LFA-1 regulates CD8+ T cell-effector function 的研究性文章,他们发现共刺激细胞表面分子 LFA-1 需要镁来改变其构象,从而促进其活化 CD8+ T 细胞的能力,最终增强 CD8+ T 的细胞毒性。同时,镁的参与也可显著提高病原体和肿瘤特异性 T 细胞的效能,增强了双特异性 T 细胞抗体的效力,并改善了 CAR-T 细胞的功能等。
总的来说,这项研究拓宽了领域内对镁在免疫系统中发挥作用的机理的认识,并在概念上将共刺激和营养感知联系了起来,具有潜在的临床应用前景。
图片来源:Cell
主要研究内容
首先,研究人员探索了体外环境下,Mg2+是如何影响记忆性 CD8+ T 细胞的功能,结果发现,在 Mg2+缺失的情况下,活化的 T 细胞前体细胞的聚集显著减少,其活性也进一步降低。随后,通过不同功能基因集的整合分析,他们鉴定出 ITGAL(CD11a)可能是 Mg2+发挥重要功能的相关基因,而 CD11a 可与 CD18 结合形成白细胞功能相关抗原 1(LFA-1),后者可通过免疫突触的形成参与 T 细胞的活化,以及白细胞的转运和外渗。
随后,他们发现,LFA-1 在 CD8+ T 细胞中表达最低,在记忆效应 CD8+ T 细胞中表达较高,而在 T 细胞前体细胞中含量最高。进一步的实验证明记忆效应 CD8+ T 细胞选择性依赖 Mg2+进行代谢重编程和激活。LFA-1 的分子构象解析也发现,Mg2+对 LFA-1 的构象改变具有调节作用,这对于由外向内的信号传导和下游的 T 细胞激活至关重要。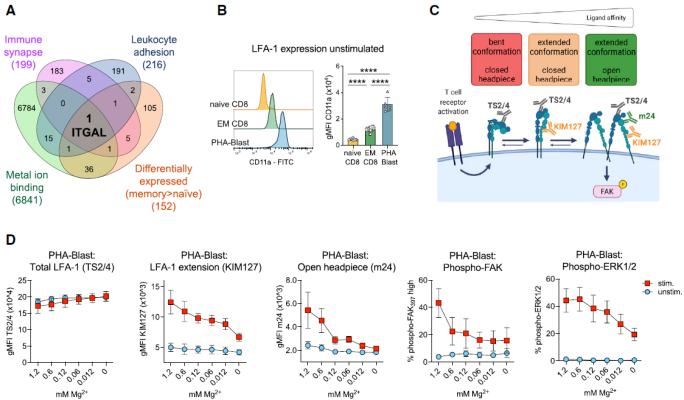
图片来源:Cell
Mg2+-LFA-1 轴增强肿瘤特异性 T 细胞免疫突触的形成
接下来,他们直观地研究了 Mg2+在肿瘤特异性 T 细胞免疫突触的形成中的作用,他们在 T 细胞和靶细胞之间物理作用密切的部位发现了早期抗原特异性的 LFA-1 构象改变,这依赖 Mg2+的参与。T 细胞和靶细胞之间相互作用位点的磷酸化酪氨酸信号强度也反映了 LFA-1 的构象改变。免疫突触成熟的特征是中心体极化和细胞溶解颗粒的集中传递,成像结果也表明这两个事件同样与 Mg2+-LFA-1 轴有关。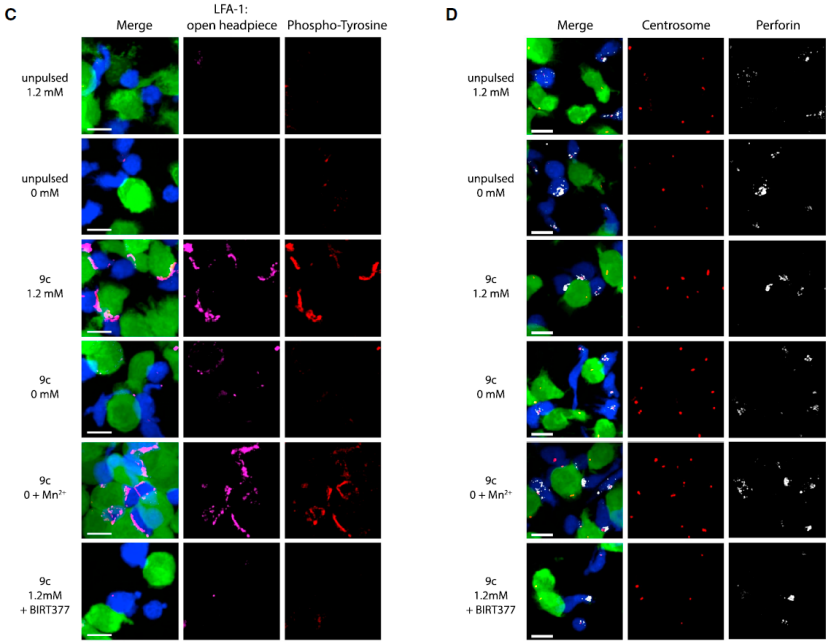
图片来源:Cell
LFA-1 是 Mg2+在体内塑造 T 细胞激活和效应功能所必需的
接下来,他们在小鼠模型上研究了 LFA-1 基因缺失是如何影响 T 细胞功能与体内 Mg2+ 丰度的关系。通过饮食限制很容易诱导 Mg2+的消耗,同时 Mg2+饮食也不影响小鼠的总体健康状况,各组间体重相当。在限制镁饮食 2 周后,他们激活体内 CD8+T 细胞,发现机体 Mg2+丰度正常小鼠的 CD8+ T 细胞能够正常激活,而相比之下,LFA-1 的缺失则使其激活显著降低。
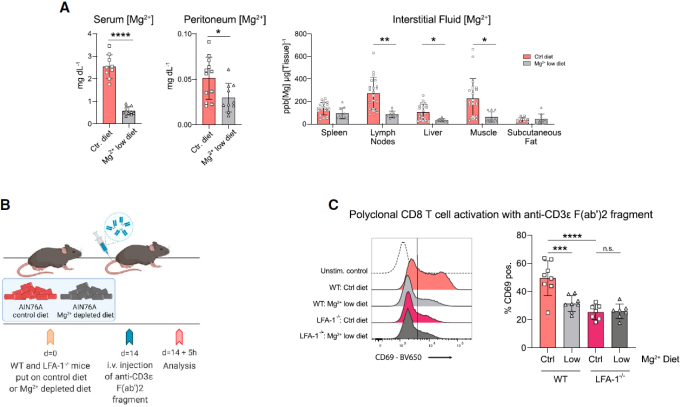
图片来源:Cell
瘤内镁给药可改善 CD8+ T 细胞介导的抗肿瘤免疫
上述实验证明镁在激活 CD8+ T 细胞层面具有重要作用,那么这种增强作用是否可用于抗肿瘤免疫?他们发现,注射 Mg2+能够改善小鼠体内肿瘤的生长。利用流式细胞术,他们分析了肿瘤浸润免疫细胞,发现 Mg2+处理组肿瘤浸润的 CD8+ T 细胞数量显著增加,并表达活化标记物 CD25,进一步反映了 CD8+ T 激活的增加。
图片来源:Cell
由于 PD-1 在 CD8+ T 细胞上的表达较高,他们接下来评估了 MgCl2 注射联合 PD-1 阻断剂在影响肿瘤特异记忆性 CD8+ T 细胞层面的效应。结果发现,同时接受瘤内 MgCl2 和 PD-1 阻断小鼠的肿瘤控制效果优于所有其他药物组,显著延长小鼠的生存。此外,单独使用 MgCl2 也可显著改善免疫状态并控制肿瘤生长。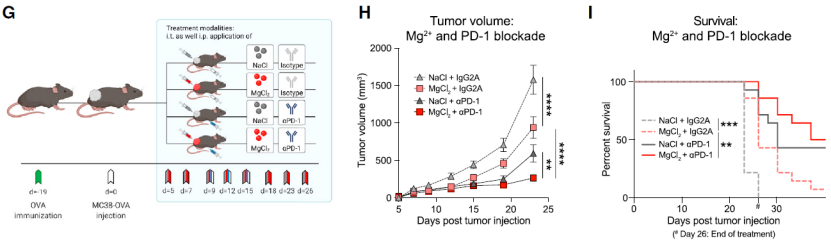
图片来源:Cell
Mg2+在 CAR-T 细胞疗法中的作用
接下来,他们探讨了 Mg2+在 CAR-T 细胞治疗中的作用。与前期的研究结果一致,Mg2+-LFA-1 调控系统亦能够增强 CD19 CAR-T 细胞的抗肿瘤活性,而 Mg2+的缺失则严重削弱了 CAR-T 细胞特异性杀伤靶细胞的能力。同时,在 Mg2+缺失的条件下,CAR-T 细胞释放的 IFN-g 也相应减少。此外,在注射 Mg2+后,CAR-T 细胞治疗中的抗肿瘤反应显著增强,小鼠生存期也得到了显著改善。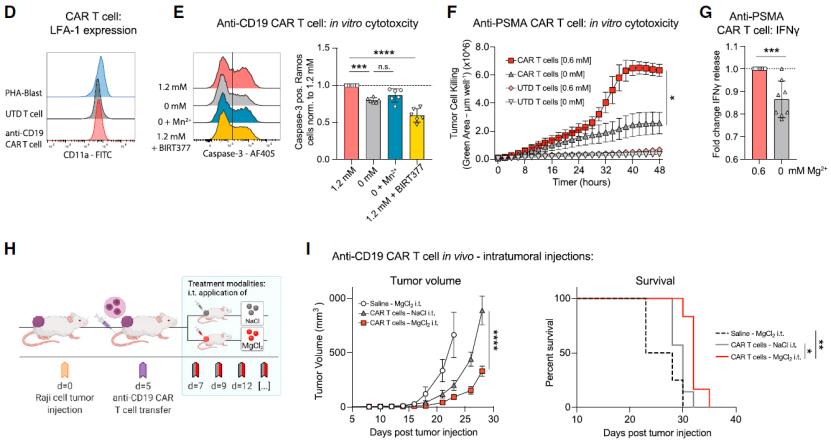
图片来源:Cell
最后,他们回顾性评估了血清 Mg2+水平与 CAR-T 细胞治疗和免疫检查点阻断疗法临床结果之间的关系。在接受 CD19 靶向 CAR-T 细胞治疗的 100 例难治性 B 细胞淋巴瘤患者中,血清 Mg2+水平较高的患者的总生存期和中位无进展生存期均显著高于低 Mg2+ 组。在另外一个接受免疫检查点阻断疗法的非小细胞肺癌患者队列中,同样发现患者的完全缓解和总生存率在低镁血症患者中均显著降低的事实。这些结果表明,Mg2+可能有助于提高人类患者中抗肿瘤疗法的临床疗效。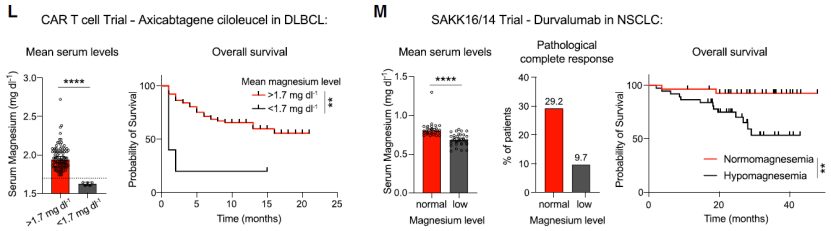
图片来源:Cell
结语
综上所述,在这项研究中,研究人员确定了细胞外 Mg2+可作为一种免疫调节剂,通过与 LFA-1 结合而调节 T 细胞的激活,并发挥抗肿瘤效应。因此,LFA-1 能够感知 Mg2+,并将其丰度整合在共刺激功能中,通过这条轴,Mg2+选择性激活特异性 T 细胞。

图片来源:Cell
本研究证实,血液中的镁含量是免疫系统应抵抗病原体和癌细胞能力的一个重要因素,这一发现为现代癌症免疫疗法增添了另一维度的信息,对指导和改善现有抗肿瘤方案具有重要意义。
该研究通讯作者 Christoph Hess 教授说:「为了在临床上验证这一研究结果,我们现在正在寻找有针对性地增加肿瘤中镁浓度的方法。虽然说现有的数据无法表明定期摄入镁是否会影响患癌症的风险,但是在未来,我们计划进行前瞻性研究,以测试镁作为免疫系统催化剂的临床效果。」