躺平减肥要成真了!中国团队发现局部热疗可激活米色脂肪助力安全减肥,登顶 Cell 封面
生物学霸
导读
肥胖是导致糖尿病、高血压、高血脂等代谢性疾病、心血管性疾病和某些肿瘤的重大危险因素,严重危害人类健康。肥胖通常是指脂肪组织中脂肪的过度积累,而脂肪根据其解剖位置和代谢功能,又可分为白色脂肪、棕色脂肪和米色脂肪(Beige fat)。
其中,米色脂肪是一类新发现的脂肪类型,拥有巨大的可塑性,其在静息时表现出白色脂肪的特质,但是当处于寒冷或肾上腺素信号激活的情况下,具有棕色化潜力,并促进产热和能量消耗,改善机体糖脂代谢。研究发现,成年人肩胛骨附近分布有米色脂肪,因此,面对当前肥胖的流行,发现有前景的基因靶点和途径,实现安全有效的米色脂肪激活,不失为一种对抗肥胖的有效手段。
热疗(Hyperthermia Therapy, HT),作为一种治疗代谢性疾病潜在的方法,成功吸引了越来越多科研人员的兴趣。前期的研究表明,通过温水浸泡的方式能改善各种动物模型的代谢状态。因此,这些数据支持了将热疗作为一种有效方式来对抗肥胖。
近日,华东师范大学生命科学学院马欣然、徐凌燕研究员携手上海交通大学附属第六人民医院胡承教授与华东师范大学生命科学学院张强研究员在国际顶尖期刊 Cell 杂志上发表了题为 Local Hyperthermia Therapy Induces Browning of White Fat and Treats Obesity 的研究论文,他们系统研究了米色脂肪局部热疗在产热和脂肪代谢中的作用,并阐明了其可通过 HSF1-A2b1 转录轴发挥作用的分子机制,这一研究成果将为治疗肥胖和代谢性疾病提供新的策略。
图片来源:Cell
主要研究内容
热疗在体外和体内诱导产热
为了测试米色脂肪细胞是否能够以细胞自主的方式感知高温,他们将米色脂肪细胞置于高温环境(HT)或室温并研究了热疗对其的影响。结果发现,与对照组相比,热疗组米色脂肪细胞温度升高,产热增强,同时他们还发现了产热相关基因 Pgc1a 和 Ucp1 (线粒体生成和热生成的标记物) 的表达显著增加。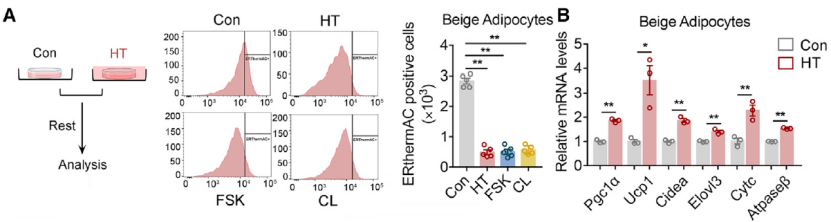
图片来源:Cell
接下来,他们研究了局部热疗(Local hyperthermia therapy, LHT)是否能激活体内米色脂肪产热。通过对小鼠模型注射基于聚多巴胺纳米颗粒构筑的光热水凝胶,并通过红外光照射,实现米色脂肪在温和温度下高效的局部热疗。结果发现,与对照处理相比,热处理组小鼠的热量明显增加,棕色化相关基因的表达水平也出现显著增加,UCP1 蛋白水平亦有增加。
随后,他们又研究了 LHT 对人类米色脂肪产热的影响。成年男女志愿者被置于温度和湿度可控的环境中,并进行局部热处理。与对照组相比,LHT 显著增强了颈部锁骨上的热量,同时还不影响血清中去甲肾上腺素(NE)的水平。因此,这些结果表明,LHT 可通过激活米色脂肪细胞来诱导人体产热,同时还不提高机体核心体温或儿茶酚胺信号通路。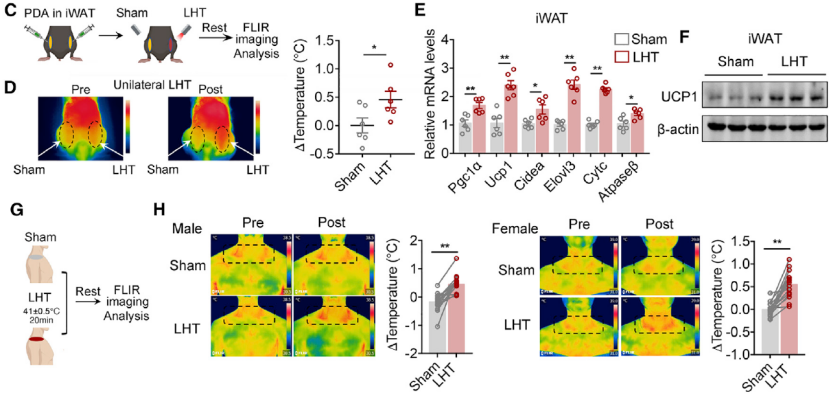
图片来源:Cell
局部热疗可保护和治疗肥胖小鼠
紧接着,他们测试了长期 LHT(超过 10 周)对小鼠的代谢影响。结果发现,在食物摄入量和运动量相似的情况下,高脂饮食诱导的肥胖小鼠(HFD)在 LHT 处理下的体重显著降低,其降重的主要原因是脂肪量的减少,同时小鼠的耐寒能力增强,能量消耗增加,胰岛素敏感性增强,不过小鼠血清中的去甲肾上腺素水平在两组之间相当。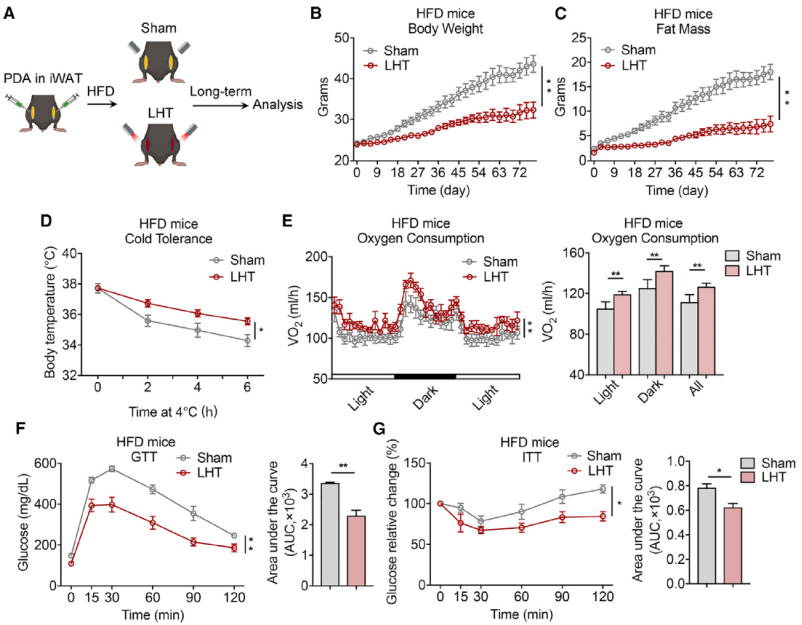
图片来源:Cell
此外,详细的组织学分析结果显示,局部热疗组小鼠的脂肪储量显著减少,肝脏脂肪变性得到了很大程度的改善,肝脏中脂质积累较少,同时小鼠的脂肪细胞尺寸也始终较小。在分子水平上,他们发现 Pgc1a 和 Ucp1 在转录组表达和蛋白水平上都有所增加。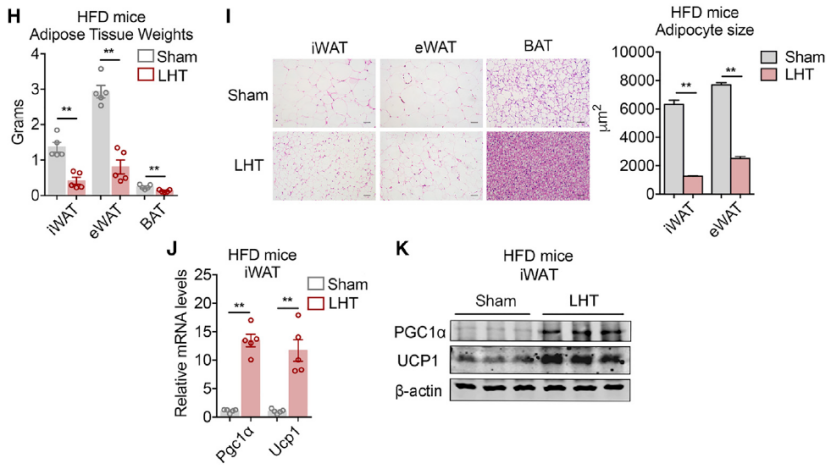
图片来源:Cell
HSF1 对于局部热疗在米色脂肪细胞中的作用是不可或缺的
接下来,他们开始探究 LHT 对米色脂肪激活的机制。前期的研究表明,HSF1 是经典的热休克转录因子,通过调节 HSPs 蛋白的重新折叠和稳态,协调细胞对各种应激的反应。鉴于 HSF1 在热激下被激活的特性,研究人员将目光转向了 HSF1。
他们对 WT 和脂肪特异性敲除 HSF1(FKO)小鼠进行高脂喂养,结果发现 HSF1-FKO 小鼠与 WT 相比明显更肥胖,体重、脂肪量、脂肪组织重量、脂肪细胞大小均升高,胰岛素抵抗和肝脂肪变性更严重。此外,脂肪细胞缺乏 HSF1 还会导致小鼠的产热能力受损。总的来说,HSF1-FKO 小鼠的能量消耗显著减少。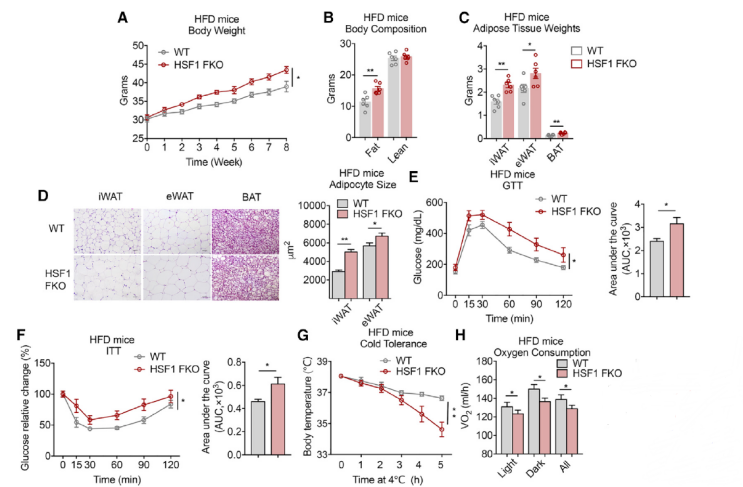
图片来源:Cell
Hnrnpa2b1 水平与米色脂肪细胞的代谢状态相关
为了进一步阐明 HSF1 调控米色脂肪激活的机制,他们采用 ChIP-seq 技术获取 HSF1 结合靶点的基因组图谱。经过和代谢相关的功能基因集进行整合,他们从中鉴定出 Hnrnpa2b1(A2b1),其作为唯一具有 RNA 结合潜力的 HSF1 蛋白靶点,引起了该研究团队的注意。
更加深入的分析显示 HSF1 特异性结合在 A2b1 启动子区域,而该区域存在一个经典的热冲击因子结合元件(HSE)。随后的 ChIP 实验也证实了在米色脂肪细胞中 HSF1 特异性与 A2b1 的 HSE 区域结合。更为重要的是,HSF1 结合在热疗处理后显著增强。此外,HSF1 缺乏在体内和体外都能消除 A2b1 的表达。总的来说,这些结果表明在局部热疗处理后可能存在 HSF1-A2b1 轴的调控。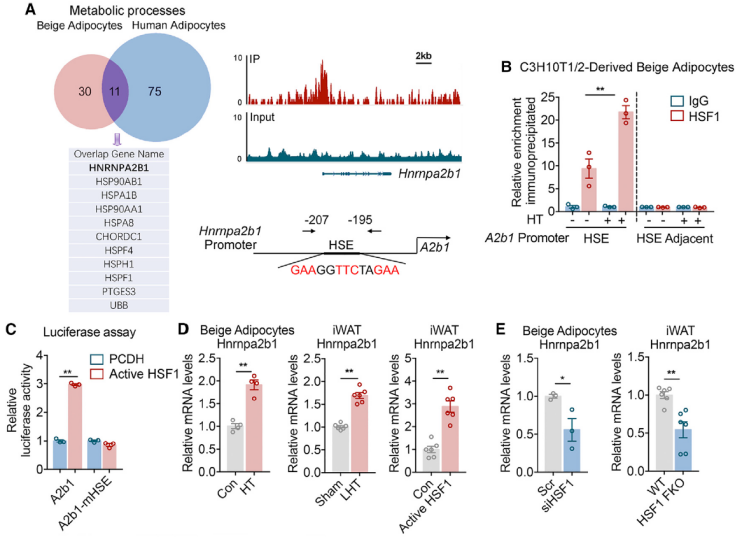
图片来源:Cell
然后,他们进一步探索了 A2b1 在介导 HSF1 在脂肪细胞中的代谢功能中的作用。为了实现这一目标,他们在 HSF1-FKO 小鼠中过表达 A2b1,并将其与 WT 小鼠进行比较。HFD 喂养后,代谢参数的评估结果显示,脂肪中过表达 A2b1 在很大程度上减轻了 HSF1-FKO 小鼠的代谢障碍。此外,A2b1 在 HSF1-FKO 的过表达也可挽救其产热相关基因表达的下降。总之,这些数据表明 HSF1-A2b1 轴可以调节脂肪细胞的褐变,并可防止肥胖和代谢障碍。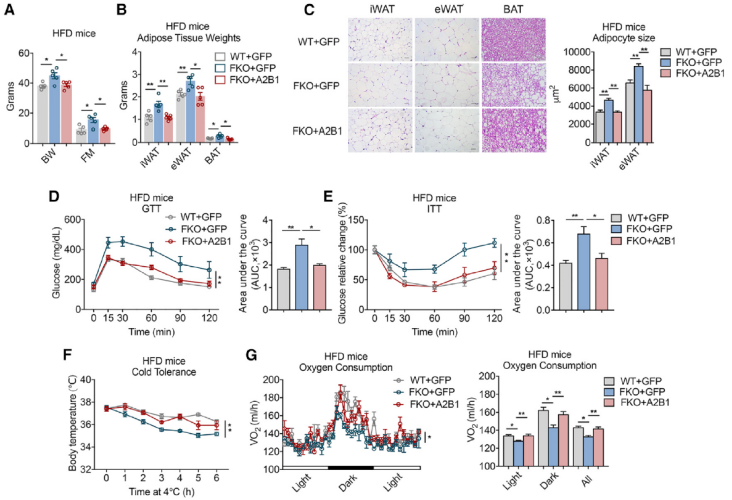
图片来源:Cell
HSF1 变体 P365T 与人类代谢性状的关联
最后,为了探究 HSF1 单核苷酸多态性(SNP)与人类代谢性状关联性,研究团队通过万余人的全基因组关联分析研究(GWAS),在 HSF1 基因的第 9 外显子中发现了错义变异 p.Pro365Thr。同时,他们还发现,突变体 p.Pro365Thr 与人群中多种代谢性状的改善相关联,如较低的 BMI,血清甘油三酯水平,胰岛素敏感性等,这些结果均提示 HSF1 在人类代谢中也发挥着重要作用。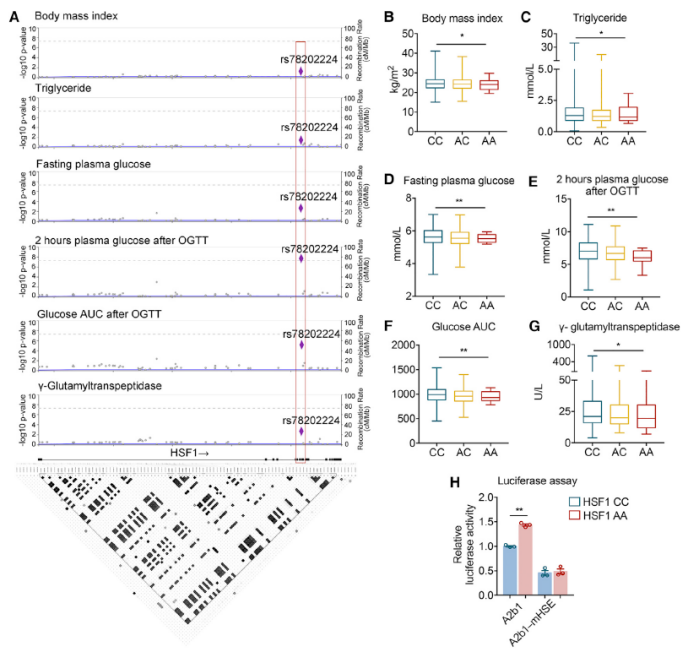
图片来源:Cell
结语
综上所述,本研究创新性地发现通过局部热疗可以精准激活米色脂肪中 HSF1 信号通路,并由此促进产热。同时,该研究还首次在基因组层面发现 HSF1-A2B1 转录轴,进一步完善了 HSF1 代谢调控网络,并在上万人群研究中明确了 HSF1 与代谢性状的关联性。
此外,他们的研究还发现,这种激活产热的途径并不影响交感神经系统或免疫系统,表明了该方法在减肥上的便捷性、安全性及有效性,并可进一步基于此研发药物治疗肥胖并改善胰岛素抵抗和肝脏脂质沉积等代谢紊乱。
总之,该研究全面系统地探索了局部热力在产热和脂肪代谢中的作用,并揭示了其分子调控机制,为肥胖和代谢疾病提供了新的治疗策略。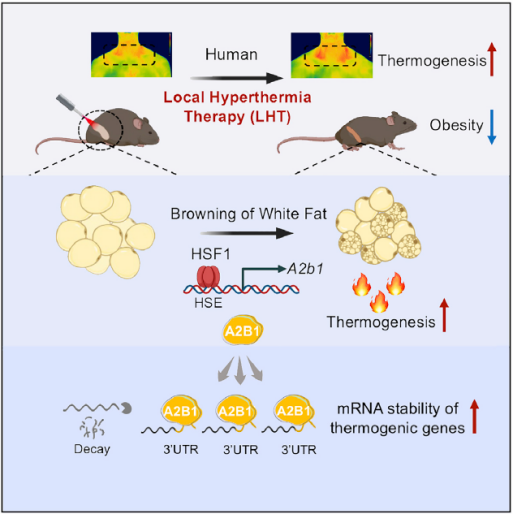
图片来源:Cell