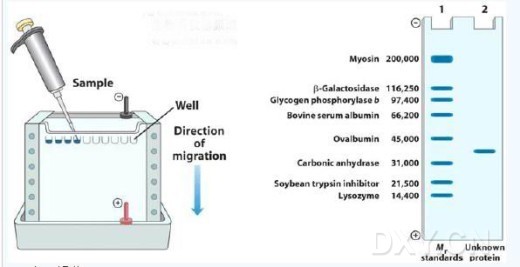
SDS聚丙烯酰胺凝胶电泳
互联网
2296
实验原理:在样品介质和聚丙烯酰胺凝胶中加入离子去污剂和强还原剂后,蛋白质亚基的点泳迁移率主要取决于亚及分子量的大小,而电荷因素可以被忽略。当蛋白质的分子量在15KD到200KD之间时,电泳迁移率与分子量的对数呈线性关系,可以用来测定蛋白质亚基的分子量。
基本过程:制胶、电泳、检测
试剂 :(储液由专业人员配置)30%丙烯酰胺单体储液、10%过硫酸铵、TEMED、1.5mol/L Tris -HCl, pH8.8、1.0mol/L Tris -HCl, pH6.8、10% SDS 、10XTris-甘氨酸系统的电泳 缓冲液 、2Xloading buffer、水饱和正丁醇
器材:灌胶支架、玻璃板、梳子、电源、加热器、电泳槽、扫描仪
实验操作程序:
1.安装灌胶模具,依照说明书进行
2.按照配方配置一定量(7cm模具配置1mm厚的胶配置5ml)的分离胶溶液和浓缩胶溶液(2ml),过硫酸铵和TEMED在用前加入。
3.分离胶溶液充分混匀后从一侧加入灌胶模具,上方留约1.5-2cm用于加浓缩胶,小心的在分离胶的表面加一层水饱和正丁醇(或水饱和的异丙醇、水),封住胶面,以促使聚合并保持胶面平整。
4.室温放置40分钟到1小时后,可以看到一个界面,去掉上层覆盖液,用浓缩胶 缓冲液 淋洗胶面,然后灌制浓缩胶,并插入与模具大小相同,凝胶厚度相当的梳子。
5.静止放置40-60分钟使凝胶聚合,电泳液清洗样品孔。
6.制备好的蛋白质样品用2Xloading buffer 1:1混合,与分子量marker 一起100℃煮3-5min, 12000rpm离心5-10min,(7cm模具、1mm厚度、10孔、考染上样量30ug)
7.加入下槽液,把夹有凝胶的玻板转移到电泳槽,加入上槽液,上样。
8.连接电源,5-10mA/胶开始电泳,待溴酚蓝前沿到达分离胶后加大电流到10-15mA/胶,
9.溴酚蓝前沿到达玻璃板底部时停止电泳,取出凝胶,做好标记,准备染色。
10.染色。见考马斯亮蓝染色操作规程及银染色操作规程。
11.扫描。扫描操作见扫描仪的使用说明。
注意事项
1.在加过硫酸铵和TEMED之前溶液最好抽气,防止溶解在溶液里的分子氧在聚合时产生气泡使胶不均一。
2.过硫酸铵和TEMED的量应根据室温和聚合情况而定。
3.分离胶聚合后最好在4℃放置12小时后再使用,以使凝胶充分聚合,改善电泳时的分辨率。
4.为防止气泡陷入,梳子应倾斜插入。
5.如果带着梳子过夜可能会影响分辨率,所以浓缩胶最好在使用前再灌制。
6.如果没有足够数目的样品,应在加样孔中加样品缓冲液,不要留有空孔,以防止电泳时邻近的带扩展。
7.对样品浓度不确定的情况下,加样时使用梯度加样法,能大致估计出样品的浓度。
参考文献:
1.《蛋白质电泳实验技术》郭尧君编著