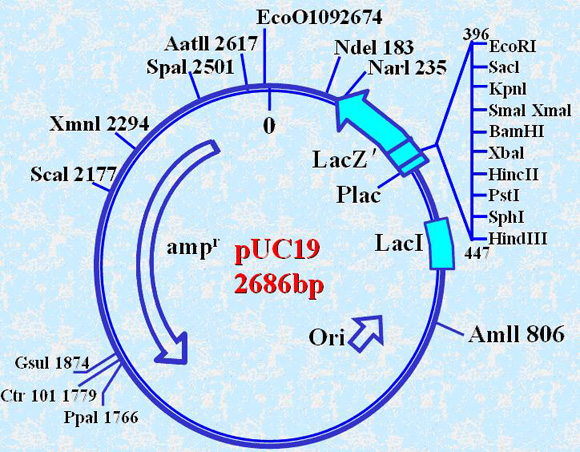
分享“质粒DNA提取鉴定”protocal
丁香园论坛
3423
主要试剂及溶液的配制
细菌培养基:
1)LB液体培养基:
胰蛋白胨 10克
酵母提取物 5克
氯化钠 10克
以950ml去离子水溶解,用5M的NaOH 调pH值至7.0(约0.2ml),最后以去离子水定容至1L。高压灭菌15磅 20分钟,4℃保存。
2)LB固体选择性培养基:
LB液体培养基 1L
琼脂 15g
高压灭菌后,室温放置,待液体温度约50℃时, 加入50mg/ml的氨苄青霉素1ml,使氨苄青霉素的终浓度为50ug/ml。将培养基混匀后在超净台内分别倒入预先灭菌好的10cm2平皿铺板,培养基层2-3mm,待冷却凝固后,密封倒置于4℃保存备用。
碱裂解法提取质粒所用液体
1)溶液I:
溶菌酶 4mg
去离子水 1.4ml
500mM葡萄糖 0.2ml
100mMEDTA 0.2ml
250mMTris-HCl (pH=8.0) 0.2ml
2)溶液II:
去离子水 2.4ml
10%SDS 0.3ml
2MNaOH 0.3ml
3)溶液III:
乙酸钾 29.25g
冰醋酸 11.5ml
加去离子水至100ml
4)1M Tris-HCl缓冲液 (pH=8.0):
Tris干粉 24.24g
去离子水 191.6ml
HCl 8.4ml
5)10% SDS:
10g SDS溶于100ml 去离子水中, 于37℃水浴中使其完全溶解后室温保存。
6)5M EDTA:
取18.612克EDTA溶于50ml去离子水中, 并同时以NaOH调节pH值至8.0 (当pH值接近8.0时, EDTA才可完全溶解), 最后定容至100ml。
7)TE缓冲液 (pH=8.0):
1M Tris-HCl缓冲液 (pH=8.0) 1ml
0.5M EDTA 0.2ml
加去离子水至100ml。
8)50mg/ml氨苄青霉素:
取0.5克氨苄青霉素溶于10ml高压消毒过的去离子水中后, 用孔径为0.22nm滤膜过滤除菌。分装后, -20℃保存。
9)5mol/l LiCl:
21.20克LiCl溶于100ml去离子水中。
10)1.6 mol/l NaCl:
4.23克NaCl溶于50ml去离子水中。
11)含13%PEG8000的1.6 mol/l NaCl溶液:
6.5克PEG8000溶于1.6 mol/l NaCl (50 ml)。
12)酚:氯仿(1:1):
等体积混合Tris平衡酚和氯仿, 现用现配。
电泳系列缓冲液
1)50×TAE:
Tris碱 242g
冰醋酸 57.1ml
0.5mol/l EDTA (pH=8.0) 100ml
以去离子水定容为1L, 4℃保存。用前1:50稀释。
2)6×凝胶加样缓冲液:
0.25%溴酚蓝, 0.25%二甲苯青FF, 30%甘油水溶液, 于4℃保存。
3)溴化乙锭溶液:
将100mg溴化乙锭溶于10ml去离子水中制成10mg/ml的储存液, 用时以0.5ug/ml的工作浓度掺入到凝胶中。
小量制备质粒DNA进行鉴定
1、用接种环从细菌冻存液(-80℃)中沾取少量菌液,点到培养皿的边缘,以其为起点直接划板于固体LB(AMP)培养皿上,37℃培养箱中(保湿)16-18小时。
2、从培养箱中取出培养皿,观察菌落的形成情况。分别挑取单个菌落接种于含6ml LB(AMP)培养液的大试管中,封口,37℃摇床(240转/分钟)培养8-12小时。
3、富集菌液,取2mL菌液加入离心管中,1000rpm,1分钟,离心。弃上清,尽量吸干。
4、用150l预冷的溶液Ⅰ将上述细菌沉淀重悬, 剧烈振荡。
5、加200l新鲜配制的溶液Ⅱ, 轻轻颠倒混匀5次,静置,使其澄清。
6、加150l预冷的溶液Ⅲ,轻轻混匀3-5分钟,使蛋白质均匀分布于水相中。
7、离心, 12000rpm 离心5min
8、小心吸取水相(约400uL)移于另一EP管中,加200uL平衡酚及200uL氯仿,混匀。
9、离心,12000rpm 3分钟。
10、取上清至另一装有1mL 无水乙醇的EP管中,来回颠倒几次,12000rpm,4℃ 离心10分钟,弃上清。
11、用70%乙醇 1mL重悬DNA(洗盐,防止以后酶切时与buffer相混)。
12、离心,12000rpm,离心3分钟,弃上清(必须吸净),37℃,室温干燥。
13、加入含RNaseA/TE 20uL, 37℃,作用6分钟。质粒DNA放置-20℃ 保存。
14、质粒DNA酶切鉴定
酶切反应体系如下:
pLXSN/TsA58 质粒DNA 10uL
Hind III 1uL
Bam H1 1uL
10× buffer K 2uL
ddH2O 6uL
离心 30秒, 37℃ 水浴 1-2小时。
15、电泳鉴定
1%琼脂糖凝胶电泳分析酶消化的DNA片段。
质粒提取试剂盒大量提取质粒
用质粒提取试剂盒(Wizard Plus Midiprepare DNA Purification System)提取。
溶解细胞:
1、取500mL锥形培养瓶,加入灭菌的液体LB细菌培养基100-200mL,按1:500的比例接种100uL小量扩增的菌液,37℃,摇床培养,200rpm/分。
2、4-5小时加氯霉素170g/ml,然后过夜(10-14小时)。
3、取过夜培养的菌液(<100ml)4℃,10,000g,10min离心细胞。倾去上清并倒置试管去除剩余液滴。[菌种保存:菌液离心后,分别加入50% SOC与50%甘油,混匀后,分装,保存于-80℃]。
4、加入3ml细胞重悬液(Cell Resuspension Solution),完全溶解菌体沉淀。
5、加入3ml细胞裂解液(Cell Lysis Solution),倒置4次混匀。细胞悬液应立即变清。如过夜培养的菌液多于50ml或菌液未立即变清,应该室温静置3-5min(勿超过5min,否则质粒会解链为单链)。
6、加入3ml中和液(Neutralization Solution)倒置4次混匀。
7、14000g,4℃,离心15min裂解的菌液,如沉淀附着不牢固,可再以同样条件离心一次。8、将上清移入一个新试管,勿吸入白色沉淀。即刻进行下一步。
纯化质粒
1、加入10ml完全混匀的纯化树脂(Wizard Midipreps DNA Purification Resin),震荡混匀。质粒与树脂结合极快,无须静置孵育。
2、立即移入Midicolumn,以真空负压抽吸(15-18inchs Hg),直至样品全部通过Midicolumn。
3、加入15ml洗柱液(Column Wash Solution)至Midicolumn中,以真空负压抽吸(15-18 inchs Hg)。重复步骤3一次。洗柱过程约需30min。
4、液体全部抽完后,继续以真空负压抽吸(15-18 inchs Hg)30sec(切勿超过30sec,以防树脂干涸),剪除并弃去Midicolumn上段容器部分(Reservoir),将Midicolumn插入一个1.5ml的EP管中,以10,000g离心2min,去除剩余的液体。
5、将Midicolumn置于一个新的1.5ml EP管中,将300ul水或TE(如果使用TE溶解质粒,将可能抑制某些酶的活性)加入Midicolumn中,静置1min,以10,000g离心20sec洗脱DNA。 弃去Midicolumn。对于大于10kb的质粒,应将水或TE预热至65-70℃以提高产量,对于大于20kb的质粒, 应将水或TE预热至80℃。一般大小的质粒可以保存在下段中长达30min,但大于20kb的质粒会出现缺刻。以10,000g离心5min,沉淀洗脱的质粒溶液中可能残留的树脂粉末,将上清转移至一个新EP管中,于4℃或-20℃保存。并用分光光度法测定DNA的含量。
细菌培养基:
1)LB液体培养基:
胰蛋白胨 10克
酵母提取物 5克
氯化钠 10克
以950ml去离子水溶解,用5M的NaOH 调pH值至7.0(约0.2ml),最后以去离子水定容至1L。高压灭菌15磅 20分钟,4℃保存。
2)LB固体选择性培养基:
LB液体培养基 1L
琼脂 15g
高压灭菌后,室温放置,待液体温度约50℃时, 加入50mg/ml的氨苄青霉素1ml,使氨苄青霉素的终浓度为50ug/ml。将培养基混匀后在超净台内分别倒入预先灭菌好的10cm2平皿铺板,培养基层2-3mm,待冷却凝固后,密封倒置于4℃保存备用。
碱裂解法提取质粒所用液体
1)溶液I:
溶菌酶 4mg
去离子水 1.4ml
500mM葡萄糖 0.2ml
100mMEDTA 0.2ml
250mMTris-HCl (pH=8.0) 0.2ml
2)溶液II:
去离子水 2.4ml
10%SDS 0.3ml
2MNaOH 0.3ml
3)溶液III:
乙酸钾 29.25g
冰醋酸 11.5ml
加去离子水至100ml
4)1M Tris-HCl缓冲液 (pH=8.0):
Tris干粉 24.24g
去离子水 191.6ml
HCl 8.4ml
5)10% SDS:
10g SDS溶于100ml 去离子水中, 于37℃水浴中使其完全溶解后室温保存。
6)5M EDTA:
取18.612克EDTA溶于50ml去离子水中, 并同时以NaOH调节pH值至8.0 (当pH值接近8.0时, EDTA才可完全溶解), 最后定容至100ml。
7)TE缓冲液 (pH=8.0):
1M Tris-HCl缓冲液 (pH=8.0) 1ml
0.5M EDTA 0.2ml
加去离子水至100ml。
8)50mg/ml氨苄青霉素:
取0.5克氨苄青霉素溶于10ml高压消毒过的去离子水中后, 用孔径为0.22nm滤膜过滤除菌。分装后, -20℃保存。
9)5mol/l LiCl:
21.20克LiCl溶于100ml去离子水中。
10)1.6 mol/l NaCl:
4.23克NaCl溶于50ml去离子水中。
11)含13%PEG8000的1.6 mol/l NaCl溶液:
6.5克PEG8000溶于1.6 mol/l NaCl (50 ml)。
12)酚:氯仿(1:1):
等体积混合Tris平衡酚和氯仿, 现用现配。
电泳系列缓冲液
1)50×TAE:
Tris碱 242g
冰醋酸 57.1ml
0.5mol/l EDTA (pH=8.0) 100ml
以去离子水定容为1L, 4℃保存。用前1:50稀释。
2)6×凝胶加样缓冲液:
0.25%溴酚蓝, 0.25%二甲苯青FF, 30%甘油水溶液, 于4℃保存。
3)溴化乙锭溶液:
将100mg溴化乙锭溶于10ml去离子水中制成10mg/ml的储存液, 用时以0.5ug/ml的工作浓度掺入到凝胶中。
小量制备质粒DNA进行鉴定
1、用接种环从细菌冻存液(-80℃)中沾取少量菌液,点到培养皿的边缘,以其为起点直接划板于固体LB(AMP)培养皿上,37℃培养箱中(保湿)16-18小时。
2、从培养箱中取出培养皿,观察菌落的形成情况。分别挑取单个菌落接种于含6ml LB(AMP)培养液的大试管中,封口,37℃摇床(240转/分钟)培养8-12小时。
3、富集菌液,取2mL菌液加入离心管中,1000rpm,1分钟,离心。弃上清,尽量吸干。
4、用150l预冷的溶液Ⅰ将上述细菌沉淀重悬, 剧烈振荡。
5、加200l新鲜配制的溶液Ⅱ, 轻轻颠倒混匀5次,静置,使其澄清。
6、加150l预冷的溶液Ⅲ,轻轻混匀3-5分钟,使蛋白质均匀分布于水相中。
7、离心, 12000rpm 离心5min
8、小心吸取水相(约400uL)移于另一EP管中,加200uL平衡酚及200uL氯仿,混匀。
9、离心,12000rpm 3分钟。
10、取上清至另一装有1mL 无水乙醇的EP管中,来回颠倒几次,12000rpm,4℃ 离心10分钟,弃上清。
11、用70%乙醇 1mL重悬DNA(洗盐,防止以后酶切时与buffer相混)。
12、离心,12000rpm,离心3分钟,弃上清(必须吸净),37℃,室温干燥。
13、加入含RNaseA/TE 20uL, 37℃,作用6分钟。质粒DNA放置-20℃ 保存。
14、质粒DNA酶切鉴定
酶切反应体系如下:
pLXSN/TsA58 质粒DNA 10uL
Hind III 1uL
Bam H1 1uL
10× buffer K 2uL
ddH2O 6uL
离心 30秒, 37℃ 水浴 1-2小时。
15、电泳鉴定
1%琼脂糖凝胶电泳分析酶消化的DNA片段。
质粒提取试剂盒大量提取质粒
用质粒提取试剂盒(Wizard Plus Midiprepare DNA Purification System)提取。
溶解细胞:
1、取500mL锥形培养瓶,加入灭菌的液体LB细菌培养基100-200mL,按1:500的比例接种100uL小量扩增的菌液,37℃,摇床培养,200rpm/分。
2、4-5小时加氯霉素170g/ml,然后过夜(10-14小时)。
3、取过夜培养的菌液(<100ml)4℃,10,000g,10min离心细胞。倾去上清并倒置试管去除剩余液滴。[菌种保存:菌液离心后,分别加入50% SOC与50%甘油,混匀后,分装,保存于-80℃]。
4、加入3ml细胞重悬液(Cell Resuspension Solution),完全溶解菌体沉淀。
5、加入3ml细胞裂解液(Cell Lysis Solution),倒置4次混匀。细胞悬液应立即变清。如过夜培养的菌液多于50ml或菌液未立即变清,应该室温静置3-5min(勿超过5min,否则质粒会解链为单链)。
6、加入3ml中和液(Neutralization Solution)倒置4次混匀。
7、14000g,4℃,离心15min裂解的菌液,如沉淀附着不牢固,可再以同样条件离心一次。8、将上清移入一个新试管,勿吸入白色沉淀。即刻进行下一步。
纯化质粒
1、加入10ml完全混匀的纯化树脂(Wizard Midipreps DNA Purification Resin),震荡混匀。质粒与树脂结合极快,无须静置孵育。
2、立即移入Midicolumn,以真空负压抽吸(15-18inchs Hg),直至样品全部通过Midicolumn。
3、加入15ml洗柱液(Column Wash Solution)至Midicolumn中,以真空负压抽吸(15-18 inchs Hg)。重复步骤3一次。洗柱过程约需30min。
4、液体全部抽完后,继续以真空负压抽吸(15-18 inchs Hg)30sec(切勿超过30sec,以防树脂干涸),剪除并弃去Midicolumn上段容器部分(Reservoir),将Midicolumn插入一个1.5ml的EP管中,以10,000g离心2min,去除剩余的液体。
5、将Midicolumn置于一个新的1.5ml EP管中,将300ul水或TE(如果使用TE溶解质粒,将可能抑制某些酶的活性)加入Midicolumn中,静置1min,以10,000g离心20sec洗脱DNA。 弃去Midicolumn。对于大于10kb的质粒,应将水或TE预热至65-70℃以提高产量,对于大于20kb的质粒, 应将水或TE预热至80℃。一般大小的质粒可以保存在下段中长达30min,但大于20kb的质粒会出现缺刻。以10,000g离心5min,沉淀洗脱的质粒溶液中可能残留的树脂粉末,将上清转移至一个新EP管中,于4℃或-20℃保存。并用分光光度法测定DNA的含量。