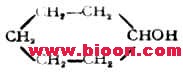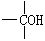醇、酚、醚-- 醇
互联网
第十四章 醇、酚、醚
醇、酚和醚都是烃含氧衍生物。
醇一般可看作是烃分子中的氢原子被羟基(-OH)取代的化合物。羟基是醇的官能团。但芳香烃苯环上的氢原子羟基取代的化合物不属于醇而属于酚。酚的官能团也是羟基。
R-h 烃R-OH 醇
Ar-H 芳香烃Ar-OH 酚
醇和酚分子中虽然都含有相同的官能团,但酚中的羟基仅限于直接连在芳香烃上,所以这种构造上的特点使酚的性质与醇不完全相同。一般把醇类的羟基称为醇式羟基,酚类的羟基称为酚式羟基。
醚是醇或酚的衍生物。它可看作是醇或酚羟基上的氢被烃基(-R‘、Ar’)取代的化合物。
R-OH 醇
Ar-OH 酚R-O-R‘醚
(Ar)(Ar`)
醇、酚和醚是重要的有机化合物。有的在医药上可用作消毒剂、麻醉剂、溶剂,有的是有机合成的常用原料。
第一节 醇
一、醇的分类
醇可根据烃基的不同、羟基所连碳原子的类型、羟基数目等三种方法进行分类。
1.根据醇分子中烃基的不同,分为饱和醇、不饱和醇、脂环醇及芳香醇等。
2.根据羟基所连接的碳原子种类不同,分为伯(1°)、仲(2°)和叔(3°)醇。
3.根据羟基数目的不同,分为一元醇、二元醇、三元醇等、含两个或两个以上羟基的醇又称为多元醇。例如:
二、醇的命名
(一)普通命名法
简单的一元醇多用普通命名法命名。通常是在醇字前面加上烃基的名称,“基”字一般可以省略。例如:
(二)系统命名法
选择连有羟基碳原子在内的最长碳链为主链,从靠近羟基的一端开始编号,根据主链碳原子数称某醇。羟基位次用阿拉伯数字表明。支链或其它取代基按“次序规则”列出。不饱和醇的命名,应选择连有羟基同时含有双键或三键碳原子在内的碳链作业主链,编号时应以羟基位次为最小。例如:
芳香醇也是按照上面的命名原则,把芳香烃当作取代基。例如:
多元醇的命名是选择包括连有尽可能我的羟基的碳链作主链,依次基数称某二醇、某三醇等。因为羟基是连在不同碳原子上的,所以当羟基数与主链碳原子数相同时可以不必标明羟基位次。例如:
三、醇的性质
(一)物理性质
低级饱和一元醇是易挥发的液体,较高级的醇为粘稠的液体,C11及C11以上的醇为蜡状固体。由于羟基的存在,醇分子间可以形成氢键,故醇随着羟基的增多,形成氢键数目增多,所以多元醇具有更高的沸点。
低级的醇如甲醇、乙醇、丙醇等均能以任何比例与水混溶,这是因为醇羟基也可与水形成氢键,结果使醇有可能在水分子间取得位置而溶入水中。当醇中的烃基链增长时,由醇的烃基部分引起的分子之间的吸引力(即范德华力)就会超过醇羟基和水间的氢键引起的吸引力。结果醇在水中的溶解度就很快随着降低。例如:在25℃的100g水中,正丁醇的溶解度为7.9g、正己醇为0.6g、正辛醇为0.5g,而癸醇则不溶于水,不溶于非极性溶剂。表14-1是饱和一元醇的物理常数。
表14-1 一些饱和一元醇的物理常数
名称 构造式 熔点/℃ 沸点/℃ 相对密度20℃ 溶解度
g・(100水)-1,,25℃ 甲醇 CH3OH -97.8 64.5 0.792 ∞ 乙醇 CH3CH2OH -117.3 78.5 0.789 ∞ 正丙醇 CH3CH2CH2OH -127 97.8 0.804 ∞ 异丙醇 (CH3)2CHOH -86 82.5 0.789 ∞ 正丁醇 CH3(CH2)2CH2OH -89.8 117.7 0.810 7.9 异丁醇 (CH3)2CHCH2OH -108 108 0.802 10.0 正戊醇 CH3(CH2)3CH2OH -78.5 137.9 0.817 2.3 正己醇 CH3(CH2)4CH2OH -52 156.5 0.819 0.6 正辛醇 CH3(CH2)6CH2OH -15 195 0.827 0.05 正癸醇 CH3(CH2)8CH2OH 6 228 0.829 正十二醇 CH3(CH2)10CH2OH 24 259 0.831 苯甲醇 C6H5CH2OH -15 205 1.046 2-苯基乙醇 C6H5CH2CH2OH -26 219 1.013 4 环己醇
25 161 0.962 5.7
(二)化学性质
醇的官能团是羟基,它由氢氧两原子组成。氧原子的电负性较大,吸电子的能力较强,所以醇分子中的C-O键和O-H键都有明显的极性。键的极性有利于异裂反应的发生,所以C-O键和O-H键都比较活泼,多数反应都发生在这两个部位。另外,由于诱导效应,与羟基邻近的碳原子上的氢也参与某些反应。
1.与碱金属的反应
醇与水相似,羟基里的氢可被活泼金属取代生成醇化物和氢氢气。例如:
2ROH+2Na→2RONa+H 2 ↑
醇钠
2CH 3 -CH 2 OH+2Na→2CH 2 CH 2 ONa+H 2 ↑
乙醇钠
醇与金属钠的反应不如水与金属反