癫痫模型制备及应用分析 (内附视频)
华联科
摘要
癫痫是一种以大脑局部病灶突发性的异常高频放电并向周围组织扩散为特征的大脑功能障碍,同时可伴随短暂的运动、感觉、意识及自主神经功能异常。在研究癫痫病理生理改变及筛选抗癫痫药物时,所选择的癫痫模型起到十分重要的作用。
癫痫的疾病模型可大致分为体外模型和整体模型。本期主要介绍:急性癫痫、慢性癫痫模型、遗传性癫痫模型以及癫痫抵抗性模型。
一、急性癫痫模型
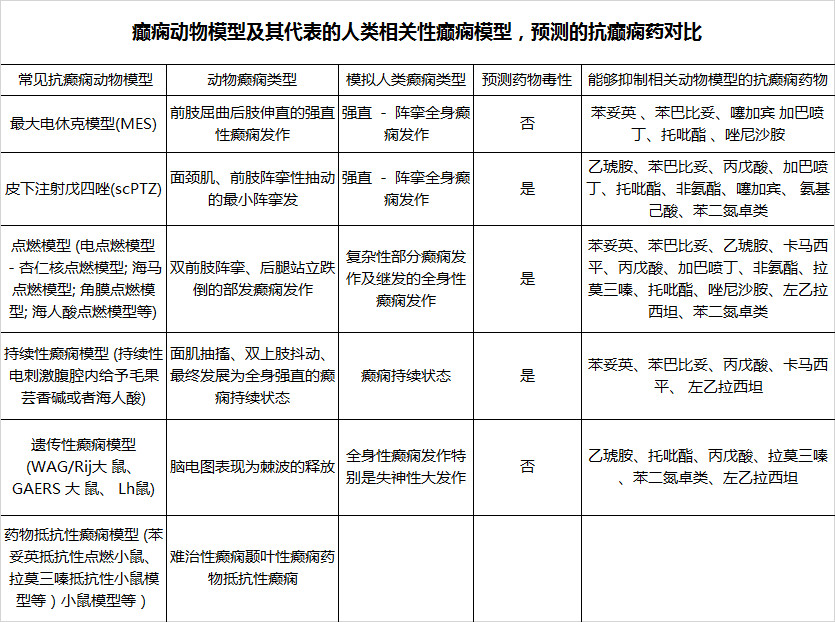
急性癫痫模型又称为痫性发作模型,常为单次处理即可诱发癫痫的一次急性发作模型。包括最大电休克模型 (maximal electroshock model,MES model) 和戊四唑癫痫模型 (Pentylenetetrazol model,PTZ model)。MES 模型是使用最多、研究最透彻的模型之一,常常用于模拟人类的强直阵挛癫痫大发作,并能用于抗强直 - 阵挛癫痫大发作的药物筛选。经典的抗癫痫药物苯妥英就是通过 MES 模型发现的。而皮下注射戊四唑 (PTZ) 癫痫模型能够模拟人类的肌阵挛癫痫全身发作,临床上使用的乙琥胺就是通过这个模型发现的。因为 MES 癫痫模型和 PTZ 癫痫模型制备方法简单,且有比较高的筛选抗癫痫化合物的效率,且成功的发现了临床有抗癫痫疗效的化合物,故在过去的几十年里 MES 模型和 PTZ 模型是作为初次筛选癫痫药物的金标准。
二、慢性癫痫模型
慢性癫痫模型与急性癫痫模型最大的不同点在于前者能够反映癫痫发作的发生、发展及其反复发作的脑部病理生理的改变,这为更深入癫痫的发生和发展提供了基础。慢性癫痫模型根据给予刺激的强度和引起的病情严重程度的不同,又可以分为点燃模型、持续性癫痫模型、自发性癫痫模型。
点燃模型 (kindling model):点燃模型是通过反复的电和化学刺激丘脑、海马等区域,从而在脑电图上表现为进行性癫痫样活动,在行为学上表现为癫痫样发作的模型。点燃模型模拟的是人类的癫痫复杂性部发作及其继发的全身性发作的癫痫动物模型,而且它能较好的模拟了癫痫进行性发展和长期反复的自限性发作的特点,如能产生脑内局限甚至广泛的病灶、降低癫痫发作的阈值、且逐渐增加癫痫发作的持续时间、加重癫痫发作的病情、最终导致自发性癫痫的发生。并且点燃模型还能够引起的丘脑、海马等区域结构和电生理的改变,从而较好地模拟了人类的颞叶性癫痫发作,为研究难治性癫痫及药物抵抗性癫痫的可能。
研究者还在点燃模型的基础上进行改进,得到诱发癫痫持续状态的癫痫动物模型,如: 持续地给予动物丘脑、海马高强度电刺激,或者腹腔内反复注射致痫剂量的胆碱能受体激动剂毛果芸香碱 (Pilocarpine)、谷氨酸受体激动剂海人酸 (kainic acid) 都能够引起癫痫持续状态的发生。但是需要注意的是诱发癫痫的持续状态有可能引起高的致死率,影响实验的观察。
因此在研究癫痫持续状态的病理生理改变时,常会给予地西泮降低其死亡率。而研究者在动物脑内埋入电极并给予持续一段时间的电刺激; 或者系统给予海人酸、毛果芸香碱等致痫药物后,都可能引起大脑的局限甚至广泛性损伤。而这种局限或者广泛性损伤有可能作为癫痫发作的病灶,从而引发慢性癫痫的自发性发作。如已有文献证明海人酸和毛果芸香碱之所以能够引起慢性癫痫的自发性发作,可能与脑内神经病理性损伤,如海马硬化症相关。
三、遗传性癫痫模型
遗传性体内模型为研究癫痫全身性发作,特别是研究癫痫失神发作提供了基础。WAG/Rij 大鼠是用于研究遗传性癫痫失神发作的大鼠,其行为学改变、脑电图 (表现为棘慢复合板波) 以及遗传特性等方面与人类癫痫失神发作极为相像,已被广泛用于研究人类癫痫失神发作。另一种遗传性模型———GAERS 大鼠行为学上表现为反复的全身非抽搐癫痫发作,并伴随双眼凝视,其脑电图表现为典型的对称同步棘波释放 (spike wave discharge,SWD)。
四、癫痫抵抗性模型
随着癫痫研究的不断发展,已使得大部分的癫痫患者的癫痫症状得到控制,但仍有 1 / 3 的癫痫患者的癫痫症状能以控制甚至表现为对药物的抵抗性,研究难治性癫痫和药物抵抗性已成为癫痫研究的新热点。其中前面提及的点燃模型也可被用药物抵抗性癫痫的研究,是因为它能够增强癫痫发作的易感性,同时能引起丘脑、海马等边缘系统的结构和电生理的改变,模拟人类的颞叶性癫痫发作,为研究难治性癫痫及药物抵抗性癫痫的提供了很好的模型。
常用 2 种点燃模型构建方法
慢性小鼠癫痫模型(PTZ 法):
1、实验动物:SPF 级 c57BL/ 6 小鼠 ,雄性 20 - 22 g。
2、建模药物:PTZ(戊四氮)sigma P6500 - 25 G
3、点燃成功标准:
每天给予 40 mg/kg 戊四氮,连续 21 天,连续三天 PTZ 腹腔注射后,均表现为 4 - 5 级发作,为点燃成功。
大鼠癫痫模型:
1、实验动物:wistar 大鼠 250 - 300 g 大鼠,雌雄兼用。
2、建模药物:
氯化锂: 阿拉丁 L116330 - 100 g
阿托品: 阿拉丁 A135946 - 1 g
匹罗卡品:西亚试剂 1012719
3、建模方法:
实验大鼠称重,腹腔注射氯化锂 150 mg/kg,18 - 20 小时后腹腔注射阿托品注射液 1 mg/kg,用以减轻匹罗卡品导致的外周胆碱能的反应,30 分钟后给予匹罗卡品 50 mg/kg 腹腔注射,空白对照组同时予以等量的生理盐水来代替氯化锂和匹罗卡品。大鼠癫痫发作达到 smialowki 分级 5 级及以上的发作并且连续发作 90 分钟后,给与 10% 水合氯醛 3~4 ml/kg 终止发作。模型成功标准:在注射完匹罗卡品 2w 后能看到发作级别在 4 级及以上的自发发作。
癫痫惊厥发作评分标准(按 smialowki 癫痫发作分级标准):
0 级,无反应;
1 级,面部运动,指鼻子、点头、奔跑;
2 级,前肢痉挛;
3 级,前肢痉挛伴后退;
4 级,前肢痉挛伴后退及摔倒发作;
5 级,摔倒、强直发作。
参考文献:
[1] LoscherW .Animal Models of Epilepsy and Epileptic Seizures[M]// AntiepilepticDrugs.Springer Berlin Heidelberg, 1999.
[2] Hernandez T .Preventing post-traumatic epilepsy after brain injury : weighing the costs andbenefits of anticonvulsant prophylaxis[J]. TIPS, 1997, 18(2):59 - 62.
[3] Marescaux C .Vergnes M. Genetic absence epilepsy in rats from Strasbourg (GAERS)[J]. Ital J NeurolSci, 1995, 16.
[4] Herzog A G .Hormonal Changes in Epilepsy[J]. Epilepsia, 1995, 36(4):323 - 326.








