假基因,真作用!余佳/张勇/石莉红合作揭示假基因的演化及其在红系发育中的作用及作用机制
丁香学术
308
背景介绍
长期以来,重复诞生新基因被认为是物种进化的主要驱动力。然而,大多数重复基因在演化过程中会积累各种功能丢失突变从而产生假基因(Pseudogene)。哺乳动物基因组中包含了数量巨大的假基因,其中大部分 (95%>) 是通过 RNA 或 DNA 水平的复制产生的。
虽然说假基因通常被认为不具有生物学功能。然而,随着技术进步,尤其是二代测序技术的突飞猛进,假基因的神秘面纱逐渐被掀开,其在肿瘤等疾病中的功能已被逐步揭示。但是,假基因在个体发育中的研究却少之又少,其在生物体正常发育中的作用更是知之甚少。
除此之外,现有研究结果表明人类特异蛋白编码基因人类特有生物学特征形成过程中发挥着重要作用,那么同样是通过重复产生的数量巨大的假基因,是否也在人类特异的生物学特征塑造中发挥重要作用呢?这一点并不为人知。
为了回答这一科学问题,2021 年 1 月 20 日,中国医学科学院基础医学研究所余佳研究组、中国科学院动物研究所张勇研究组、中国医学科学院血液病医院(血液病研究所)石莉红研究组在国际发育学著名期刊 Developmental Cell 杂志上在线发表了题为 Genome-wide analysis of pseudogenes reveals HBBP1's human-specific essentiality in erythropoiesis and implication in β-thalassemia 的研究性文章。
该研究系统性地分析了人类多种组织中假基因的表达特征,明确了假基因 HBBP1 在红细胞中特异表达,并在红细胞发育过程中发挥着关键调控作用。随后根据多个物种之间的关联比较分析,提出人类特异表达的假基因可能参与人类特异性状演化的新概念,并发现起源方式不同的假基因在作用方式上存在巨大差异,为假基因功能机制研究提供重要参考。

图片来源:Developmental Cell
研究内容
假基因 HBBP1 在人红细胞生成中的特异性功能
为了全面了解假基因的潜在功能,研究人员考虑了序列相似性后,对它们的转录组特征和基因型关联进行了分析,随后基于人类蛋白质组图谱的转录组数据集,它们进行了加权的共表达网络分析,即将具有相似表达谱的基因聚集在一起作为共表达模块。
研究发现在骨髓中富集了最多的假基因数量和比例,鉴于骨髓中存在着不同谱系的造血细胞,研究人员检测了这些假基因在每个特定谱系中的表达,发现超过一半的基因出现谱系特异性表达。
在之后的全基因组关联分析中,假基因 HBBP1 引起了研究人员的关注,因为 HBBP1 中的 3 个单核苷酸多态性(Single nucleotide polymorphism, SNP)均与人类红细胞疾病相关。
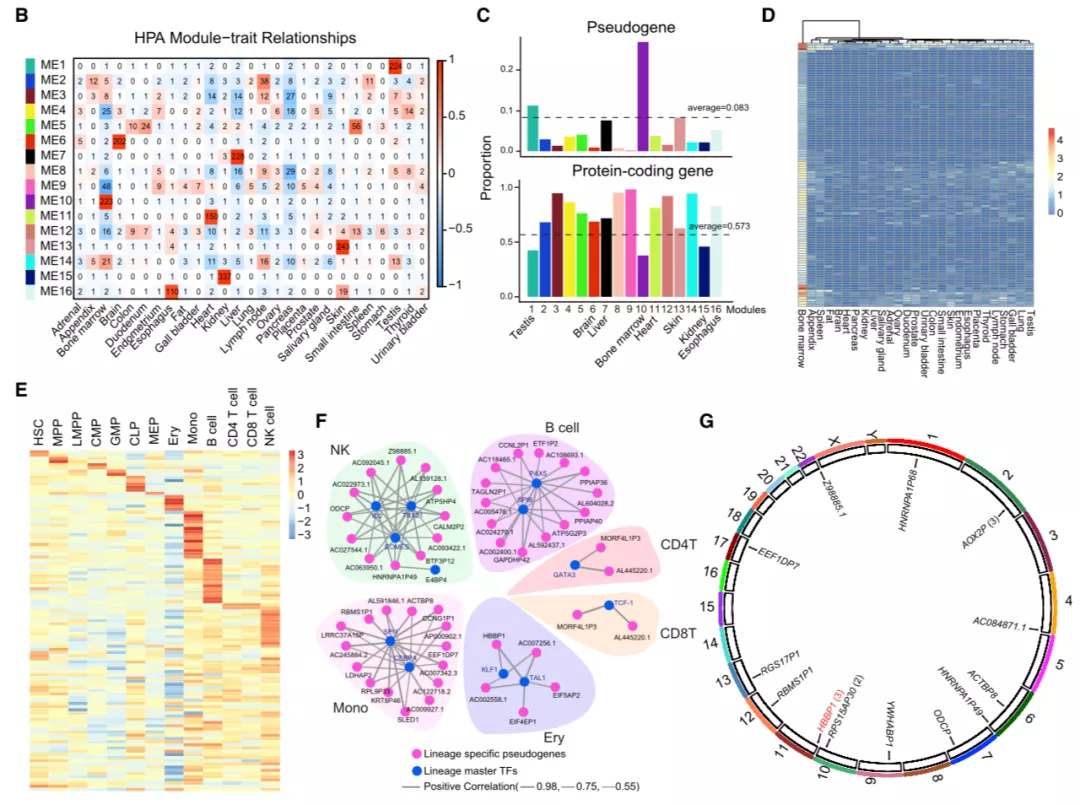
图片来源:Developmental Cell
HBBP1 于 1984 年被发现,是最早被鉴定的假基因之一,该基因位于红细胞发育分化中最为关键的功能基因簇,即 β 珠蛋白基因簇中,因此之前的研究也都围绕 HBBP1 与珠蛋白的表达及血红蛋白的形成上进行,但是 HBBP1 是否会转录,其转录本是否发挥作用以及其与疾病之间的关联等都是未知的。
基于此,研究人员首先明确了 HBBP1 特异表达于红细胞,并且会随着红细胞的分化逐渐上调其表达,但是不具备蛋白编码功能。随后,在 3 种不同的体内外红细胞诱导分化体系中的实验均证明 HBBP1 在红系发育成熟中的必要性,该基因的缺失会导致胚胎干细胞向红系分化能力的完全丧失。
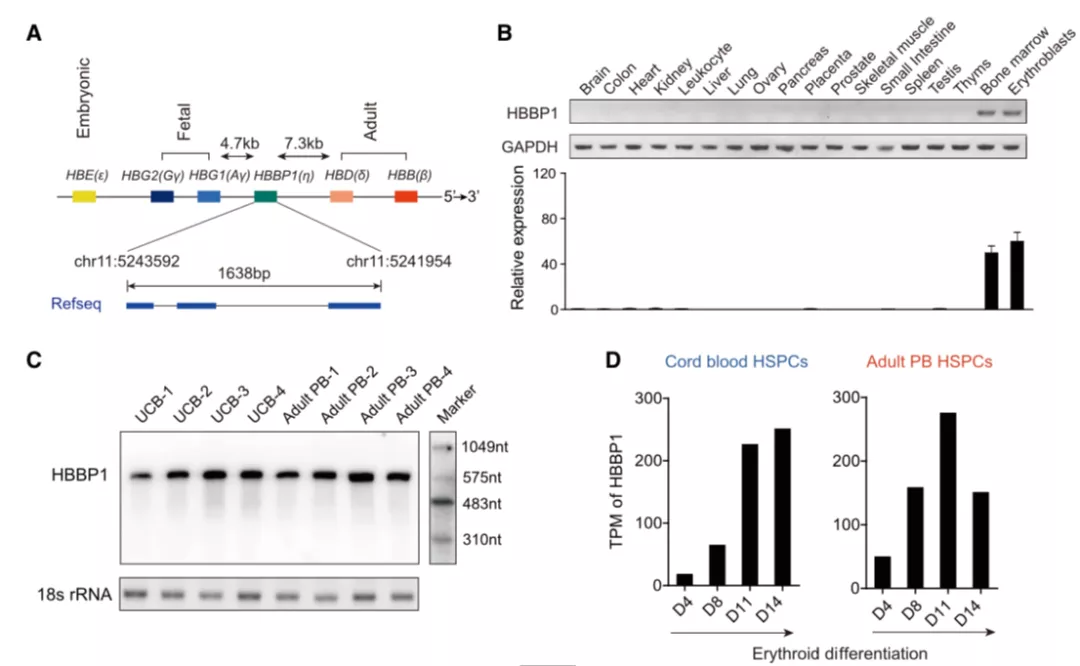
图片来源:Developmental Cell
HBBP1 通过竞争性结合 RNA 结合蛋白 HNRNPA1 稳定 TAL1 mRNA
那么 HBBP1 是通过何种机制调控红细胞的发育的呢?
他们发现 HBBP1 大量聚集在细胞质中,与 TAL1 距离较近,而 TAL1 是已知的调控红系发育的关键转录因子,进一步的实验和分析表明,HBBP1 通过与 TAL1 竞争性结合 RNA 结合蛋白(RNA binding protein, RBP)--hnRNPA1,而发挥红系的调控作用。
hnRNPA1 与 TAL1 mRNA 结合可诱导后者降解,削弱其调控红系发育的功能,但是 HBBP1 的存在则会与 hnRNPA1 竞争性结合,进而释放了 TAL1 mRNA,提高了后者的稳定性,以此维持红细胞的正常分化。
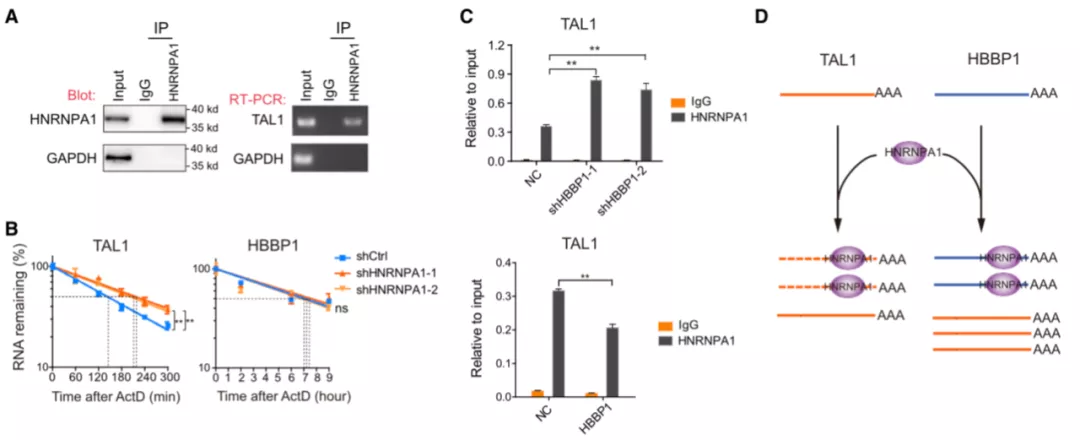
图片来源:Developmental Cell
上述的研究结果表明,在生理条件下,HBBP1 通过提高 TAL1 的稳定性而发挥红系调控功能,那么其在病理条件下,尤其是在血红蛋白疾病中是否仍然扮演着重要的角色呢?
为此,研究人员对 HBBP1 在 β- 地中海贫血患者中的作用进行了探索。结果发现,HBBP1 在 β- 地中海贫血患者中会代偿性升高,通过促进 TAL1 的表达参与患者体内 HbF 活化及贫血症状的缓解。HBBP1 与 HbF 的表达水平呈显著正相关,这也解释了 HBBP1 SNP 与血红蛋白疾病症状关联的现象。
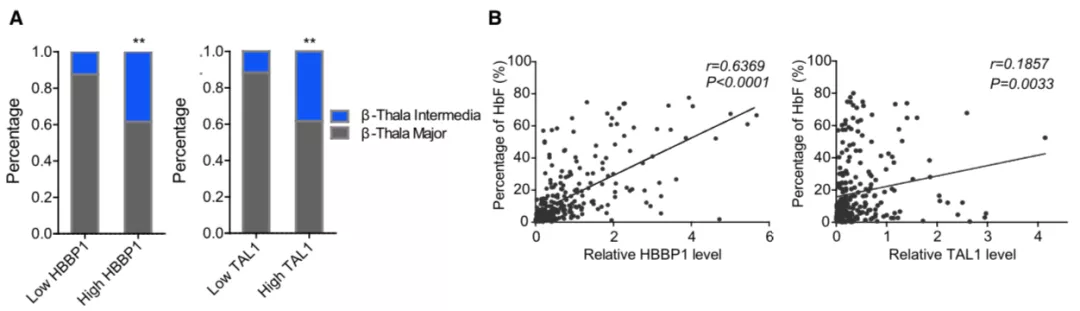
图片来源:Developmental Cell
HBBP1 的进化角色
综合以上实验结果发现,HBBP1 并不直接调控珠蛋白基因簇成员表达,而是通过与 hnRNPA1 结合而间接发挥红系调控功能。那么假基因 HBBP1 在进化上又反映着怎样的现象呢?
为此研究人员对假基因 HBBP1 的进化及在多物种中的表达进行了分析,结果发现,HBBP1 虽然通过重复起源于哺乳动物的祖先,显然是一个古老的假基因,但是,在进化过程中,其在获得结合位点序列后的物种演化中却呈现出复杂的多样性,具体表现为:在偶蹄类不同物种中分别作为蛋白编码基因和假基因;在啮齿类等中发生了丢失;在大多数灵长类中作为不表达的假基因、且在恒河猴中再次丢失结合位点,仅在人红细胞中获得了大量表达,并参与到了 TAL1-hnRNPA1 调控网络中,发挥关键的调控功能。

图片来源:Developmental Cell
综上所述,该研究首次在全基因组水平探索了假基因的表达特征,以及其与疾病的关联分析,并解释了其发挥生物学调控功能的内在分子机制,最后在进化生物学上探究了 HBBP1 的来龙去脉。
因此,该研究系统阐释了一个假基因从产生到消亡,并再次获得新生,并发挥物种特异调控功能的全过程,从而提出假基因参与塑造人类特异的生物学特征这一新概念,为未来假基因的研究提供了重要参考,同时该工作也使我们得以窥见自然选择、物种进化的精彩动态。

图片来源:Developmental Cell
美国纽约血液中心膜生物学实验室主任安秀丽教授提到:「该研究充分体现了学科交叉的优势,不仅发现了假基因 HBBP1 对红细胞发育的必需功能也揭示了其在血红蛋白疾病中的保护作用,还发现了假基因 HBBP1 新的调控机理并解析了其功能的起源过程。」
著名进化基因组学研究科学家,西北工业大学王文教授评价道:「整体来看,该研究整合进化基因组学、进化发育生物学和分子生物学手段,通过假基因这一独特视角,围绕着基因型 - 表型映射关系这一基础问题所带来的一系列发现有其概念创新性,是值得一读的佳作。」
据悉,中国医学科学院基础医学研究所副研究员马艳妮、博士刘思琪,中国医学科学院血液病医院助理研究员高洁,中科院动物所博士陈春燕,汕头大学医学院第一附属医院张昕研究员为该研究论文的第一作者。余佳研究员、张勇研究员、石莉红研究员、马艳妮副研究员为该论文的通讯作者。
参考文献:
1、Ma et al., Genome-wide analysis of pseudogenes reveals HBBP1’s human-specific essentiality in erythropoiesis and implication in b-thalassemia, Developmental Cell (2020)
2、Bray, N.L., Pimentel, H., Melsted, P., and Pachter, L. (2016). Near-optimal probabilistic RNA-seq quantification. Nat. Biotechnol. 34, 525–527.
3、Jacq, C., Miller, J.R., and Brownlee, G.G. (1977). A pseudogene structure in 5S DNA of Xenopus laevis. Cell 12, 109–120.



![[JL43707] 犬唾液酸结合免疫球蛋白样凝集素12(基因和假基因)(SIGLEC12)ELISA试剂盒](https://img1.dxycdn.com/2018/0109/785/3254426312274143674-14.jpg!wh200)