Nature Medicine 重磅:40 年前开始失明,一招光遗传学疗法重获光明!
丁香学术
770
「如果我能看得见,就能轻易分辨白天黑夜,…., 如果我能看得见,生命也许完全不同。」
无论是广为传唱的《你是的我眼》,还是海伦凯勒感人肺腑的《假如给我三天光明》
对于盲人,总是有太多的「如果」。
各种各样的眼部疾病,导致了全球数亿人视力受损,以及接近 5000 万的全盲人口。对于普通人再也正常不过的多彩世界,成为了这些人永远的遗憾。
如何解决日益严重视力损害问题,也成为了全球医药行业的重要议题。

图片来源:Nature Medicine
2021 年 5 月 24 日,来自瑞士巴塞尔大学的 Botond Roska 教授联合匹兹堡大学 José-Alain Sahel 教授在 Nature Medicine 发表了题为 Partial recovery of visual function in a blind patient after optogenetic therapy 的临床研究 [1], 报道了他们如何利用光遗传技术,让一名已经失明四十年的视网膜色素变性 (retinitis pigmentosa, RP) 患者重新获得了部分视觉功能,为视网膜色素变性的治疗翻开了新的篇章。
研究内容:
作为一种遗传性眼科疾病,视网膜色素变性(RP)在全球范围内影响着两百万人。患者一般会在童年时发病,病情会随着年龄的增长逐渐恶化,最终可导致失明。
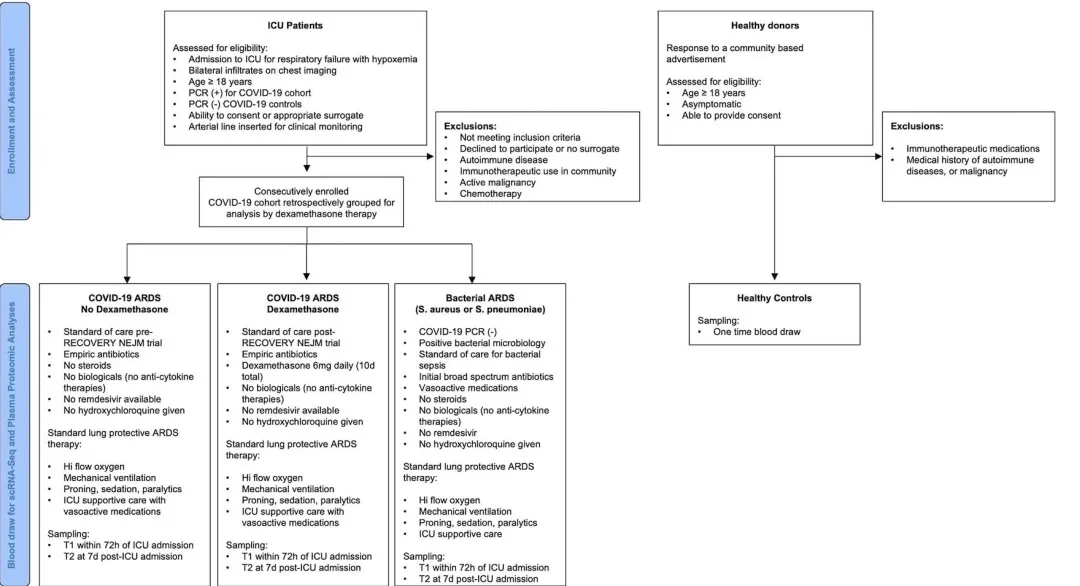
为了解决这个问题,并为其他眼部病变开拓新的治疗思路。研究团队于 2017 年开始了一项名为 PIONEER 的开放标签 1/2a 期临床试验,旨在使用一种光遗传学与光刺激护目镜联合疗法治疗 RP。
入组人员中,有一位 58 岁的 RP 患者,在接受光遗传疗法之前,他的一侧眼睛已看不清任何物体。作为光遗传治疗的一部分,研究人员向双眼中视力更糟糕的一只注射了搭载有感光蛋白 ChrimsonR 的腺病毒相关载体,并使其带上了能够将真实视觉世界中图像转换为 ChrimsonR 能够感受的 590nm 琥珀色光的护目镜。当 ChrimsonR 接收到护目镜传递而来的琥珀色光时,就能将实时的视觉信号传递到视网膜。
图片来源:Nature Medicine
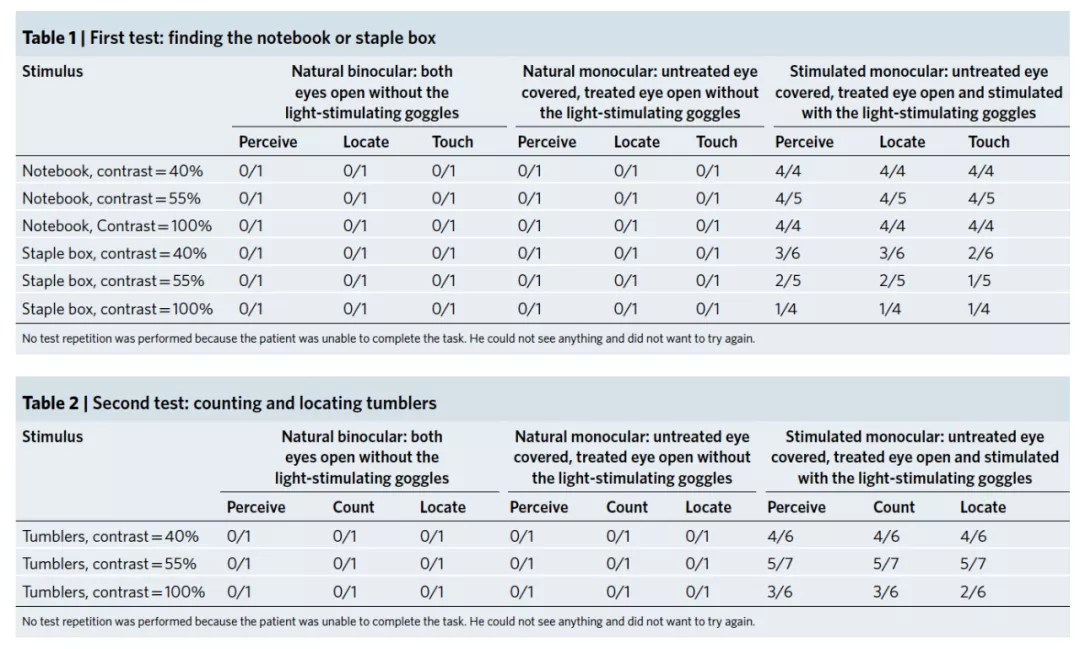
通过对比治疗前与治疗后 15 次的视力检测结果,研究人员发现与没有治疗的眼睛,以及没有佩戴光转化护目镜的情况相比,接受治疗的眼睛在佩戴特制护目镜的时候表现出了显著的改善。接受治疗的眼睛能够有效帮助受试者感知、定位与触碰前方 40 厘米除不同对比度的笔记本与订书钉盒,准确率整体超过 50%。在患者适应这套设备的使用方法后,患者还能够数出眼前杯子的数量。对于一个失明四十年的人来说,这是非常鼓舞人心的「能力」。
在安全性方面,研究人员对受试者眼睛与全身身体状况进行了持续性的跟踪。首先,患者眼睛中并未出现由于注射搭载 ChrimsonR 的腺病毒相关载体导致的炎症现象;视网膜也没有出现解剖学上的病变。在持续性的随访中,研究人员也没发现其他形式的副作用。整体而言,研究人员还未观测到这套治疗方法的安全性风险。

图片来源:Nature Medicine
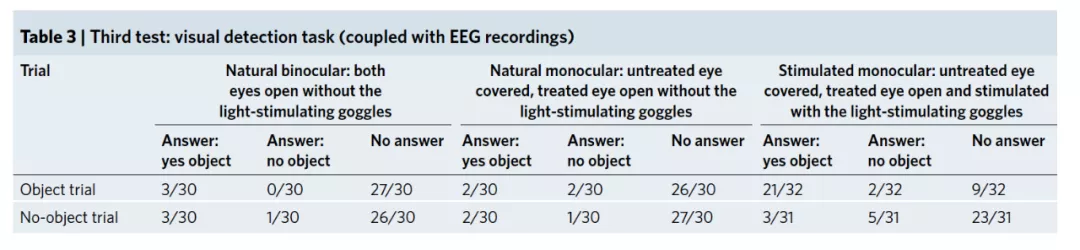
在完成了感知与数杯子数量的两项测试后,研究人员对受试者进行了脑电图测试,以探究患者视觉感受与大脑活动之间的联系。
图片来源:Nature Medicine
如果不佩戴护目镜,受试者大脑根本无法区分出前方有没有物品,大脑对前方物品的响应率极低。但当佩戴上护目镜,张开接受治疗的眼睛之后。一旦受试者视野中出现了物品,其大脑将有更高的概率针对物品产生相应的脑电波。这都证明这套疗法成功将部分视觉信号传入了大脑。
图片来源:Nature Medicine
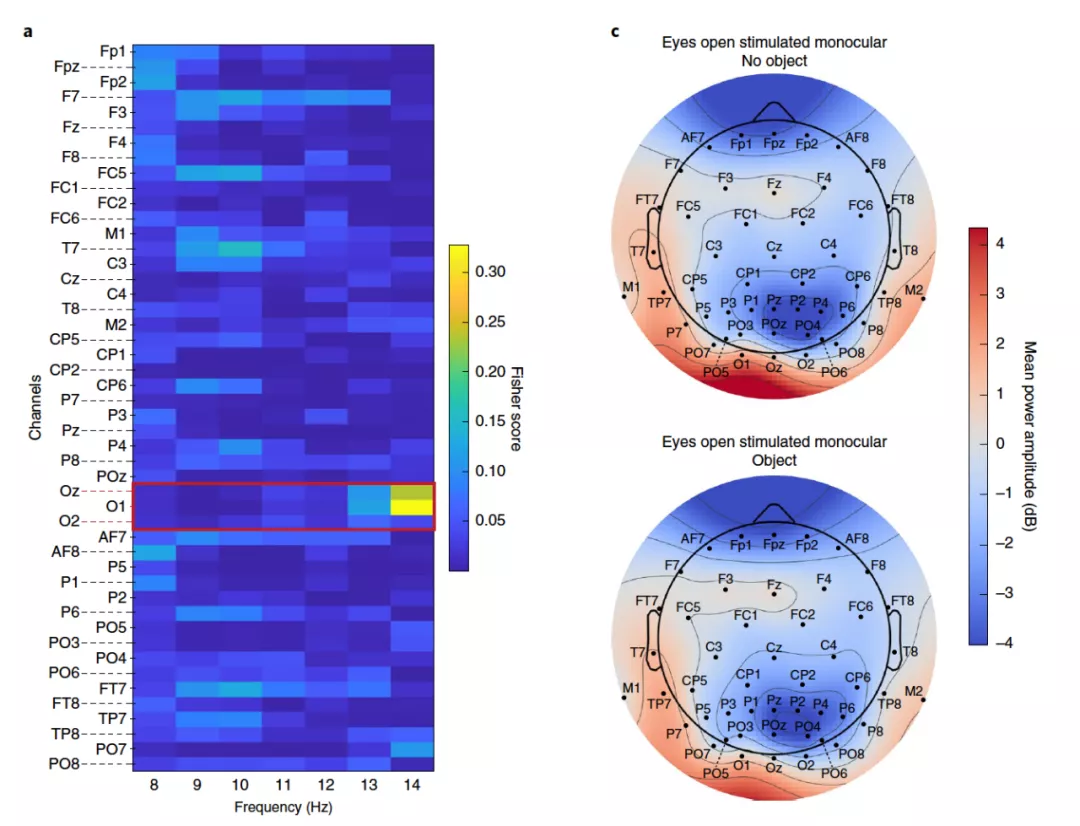
在患者佩戴护目镜的情况下,作者进一步探究了受试者的大脑活动。
通过脑电波的频谱分析,研究团队发现 48 个脑电波频道中的 O1 与 Oz 与视线内物品的出现关系最为紧密。在睁眼受刺激的状态下,研究团队训练出来的解码器准确度出现了显著的提高,远高于随机水平。而 O1 与 Oz 对应的正好是负责处理视觉信号的枕叶皮质区。这些数据再次证明了,研究团队的治疗方法能有效恢复受试者的视觉能力。
研究意义:
该研究是全球首个在人体证明光遗传学与光激活护目镜的联合使用,可以使因视网膜色素变性丧失绝大部分视力的患者部分恢复视觉的临床探索,并呈现出了令人振奋的结果。
虽然目前的疗效与安全性数据仅仅是基于这位失明四十年的患者,但我们很期待看到更大规模临床实验的数据。该疗法如果能真正投入使用,将给全球 200 万 RP 患者的生活带来全新的可能。
延伸阅读:
本文的两位通讯作者 Botond Roska 与 José-Alain Sahel 是视力再生领域的执牛耳者。他们的研究尝试使用多种不同的策略恢复患者的视力,光遗传学疗法只是他们研究领域中的方向之一,全球视力障碍患者对他们的研究寄予了厚望。

图片来源:Nature Neuroscience
2019 年,Botond Roska 团队在 Nature Neuroscience 发表了题为 Targeting neuronal and glial cell types with synthetic promoter AAVs in mice, non-human primates and humans 的研究 [2], 识别出了多种能够用于非人灵长类动物以及人类视网膜基因治疗的腺病毒相关载体,为眼部疾病基因治疗的进一步推广扫清了障碍。

图片来源:Science
除了基因疗法,Botond Roska 团队也尝试使用纳米红外传感器帮助眼睛重新感受光线,并以此恢复视力。相关研究 2020 年以 Restoring light sensitivity using tunable near-infrared sensors 为题刊登在 Science 之上 [3]。
图片来源:Nature

图片来源:Science Translational Medicine
对于「治疗失明」最新进展感兴趣的小伙伴,也可以阅读 Botond Roska 与 José-Alain Sahel 于 2018 年发表在 Nature 上题为 Restoring Vision 的重量级综述 [4]。以及 2019 年发表在 Science Translational Medicine 的综述 Depicting brighter possibilities for treating blindness[5]。
希望在不久的将来,海伦凯勒以及数千万失明患者的梦想都能照进现实。
三句话读懂一篇 CNS:好奇心的发生机制,意念打字速度接近手机打字,古代粪便揭示肠道微生物信息...
参考文献
1.Sahel, J.-A., etal., Partial recovery of visual function in a blind patient after optogenetic therapy. Nat Med, 2021.
2.Jüttner, J., et al., Targeting neuronal and glial cell types with synthetic promoter AAVs in mice, non-human primates and humans. Nature Neuroscience, 2019. 22(8): p. 1345-1356.
3.Nelidova, D., et al., Restoring light sensitivity using tunable near-infrared sensors. Science, 2020. 368(6495): p. 1108.
4.Roska, B. and J.-A. Sahel, Restoring vision. Nature, 2018. 557(7705): p. 359-367.
5.Sahel, J.-A., J. Bennett, and B. Roska, Depicting brighter possibilities for treating blindness. Science Translational Medicine, 2019. 11(494): p. eaax2324.