基因工程的克隆载体
丁香园论坛
4691
基因工程所用的克隆载体常称之为分子克隆载体(molecular cloning vector),它是一类可供外源DNA插入并携带重组DNA分子进入适当宿主细胞的DNA分子。如果打一个十分浅显的比喻,分子克隆载体犹如航天技术中的运载火箭,外源DNA分子就如火箭上搭载的卫星,宿主细胞则如外部深邃的空间。分子克隆载体的主要功能就是将外源基因携带入宿主细胞,并在宿主细胞中进行DNA扩增和使外源基因得以高效表达。在这一点上又与火箭不一样,因为火箭在运载卫星的过程中分级脱落和烧毁。
尽管克隆载体是由DNA分子所构成,但与宿主细胞的染色体DNA分子相比,它们一般都比较小。比如常用的质粒载体多数都在10 kb以下,而常用的噬菌体载体,一般都在20 kb左右。我们知道,大肠杆菌的染色体DNA是4200kb。正是由于克隆载体的分子量比较小,在操作过程中不会造成载体DNA分子的断裂,而大分子的DNA容易在操作中发生断裂。
克隆载体的基本结构和功能
在短短的20年间,用于不同生物和不同目的的分子克隆载体至少也有好几千种,那么它们应该有些什么样的基本结构呢?经过仔细分析发现,所有的分子克隆载体都具备了以下3个最基本的结构:
1) 至少有一个复制起点,因而至少可在一种生物体中自主复制;
2) 至少应有一个克隆位点,以供外源DNA插入;
3) 至少应有一个遗传标记基因,以指示载体或重组DNA分子是 否进入宿主细胞。
既然说每一个载体至少应有一个复制起点,一个克隆位点和一个标记基因,那么一个载体可否有多个复制起点,多个克隆位点和多个标记基因呢?答案是肯定的。不过,我们还是先看看载体中的三个基本结构
克隆载体的复制起点
由于DNA的复制是始于复制起点的,因此只要一个DNA分子有了复制起点,那么这个DNA分子就可以自主复制。如果一个分子克隆载体有了复制起点,那么该载体就可以在某种生物的细胞中自主复制,因此这个载体就可以多拷贝地存在于某种细胞内。多拷贝DNA有两个好处:一是可以用于大量制备克隆载体DNA分子,以利于外源基因的克隆,这样可大大减少工作量;二是如果载体中插入了外源基因,那么外源基因的拷贝数也就大量增加了,这就有利于大量地表达外源基因,从而获得大量的基因表达产物,这也正是基因工程的目的之一。
如果一个载体有两个或两个以上的复制起点,那么这个载体会有什么不一样?有两种情况:一是两个复制起点适用的宿主细胞不一样,比如说,一个复制起点适合于大肠杆菌,因为大肠杆菌是基因工程中使用频率最高的宿主菌,另一个复制起点适合于另一种细菌或真核生物细胞,那么这种克隆载体常称之为穿梭载体(shuttle vector),换言之,穿梭载体可在两种生物内进行来回的穿梭;另一种情况是同一个载体中的两个复制起点都是适合于一种细胞的,只不过这两个复制起点分别是在一定遗传背景条件下起作用,这种类型的载体多数是属于大肠杆菌的载体。
克隆载体的克隆位点
分子克隆载体的目的就是要将外源基因通过体外重组,形成重组DNA分子,然后再转移到某种宿主细胞内,那么克隆载体就应该有一个位点供外源DNA插入,这个位点就是克隆位点。克隆位点一定是一个限制酶切位点,而且必须是由6个核苷酸或6个核苷酸以上的序列组成的限制酶识别位点。虽然克隆位点是限制酶识别位点,但不是载体上所有限制酶位点都能作为克隆位点。一般说来,载体中的克隆位点必须是唯一的,即同一种限制酶识别位点在一个载体中只能有一个。由于不同基因的末端可以由不同的限制酶所产生,因而为了减少分子克隆的工作量,科学家们构建了具有多个克隆位点的载体,而且将多个克隆位点集中在一个很短的序列内,这种序列常常被称之为多克隆位点区(multiple cloning site)。有关多克隆位点区的详细情况见后述。
克隆载体的标记基因
当试图把一个载体DNA或重组DNA分子导入某种宿主细胞时,我们如何知道载体或重组DNA分子已经进入了宿主细胞?标记基因就能起到这个作用。获得了外源DNA分子进入的细胞被称之为转化细胞。标记基因往往可以赋予宿主细胞一种新的表型,这种转化细胞可明显地区别于非转化细胞:转化细胞有了新的表型,而非转化细胞仍保持原有的表型。这种表型的区别往往是选择性的,即只有转化细胞才能在研究者提供的生长条件下生长,而那些没有载体DNA分子进入的细胞就不能在相同的生长条件下生长,因此,转化细胞和非转化细胞是十分容易区别开来的(详见下述)。这是标记基因最重要的功能,即指示哪些细胞是转化细胞。
标记基因还有一个十分重要的功能,即指示外源DNA分子是否插入载体分子形成了重组子。换句话说,当我们把一个DNA片段插入到某一个标记基因内时,该基因就失去了相应的功能。当把这种重组DNA分子转到宿主细胞后,该基因原来赋予的表型也就消失了。要是仍保留了原来表型的转化细胞,细胞内含有的DNA分子一定不是重组子。很显然,既要指示外源DNA是否进入了宿主细胞,又要指示载体DNA分子中是否插入了外源DNA片段,那么这种载体必须至少具有两个标记基因。
上述的标记基因是针对一种生物而言的,那么当载体可用于多种生物时,一个载体就可以有多个标记基因,每个标记基因的用途是不相同的,不同的标记基因可能只适合于某种生物。比如植物的克隆载体就可能有3-4个标记基因。由于绝大多数标记基因都是分离自原核生物,因而这些标记基因要用于其它生物,还得对这些基因进行改造,即将基因的启动子和终止子换成另一种生物的基因启动子和终止子。
遗传标记基因的种类
现有的标记基因的种类很多,但可以将它们划分为以下三大类:
1)抗性标记基因。这类抗性基因可赋予宿主细胞对些物质的抗性,而这些物质对宿主细胞可能是致死的,因此,这类标记基因可直接用于选择转化子。这类基因又可分为以下3类:
i. 抗生素抗性基因。这类抗性基因常常赋予宿主细胞对抗生素产生抗性,而抗生素往往对宿主细胞是致死的,这类标记基因中常用的基因有:氨苄青霉素抗性基因(Apr)、四环素抗性基因(Tcr)、氯霉素抗性基因(Cm r)、卡那霉素抗性基因(Kanr)、G418抗性基因(G418r)、潮霉素抗性基因(Hygr)、新霉素抗性基因(Neor)。
ii. 重金属抗性基因。重金属对生物细胞是有毒的,但有的基因能产生一些可与重金属相结合的蛋白质,从而从环境中除去重金属。目前所用的重金属抗性基因有:铜抗性基因(Cur),锌抗性基因(Znr),镉抗性基因(Cdr)。
iii. 代谢抗性基因。抗除草剂基因,胸苷激酶基因(TK)。
在上述三种抗性标记基因中,抗生素抗性基因使用最为频繁,且适用范围很广,包括动物、植物和微生物。抗除草剂基因在植物中使用较为广泛。
2)营养标记基因。有的生物细胞因为突变而导致需要某些营养物质才能生长,其原因是参与某些营养物质合成的基因发生了突变。如果将没有发生突变的相应基因转入这种突变体细胞中,那么这些细胞就不再需要相应的营养物质,而那些未被转化的细胞则不能生长,因而这类标记基因也可直接用于选择转化子。
这类基因主要是参与氨基酸,核苷酸及其他必需营养物合成酶类的基因,在酵母转化中使用最频繁,如色氨酸合成酶基因(TRP1),尿嘧啶合成酶基因(URA3),亮氨酸合成酶基因(LEU2),组氨酸合成酶基因(HIS4)等。
3) 生化标记基因。这类标记基因的表达产物可催化某些易检测的生化反应,常用的基因有β-半乳苷酶基因(lacZ)、葡萄糖苷酸酶基因(GUS)、氯霉素乙酰转移酶基因(CAT)。
为了进一步说明载体的结构和各个结构的功能,下面举一个在基因工程中使用比较频繁的大肠杆菌载体—pBR322作为例子。
大肠杆菌载体pBR322
载体pBR322是由Bolivar 等人于1977年构建的。该载体长4362 bp,它有一个来自大肠杆菌中高拷贝天然质粒的复制起点(ori),这个复制起点可使pBR322在大肠杆菌中的拷贝数达到20个,因而pBR322载体的DNA很容易从大肠杆菌中提取出来。这是pBR322中的第一个结构特征。
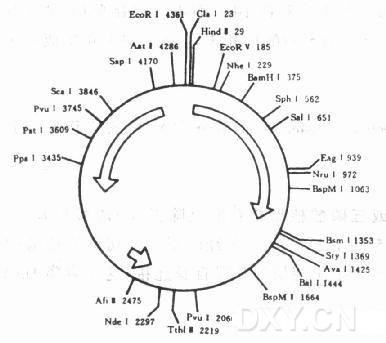
图1 大肠杆菌克隆载体pBR322的物理图谱
此载体中有两个标记基因,一个是氨苄青霉素抗性基因(Apr),另一个是四环素抗性基因(Tcr)。氨苄青霉素和四环素都是人类治疗疾病的抗生素药物。当把pBR322 DNA转化大肠杆菌细胞,其中部分细胞就被该载体所转化,而有一部分细胞则没有被转化。如何区分这两种细胞呢?很简单,将转化后的细胞涂布在一种加有氨苄青霉素或四环素的培养基上,然后放在37° C下培养。由于转化细胞中有pBR322 DNA,该载体上的氨苄青霉素抗性基因和四环素抗性基因都会表达,那么这种转化细胞就能在加有氨苄青霉素或四环素的培养基上生长,于是就可以在培养基的表面看到相应的抗性菌落。菌落是由许多大肠杆菌细胞生长后堆积在一起,能为肉眼可见的生长物。那些没有被转化的细胞,因为细胞中没有pBR322,当然就没有两种抗性基因的表达,那么这些细胞就不能在加有氨苄青霉素或四环素的培养基上生长,因此我们也就无法获得未转化细胞的菌落。这样就很简单地将转化的细胞与非转化的细胞区别开来了。
现在再来看看pBR322的克隆位点。在这个载体中,ScaI、PstI、BamHI、SalI、 EcoRI和HindIII等6个限制酶位点都是唯一的,因此它们都可以用作克隆外源基因的位点。但是,在克隆外源基因的时候,选择不同的克隆位点将会获得不同的表型,筛选重组子的策略也是不相同的。究竟有何不同?
ScaI和PstI两个位点都位于氨苄青霉素抗性基因的编码区内。当一个外源基因片段插入这两个位点中的任何一个位点时,该抗性基因就会失去活性,这种重组子就再也不会赋予转化细胞以氨苄青霉素抗性,因此,这种重组子所转化的细胞就只能涂布在加有四环素的平板上。因为四环素抗性基因没有外源DNA插入,因此仍保留了生物学活性。
要是不把外源基因插入Apr基因中,而是将其插入Tcr基因中,结果会怎样?已知四环素抗性基因中有BamHI和SalI两个克隆位点,如果其中一个位点插入了外源基因片段,那么四环素抗性基因也就失去了活性,因此当把这种重组DNA分子转化大肠杆菌细胞,转化细胞就不能在四环素平板上生长,换句话说,这种转化细胞则只能涂布在加有氨苄青霉素的平板上。
另外还有两个位点EcoRI和HindIII,它们不在两种抗生素抗性基因的编码区内,因此外源基因插入这两个位点时不会引起标记基因的失活,所以转化细胞可以涂布在氨苄青霉素或四环素的平板上。由此可以看出,克隆位点不仅仅是供外源DNA分子插入的地方,而且将直接影响到后面的实验操作。
通过上面的叙述,我们已经知道基因工程的克隆载体中的三种基本结构和它们的功能。实际上,载体会因为在使用时的宿主细胞种类、实验用途不同而有较大差别,但这三种基本结构是最基本的。
克隆载体的种类
自1977年Bolivar等人组建了第一个系列的克隆载体pBR以来,已建立起各种不同的分子克隆载体用于不同的研究目的和不同的生物种类。
如果按照载体的复制子来源划分,所有的载体可分为以下三种类型:
1) 质粒型载体:这一类载体所含的复制起点主要来自不同的原核生物,特别是大肠杆菌和一些低等真核生物(如酵母菌和一些丝状真菌)中的质粒DNA。有的复制起点则来自染色体DNA(如酵母菌)。许多载体DNA上只含有一种复制起点,如用于大肠杆菌的pBR和pUC系列质粒载体,然而有的克隆载体却含有两种复制子顺序,它们常来自于不同的生物,比如大肠杆菌-酿酒酵母(Saccharomyces cerevisiae)穿梭载体YRp12 和YEp13等,这类载体能在这两种不同的生物中自主复制。
2) 病毒型载体:这类载体中所含的复制起点是来自病毒DNA。在大肠杆菌中,以噬菌体λ所组建的charon系列,λEMBL和λNM系列载体和以单链DNA噬菌体M13组建的M13mp系列载体。在动物细胞中,也有好几种病毒复制被用来组建克隆载体。
3) 混合型载体:这类载体复制起点来自质粒和病毒,比如适合于大肠杆菌的DNA载体pEMBL8和pEMBL9含有质粒pMB1和单链噬菌体f1复制起点。 用于动物细胞的DNA载体则含有大肠杆菌的质粒复制和动物病毒复制起点。 使用得最广泛的动物病毒复制起点来源子SV40。实际上,这类混合型载体也是穿梭型的,即它们既可以在大肠杆菌中复制,亦可在动物细胞中复制。
要是按照克隆载体的功能或用途来划分,则可将DNA载体分为以下两大类:
1) 普通型载体:这类载体主要用于各种基因组文库和cDNA文库的建立, 比如常用的pBR322,由λ衍生的载体和COs质粒,以及一些大肠杆菌- 酿酒酵母穿梭载体, 如YRp7,YEp13等。染色体DNA片段或cDNA均可用这类载体进行增殖。它们通常含有两个或两个以上的标记基因,其中一个基因用于选择转化体(transformant),另一基因则是用于检查载体中是否有外源DNA插入。
2) 表达型基因(expression vector):这类载体主要用于研究基因的表达或是用于大量生产一些有用的转录产物或蛋白质,有的也可用于cDNA文库的建立。这类载体除具有普通型载体的特征外,它还含有某些基因的启动子序列,有的还含有转录终止子序列,为了基因表达产物便于检测或是为了简化基因表达产物的分离纯化,有的表达型载体除含有基因启动子序列外,它还有一段为信号肽链编码的DNA序列,这段信号肽链可以使蛋白质分必到细胞外。 这类载体又可称为分泌表达型载体(Secretion expression vector)。为了使某些基因产物能投入大规模的工业生产,科学家们已组建了各种高效表达的分泌型载体。
图1 大肠杆菌克隆载体pBR322的物理图谱

尽管克隆载体是由DNA分子所构成,但与宿主细胞的染色体DNA分子相比,它们一般都比较小。比如常用的质粒载体多数都在10 kb以下,而常用的噬菌体载体,一般都在20 kb左右。我们知道,大肠杆菌的染色体DNA是4200kb。正是由于克隆载体的分子量比较小,在操作过程中不会造成载体DNA分子的断裂,而大分子的DNA容易在操作中发生断裂。
克隆载体的基本结构和功能
在短短的20年间,用于不同生物和不同目的的分子克隆载体至少也有好几千种,那么它们应该有些什么样的基本结构呢?经过仔细分析发现,所有的分子克隆载体都具备了以下3个最基本的结构:
1) 至少有一个复制起点,因而至少可在一种生物体中自主复制;
2) 至少应有一个克隆位点,以供外源DNA插入;
3) 至少应有一个遗传标记基因,以指示载体或重组DNA分子是 否进入宿主细胞。
既然说每一个载体至少应有一个复制起点,一个克隆位点和一个标记基因,那么一个载体可否有多个复制起点,多个克隆位点和多个标记基因呢?答案是肯定的。不过,我们还是先看看载体中的三个基本结构
克隆载体的复制起点
由于DNA的复制是始于复制起点的,因此只要一个DNA分子有了复制起点,那么这个DNA分子就可以自主复制。如果一个分子克隆载体有了复制起点,那么该载体就可以在某种生物的细胞中自主复制,因此这个载体就可以多拷贝地存在于某种细胞内。多拷贝DNA有两个好处:一是可以用于大量制备克隆载体DNA分子,以利于外源基因的克隆,这样可大大减少工作量;二是如果载体中插入了外源基因,那么外源基因的拷贝数也就大量增加了,这就有利于大量地表达外源基因,从而获得大量的基因表达产物,这也正是基因工程的目的之一。
如果一个载体有两个或两个以上的复制起点,那么这个载体会有什么不一样?有两种情况:一是两个复制起点适用的宿主细胞不一样,比如说,一个复制起点适合于大肠杆菌,因为大肠杆菌是基因工程中使用频率最高的宿主菌,另一个复制起点适合于另一种细菌或真核生物细胞,那么这种克隆载体常称之为穿梭载体(shuttle vector),换言之,穿梭载体可在两种生物内进行来回的穿梭;另一种情况是同一个载体中的两个复制起点都是适合于一种细胞的,只不过这两个复制起点分别是在一定遗传背景条件下起作用,这种类型的载体多数是属于大肠杆菌的载体。
克隆载体的克隆位点
分子克隆载体的目的就是要将外源基因通过体外重组,形成重组DNA分子,然后再转移到某种宿主细胞内,那么克隆载体就应该有一个位点供外源DNA插入,这个位点就是克隆位点。克隆位点一定是一个限制酶切位点,而且必须是由6个核苷酸或6个核苷酸以上的序列组成的限制酶识别位点。虽然克隆位点是限制酶识别位点,但不是载体上所有限制酶位点都能作为克隆位点。一般说来,载体中的克隆位点必须是唯一的,即同一种限制酶识别位点在一个载体中只能有一个。由于不同基因的末端可以由不同的限制酶所产生,因而为了减少分子克隆的工作量,科学家们构建了具有多个克隆位点的载体,而且将多个克隆位点集中在一个很短的序列内,这种序列常常被称之为多克隆位点区(multiple cloning site)。有关多克隆位点区的详细情况见后述。
克隆载体的标记基因
当试图把一个载体DNA或重组DNA分子导入某种宿主细胞时,我们如何知道载体或重组DNA分子已经进入了宿主细胞?标记基因就能起到这个作用。获得了外源DNA分子进入的细胞被称之为转化细胞。标记基因往往可以赋予宿主细胞一种新的表型,这种转化细胞可明显地区别于非转化细胞:转化细胞有了新的表型,而非转化细胞仍保持原有的表型。这种表型的区别往往是选择性的,即只有转化细胞才能在研究者提供的生长条件下生长,而那些没有载体DNA分子进入的细胞就不能在相同的生长条件下生长,因此,转化细胞和非转化细胞是十分容易区别开来的(详见下述)。这是标记基因最重要的功能,即指示哪些细胞是转化细胞。
标记基因还有一个十分重要的功能,即指示外源DNA分子是否插入载体分子形成了重组子。换句话说,当我们把一个DNA片段插入到某一个标记基因内时,该基因就失去了相应的功能。当把这种重组DNA分子转到宿主细胞后,该基因原来赋予的表型也就消失了。要是仍保留了原来表型的转化细胞,细胞内含有的DNA分子一定不是重组子。很显然,既要指示外源DNA是否进入了宿主细胞,又要指示载体DNA分子中是否插入了外源DNA片段,那么这种载体必须至少具有两个标记基因。
上述的标记基因是针对一种生物而言的,那么当载体可用于多种生物时,一个载体就可以有多个标记基因,每个标记基因的用途是不相同的,不同的标记基因可能只适合于某种生物。比如植物的克隆载体就可能有3-4个标记基因。由于绝大多数标记基因都是分离自原核生物,因而这些标记基因要用于其它生物,还得对这些基因进行改造,即将基因的启动子和终止子换成另一种生物的基因启动子和终止子。
遗传标记基因的种类
现有的标记基因的种类很多,但可以将它们划分为以下三大类:
1)抗性标记基因。这类抗性基因可赋予宿主细胞对些物质的抗性,而这些物质对宿主细胞可能是致死的,因此,这类标记基因可直接用于选择转化子。这类基因又可分为以下3类:
i. 抗生素抗性基因。这类抗性基因常常赋予宿主细胞对抗生素产生抗性,而抗生素往往对宿主细胞是致死的,这类标记基因中常用的基因有:氨苄青霉素抗性基因(Apr)、四环素抗性基因(Tcr)、氯霉素抗性基因(Cm r)、卡那霉素抗性基因(Kanr)、G418抗性基因(G418r)、潮霉素抗性基因(Hygr)、新霉素抗性基因(Neor)。
ii. 重金属抗性基因。重金属对生物细胞是有毒的,但有的基因能产生一些可与重金属相结合的蛋白质,从而从环境中除去重金属。目前所用的重金属抗性基因有:铜抗性基因(Cur),锌抗性基因(Znr),镉抗性基因(Cdr)。
iii. 代谢抗性基因。抗除草剂基因,胸苷激酶基因(TK)。
在上述三种抗性标记基因中,抗生素抗性基因使用最为频繁,且适用范围很广,包括动物、植物和微生物。抗除草剂基因在植物中使用较为广泛。
2)营养标记基因。有的生物细胞因为突变而导致需要某些营养物质才能生长,其原因是参与某些营养物质合成的基因发生了突变。如果将没有发生突变的相应基因转入这种突变体细胞中,那么这些细胞就不再需要相应的营养物质,而那些未被转化的细胞则不能生长,因而这类标记基因也可直接用于选择转化子。
这类基因主要是参与氨基酸,核苷酸及其他必需营养物合成酶类的基因,在酵母转化中使用最频繁,如色氨酸合成酶基因(TRP1),尿嘧啶合成酶基因(URA3),亮氨酸合成酶基因(LEU2),组氨酸合成酶基因(HIS4)等。
3) 生化标记基因。这类标记基因的表达产物可催化某些易检测的生化反应,常用的基因有β-半乳苷酶基因(lacZ)、葡萄糖苷酸酶基因(GUS)、氯霉素乙酰转移酶基因(CAT)。
为了进一步说明载体的结构和各个结构的功能,下面举一个在基因工程中使用比较频繁的大肠杆菌载体—pBR322作为例子。
大肠杆菌载体pBR322
载体pBR322是由Bolivar 等人于1977年构建的。该载体长4362 bp,它有一个来自大肠杆菌中高拷贝天然质粒的复制起点(ori),这个复制起点可使pBR322在大肠杆菌中的拷贝数达到20个,因而pBR322载体的DNA很容易从大肠杆菌中提取出来。这是pBR322中的第一个结构特征。
图1 大肠杆菌克隆载体pBR322的物理图谱
此载体中有两个标记基因,一个是氨苄青霉素抗性基因(Apr),另一个是四环素抗性基因(Tcr)。氨苄青霉素和四环素都是人类治疗疾病的抗生素药物。当把pBR322 DNA转化大肠杆菌细胞,其中部分细胞就被该载体所转化,而有一部分细胞则没有被转化。如何区分这两种细胞呢?很简单,将转化后的细胞涂布在一种加有氨苄青霉素或四环素的培养基上,然后放在37° C下培养。由于转化细胞中有pBR322 DNA,该载体上的氨苄青霉素抗性基因和四环素抗性基因都会表达,那么这种转化细胞就能在加有氨苄青霉素或四环素的培养基上生长,于是就可以在培养基的表面看到相应的抗性菌落。菌落是由许多大肠杆菌细胞生长后堆积在一起,能为肉眼可见的生长物。那些没有被转化的细胞,因为细胞中没有pBR322,当然就没有两种抗性基因的表达,那么这些细胞就不能在加有氨苄青霉素或四环素的培养基上生长,因此我们也就无法获得未转化细胞的菌落。这样就很简单地将转化的细胞与非转化的细胞区别开来了。
现在再来看看pBR322的克隆位点。在这个载体中,ScaI、PstI、BamHI、SalI、 EcoRI和HindIII等6个限制酶位点都是唯一的,因此它们都可以用作克隆外源基因的位点。但是,在克隆外源基因的时候,选择不同的克隆位点将会获得不同的表型,筛选重组子的策略也是不相同的。究竟有何不同?
ScaI和PstI两个位点都位于氨苄青霉素抗性基因的编码区内。当一个外源基因片段插入这两个位点中的任何一个位点时,该抗性基因就会失去活性,这种重组子就再也不会赋予转化细胞以氨苄青霉素抗性,因此,这种重组子所转化的细胞就只能涂布在加有四环素的平板上。因为四环素抗性基因没有外源DNA插入,因此仍保留了生物学活性。
要是不把外源基因插入Apr基因中,而是将其插入Tcr基因中,结果会怎样?已知四环素抗性基因中有BamHI和SalI两个克隆位点,如果其中一个位点插入了外源基因片段,那么四环素抗性基因也就失去了活性,因此当把这种重组DNA分子转化大肠杆菌细胞,转化细胞就不能在四环素平板上生长,换句话说,这种转化细胞则只能涂布在加有氨苄青霉素的平板上。
另外还有两个位点EcoRI和HindIII,它们不在两种抗生素抗性基因的编码区内,因此外源基因插入这两个位点时不会引起标记基因的失活,所以转化细胞可以涂布在氨苄青霉素或四环素的平板上。由此可以看出,克隆位点不仅仅是供外源DNA分子插入的地方,而且将直接影响到后面的实验操作。
通过上面的叙述,我们已经知道基因工程的克隆载体中的三种基本结构和它们的功能。实际上,载体会因为在使用时的宿主细胞种类、实验用途不同而有较大差别,但这三种基本结构是最基本的。
克隆载体的种类
自1977年Bolivar等人组建了第一个系列的克隆载体pBR以来,已建立起各种不同的分子克隆载体用于不同的研究目的和不同的生物种类。
如果按照载体的复制子来源划分,所有的载体可分为以下三种类型:
1) 质粒型载体:这一类载体所含的复制起点主要来自不同的原核生物,特别是大肠杆菌和一些低等真核生物(如酵母菌和一些丝状真菌)中的质粒DNA。有的复制起点则来自染色体DNA(如酵母菌)。许多载体DNA上只含有一种复制起点,如用于大肠杆菌的pBR和pUC系列质粒载体,然而有的克隆载体却含有两种复制子顺序,它们常来自于不同的生物,比如大肠杆菌-酿酒酵母(Saccharomyces cerevisiae)穿梭载体YRp12 和YEp13等,这类载体能在这两种不同的生物中自主复制。
2) 病毒型载体:这类载体中所含的复制起点是来自病毒DNA。在大肠杆菌中,以噬菌体λ所组建的charon系列,λEMBL和λNM系列载体和以单链DNA噬菌体M13组建的M13mp系列载体。在动物细胞中,也有好几种病毒复制被用来组建克隆载体。
3) 混合型载体:这类载体复制起点来自质粒和病毒,比如适合于大肠杆菌的DNA载体pEMBL8和pEMBL9含有质粒pMB1和单链噬菌体f1复制起点。 用于动物细胞的DNA载体则含有大肠杆菌的质粒复制和动物病毒复制起点。 使用得最广泛的动物病毒复制起点来源子SV40。实际上,这类混合型载体也是穿梭型的,即它们既可以在大肠杆菌中复制,亦可在动物细胞中复制。
要是按照克隆载体的功能或用途来划分,则可将DNA载体分为以下两大类:
1) 普通型载体:这类载体主要用于各种基因组文库和cDNA文库的建立, 比如常用的pBR322,由λ衍生的载体和COs质粒,以及一些大肠杆菌- 酿酒酵母穿梭载体, 如YRp7,YEp13等。染色体DNA片段或cDNA均可用这类载体进行增殖。它们通常含有两个或两个以上的标记基因,其中一个基因用于选择转化体(transformant),另一基因则是用于检查载体中是否有外源DNA插入。
2) 表达型基因(expression vector):这类载体主要用于研究基因的表达或是用于大量生产一些有用的转录产物或蛋白质,有的也可用于cDNA文库的建立。这类载体除具有普通型载体的特征外,它还含有某些基因的启动子序列,有的还含有转录终止子序列,为了基因表达产物便于检测或是为了简化基因表达产物的分离纯化,有的表达型载体除含有基因启动子序列外,它还有一段为信号肽链编码的DNA序列,这段信号肽链可以使蛋白质分必到细胞外。 这类载体又可称为分泌表达型载体(Secretion expression vector)。为了使某些基因产物能投入大规模的工业生产,科学家们已组建了各种高效表达的分泌型载体。
图1 大肠杆菌克隆载体pBR322的物理图谱