看完《我不是药神》,聊聊新药审核背后的利益交易
丁香园
上个周末,我去影院二刷《我不是药神》,电影中跨国制药公司在癌症患者面临生死的时候,依然阻不顾一切打击仿制药的走私。事实上,电影没有说明的是,这款天价药背后数十亿美元的研发成本和一次次失败的试验,如果没有没有专利加身维持暴利,制药公司可能就入不敷出了,那以后谁来研制新药呢?
这场刷屏的电影引发了民众关于药物的讨论和深思,这就是电影的价值。一周前,另外一个事件也让药品问题走进了民众的视线,只不过,是另一个角度。
科研界大佬 Science 杂志连续报道了美国新药审核上市过程中存在的暗箱操作与利益输送,引发业界及一众看客的轩然大波,尤其在新药立法上市制度历经波折饱受诟病、国家药监局前领导被处极刑的中国生物医疗及制药行业,关于药物的讨论从业界到民众再次站在了风口。

图片来源:quanjing.com
01 Science :新药审批的交易
Science 在 2018 年 7 月 6 日的封面文章中,从个案到统计,有点有面地揭露了美国食品药品监督管理局 FDA 和药品企业在新药审批手续上存在的利益输送。文章指名道姓地列举了审核人员与药企之间的交易数额、药品名称、交易手段等等,从统计数据到图表分析,Science 怼起人来也是严丝合缝毫不含糊,一副求锤给锤负责到底,让人无法反驳架势,从下图中可以随意感受一下 Science 优美地展示医疗服务机构利益输送金额。
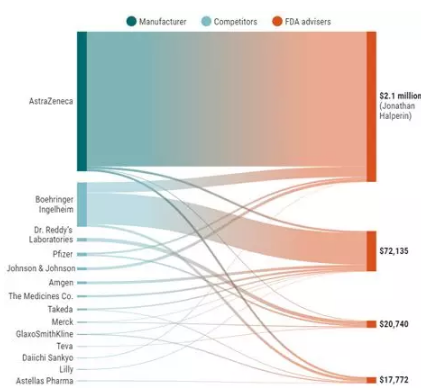
某种预防心血管血栓新药赞助 FDA 参与审批的医生并最终获得通过
图片来源:Science 官网
根据 Science 的爆料,赞助费也是名目众多,不但有 「酬金」「研究赞助」 大众熟知的直白利益输送方式,还有 「旅游费」「车马费」「咨询费」 等巧立名目的形式,让中国看客不禁感慨太阳底下无新事。在事情发酵的这几天,也有不少评论指出 Science 的爆料并非完全处于公义,被揭露的特定冰山一角只不过是利益集团博弈的一部分罢了。
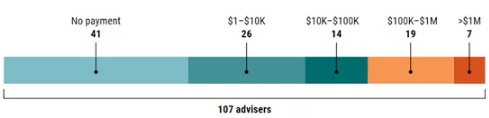
药物生产商 2008 年至 2014 年间向 FDA 的 107 名医生支付各种名目费用分布
图片来源:Science 期刊官网
02 中国的药物监管与审批
从十年前中国药监局(CFDA)局长郑筱萸的死刑开始,中国的制药行业就对标号称体系最完善的美国药物监管体系,引进国际化的监管团队,对我国药物审批过程中临床数据真实性进行反复核查。
但事实上,我国药品监管以及新药上市的流程以及工作成效至今还面临巨大争议,尤其是在涉及中药材、中药饮片、中成药等相关领域上,中国并没有完全可以照搬的成熟经验,这让普通民众在对机制存在质疑的情况下对药品的疗效和安全性产生了不信任。
相关数据表明,中国游客在日本购买最多的几类商品就包括药品和保健类食品,不时出现的海外药品店限购或者断货的新闻也正在印证中国消费者对国产药物的不满。另一方面,这种不信任加之公众对药品的理解偏差使得各种 「XX 药酒」「XX 口服液」 有了巨大的生存空间,形形色色打着治疗旗号的食品药品保健品在民间肆意横行。

图片来源:shutterstock.com
事实上,我国医药行业低水平重复生产、流通领域中层层加码药品价格虚高、医院以药养医模式难以消除的现状在这十年内有了很大改观,但唯独在新药审批上市这方面的争议从来都没有停止过,每一个涉及 「药物」 的热点出现中国的新药审批制度都会被拿出来探讨一番。
中国对药品监督和审核推行的是 GMP。GMP 是国际上对《药品生产质量管理规范》Good Manufacturing Practice 的简称,GMP 是世界各国对药品生产全过程监督管理时普遍采用的法定技术规范,是保证药品质量的可靠措施。
中国修订发布的《中华人民共和国药品管理法》规定,药品生产必须按照 GMP 组织生产,并对监督实施办法和实施步骤提出具体规定和要求。监督实施 GMP 可以从整体上提高我国制药工业的水平,保证人民群众的用药安全,缩小与发达国家制药工业的差距,同时也将使不符合 GMP 要求的企业停产、关闭,有效制止药品生产领域的低水平重复建设。
客观地说,对于民众以及中国制药行业 GMP 的推行是毋庸置疑的利好,但各种利益集团间的冲突,观念的冲突让中国的 GMP 之路也被各种交易、操纵以及利益输送等负面问题困扰,显得步履维艰。

图片来源:quanjing.com
大量药效和作用机制不明的保健食品在宣传中号称具有治疗功能并受到公众的追捧。
03 新药之殇
从 Science 的爆料可以看出,即便是被认为最发达最成熟的美国新药上市审批体系都存在着巨大的漏洞,这一漏洞是根源性的。
一方面 GMP 过程的裁判员和规则制定员都是政府的药监部门,集中的权力给寻租带来了空间,另一方面新药上市过程高度的专业性和复杂性让新药的审批过程很难被通过机制性流程实现无死角监管。
国际通行的新药上市一般经过四个主要步骤:化学合成研究 - 动物实验 - 人体试验 - 管理局审核,这其中最后两个环节涉及人的主观判断很难做到没有任何偏好以及无个体差异的完全准确客观,Science 提供的案例中 1 个人体实验患者和 7 个专业审核人员的判断出现冲突时,最终是按照多人的意见对新药予以审批通过,而一种新药是否应该以服从多数的方式做裁决,本身就是一个尚未完全解决也不可能彻底解决的问题。

《我不是药神》剧照
被利益操纵的还远不止审批过程中的利益输送,新中药和新化学药的专利申请及保护体系中的利益输送,新药原始资料认定体系中的利益输送,各种利益与诉求的激烈对撞使得药物被无数看不见的手推动着,交易无处不在而最终呈现出来的只是一个合力。
涉及新药的伦理问题远不止这些,除了判断标准的科学性论证,各种仿药甚至缺陷药物的巨大需求,各国新药保护周期与政策的差异等等,都使得任何一个国家的新药上市与保护伴都随着巨大的非议,道阻且长。