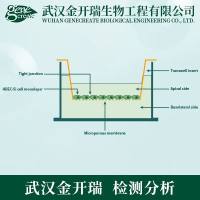
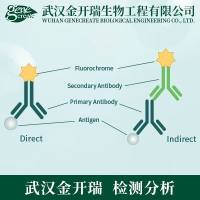
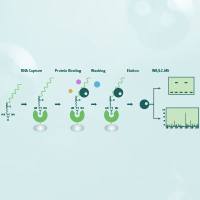
原理
血清葡萄糖能与白蛋白及其它血清蛋白分子N末端的氨基上发生非酶促糖化反应,形成高分子酮胺结构.此酮胺结构能在碱性溶液中与硝基四氮唑蓝(NBT)发生还原反应,生成用甲胺,并以1-脱氧―1―吗啉果糖(OMF)为标准参照物进行比色测定,本实验来源于牡丹江医学院 本科 5 年制检验专业实验指导
材料与仪器
步骤
一、实验试剂:
1、0.1mmol/L碳酸盐缓冲液,PH10.8:无水碳酸钠9.54g,碳酸氢钠0.84g, 溶于蒸馏水并稀释至1000ml。
2、0.11mol/L NBT试剂:称取氯化硝基氮唑蓝100mg,用于上述缓冲液溶解并稀释至1000mL.置冰箱保存,至少可稳定3个月;
3、4mmol/L DMF标准液:称取DMF99.6g,熔于40g/L牛血清白蛋白溶液100ml中.
二、实验操作:
测定管加待检血清(血浆)0.1ml,空白管加蒸馏水0.1ml,各加37℃预温的NBT试剂4ml,混匀,置37℃水浴准确15min,立即取出,流水冷却(低于25℃),冷却后15分钟内分光光度计波长550nm,10nm光径比色杯以空白管调零,读取测定管.从标准曲线查得结果,以果糖胺mmol/L报告。
标准曲线制备:
取4mmol/L DMF标准液用牛血清蛋白溶液(40g/L)稀释成1、2、3、4mmol/L,并以血清蛋白,40g/L与测定管同样操作,读取各浓度DMF相应的吸光度,以DMF浓度为横坐标,吸光度为纵坐标,制成标准曲线。浓度在4mmol/L以内与吸光度呈线性关系.
参考值:1.9十0.25mmol/L
1、0.1mmol/L碳酸盐缓冲液,PH10.8:无水碳酸钠9.54g,碳酸氢钠0.84g, 溶于蒸馏水并稀释至1000ml。
2、0.11mol/L NBT试剂:称取氯化硝基氮唑蓝100mg,用于上述缓冲液溶解并稀释至1000mL.置冰箱保存,至少可稳定3个月;
3、4mmol/L DMF标准液:称取DMF99.6g,熔于40g/L牛血清白蛋白溶液100ml中.
二、实验操作:
测定管加待检血清(血浆)0.1ml,空白管加蒸馏水0.1ml,各加37℃预温的NBT试剂4ml,混匀,置37℃水浴准确15min,立即取出,流水冷却(低于25℃),冷却后15分钟内分光光度计波长550nm,10nm光径比色杯以空白管调零,读取测定管.从标准曲线查得结果,以果糖胺mmol/L报告。
标准曲线制备:
取4mmol/L DMF标准液用牛血清蛋白溶液(40g/L)稀释成1、2、3、4mmol/L,并以血清蛋白,40g/L与测定管同样操作,读取各浓度DMF相应的吸光度,以DMF浓度为横坐标,吸光度为纵坐标,制成标准曲线。浓度在4mmol/L以内与吸光度呈线性关系.
参考值:1.9十0.25mmol/L
注意事项
1、PH值、反应温度,反应时间对本实验影响较大,必须严格控制.
2、血清蛋白经非酶促糖化反应可形成酮胺结构。DMF在适当的PH值及温度条件下,经过结构重排可由氧环式结构形成1-脱氧-氨基-2-酮基的酮胺结构,因此用它作为标准参照物是合理的.以mmol/L报告结果较为理想.
3、固定值冻于精化血红蛋白做标准,测定结果更稳定,因为不同的标准物时所测得结果不完全一致,最好建立实验室的参考值。
2、血清蛋白经非酶促糖化反应可形成酮胺结构。DMF在适当的PH值及温度条件下,经过结构重排可由氧环式结构形成1-脱氧-氨基-2-酮基的酮胺结构,因此用它作为标准参照物是合理的.以mmol/L报告结果较为理想.
3、固定值冻于精化血红蛋白做标准,测定结果更稳定,因为不同的标准物时所测得结果不完全一致,最好建立实验室的参考值。
来源:丁香实验